名校
1 . 甲硝唑主要用作治疗或预防厌氧菌引起的系统或局部感染,结构简式如图所示,杂环中存在大 键。下列说法错误的是
键。下列说法错误的是
 键。下列说法错误的是
键。下列说法错误的是
A.该分子中①号 更易和盐酸形成盐,增大药物水溶性 更易和盐酸形成盐,增大药物水溶性 |
| B.该分子可发生加成反应、消去反应 |
| C.该分子中含有两种含氧官能团 |
| D.该分子是极性分子 |
您最近一年使用:0次
名校
2 . 下图是分别用 和
和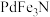 电催化甲酸间接氧化的反应历程,吸附在催化剂表面的粒子用
电催化甲酸间接氧化的反应历程,吸附在催化剂表面的粒子用 标注。下列说法
标注。下列说法错误 的是
 和
和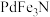 电催化甲酸间接氧化的反应历程,吸附在催化剂表面的粒子用
电催化甲酸间接氧化的反应历程,吸附在催化剂表面的粒子用 标注。下列说法
标注。下列说法 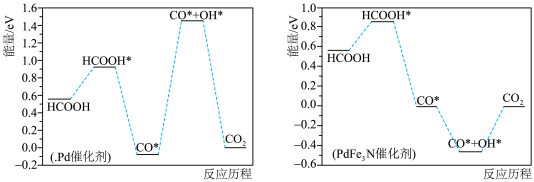
A. 为阳极产物之一 为阳极产物之一 | B.催化剂活性: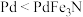 |
C. 催化剂比 催化剂比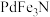 更难吸附 更难吸附 | D.消耗相同甲酸时,总反应焓变: |
您最近一年使用:0次
2024-06-04更新
|
130次组卷
|
2卷引用:福建省龙岩市2024届高三下学期5月质检化学试题
名校
解题方法
3 . 药物贝诺酯有消炎、镇痛、解热的作用,其制备原理为:
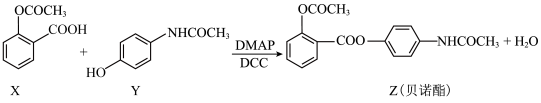
A.X与 加成后的产物不存在对映异构 加成后的产物不存在对映异构 |
| B.Y分子中所有碳原子不可能在同一平面 |
C.可用核磁共振氢谱确定 含有的官能团 含有的官能团 |
D.X、Y可用 溶液鉴别 溶液鉴别 |
您最近一年使用:0次
2024-06-04更新
|
205次组卷
|
2卷引用:福建省龙岩市2024届高三下学期5月质检化学试题
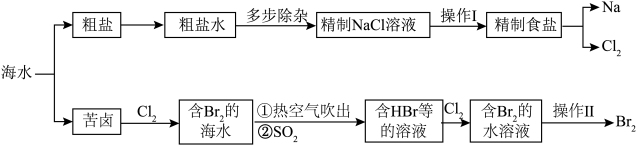
4 . 海水综合利用流程如图。请根据所学知识回答下列问题: 、
、 。
。
(1)多步除杂中所用除杂试剂为① 、②
、② 、③稀盐酸,由粗盐水得到精制NaCl溶液,应先向粗盐水中加入
、③稀盐酸,由粗盐水得到精制NaCl溶液,应先向粗盐水中加入___________ (填标号,下同),再加入___________ ,过滤后再加入___________ ,将精制NaCl溶液倒入___________ (填仪器名称)中进行蒸发结晶,即可得到NaCl。该过程中加入①的作用是___________ (用离子方程式表示)。
(2)写出通入 生成
生成 的离子方程式:
的离子方程式:___________ ;热空气吹出后加 还原及其后续工序,可用下列流程代替,请写出其优点:
还原及其后续工序,可用下列流程代替,请写出其优点:___________ (1条即可)。 。
。___________ 。
②说明Br的非金属性比I强的操作为___________ 。
 、
、 。
。(1)多步除杂中所用除杂试剂为①
 、②
、② 、③稀盐酸,由粗盐水得到精制NaCl溶液,应先向粗盐水中加入
、③稀盐酸,由粗盐水得到精制NaCl溶液,应先向粗盐水中加入(2)写出通入
 生成
生成 的离子方程式:
的离子方程式: 还原及其后续工序,可用下列流程代替,请写出其优点:
还原及其后续工序,可用下列流程代替,请写出其优点:
 。
。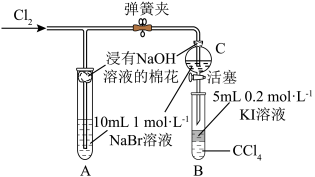
②说明Br的非金属性比I强的操作为
您最近一年使用:0次
5 . 下列实验装置或操作能达到实验目的的是
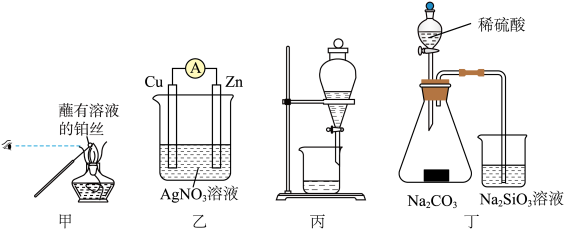
A.图甲:检验某溶液中是否含有 |
B.图乙:将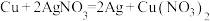 设计成原电池 设计成原电池 |
| C.图丙:用乙醇萃取碘水中的碘 |
D.图丁:验证非金属性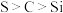 |
您最近一年使用:0次
6 . 工业制备高纯硅的流程如下,下列说法正确的是
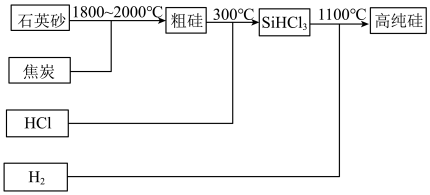
| A.粗硅与HCl反应时,需要在富氧的环境中进行 |
| B.盛装NaOH溶液的玻璃瓶需要使用磨口玻璃塞 |
C.制粗硅的化学方程式为 |
| D.高纯硅常用于制备光导纤维 |
您最近一年使用:0次
7 . 化学反应与生产研究息息相关。现有如下反应:
A.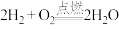
B.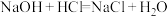
C.
D.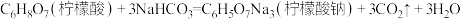
请根据要求,回答下列问题:
(1)上述反应中属于吸热反应的有___________ (填标号,下同);属于放热反应的有___________ 。
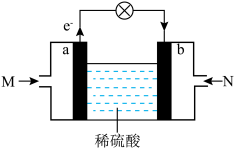
(2)能设计成原电池的反应为___________ ,其装置如图所示。___________ (填物质名称),a极上的电极反应式为___________ 。
②N为___________ (填物质名称),b极上的电极反应式为___________ 。
③电池工作时, 移向
移向___________ (填“a”或“b”)极。
④当负极消耗8gM时,导线中转移电子的物质的量为___________ mol。
A.
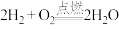
B.
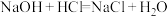
C.

D.
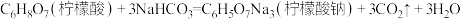
请根据要求,回答下列问题:
(1)上述反应中属于吸热反应的有
(2)能设计成原电池的反应为
②N为
③电池工作时,
 移向
移向④当负极消耗8gM时,导线中转移电子的物质的量为
您最近一年使用:0次
8 . A、B、C、D、E是原子序数依次增大的短周期主族元素,它们在元素周期表中的相对位置如表,已知C的内层电子总数是最外层电子数的2倍。
(1)C在元素周期表中的位置为___________ 。
(2)A、B、C的最简单氢化物的稳定性由弱到强的顺序是___________ (填化学式);用电子式表示出A的最简单氢化物的形成过程:___________ 。
(3)C、D、E的简单离子半径由大到小的顺序是___________ (填离子符号),画出C的简单离子的结构示意图:___________ 。
(4)实验室制取 气体的离子方程式为
气体的离子方程式为___________ 。
(5)工业上,A的最简单气态氢化物可用来检测输送 气体的管道是否泄漏,发生反应的现象为
气体的管道是否泄漏,发生反应的现象为___________ ,写出反应的化学方程式:___________ 。
| A | B | |
| C | D | E |
(2)A、B、C的最简单氢化物的稳定性由弱到强的顺序是
(3)C、D、E的简单离子半径由大到小的顺序是
(4)实验室制取
 气体的离子方程式为
气体的离子方程式为(5)工业上,A的最简单气态氢化物可用来检测输送
 气体的管道是否泄漏,发生反应的现象为
气体的管道是否泄漏,发生反应的现象为
您最近一年使用:0次
9 . 碱性锌锰电池的结构示意图如图,总反应为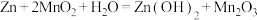 ,下列说法正确的是
,下列说法正确的是
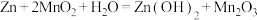 ,下列说法正确的是
,下列说法正确的是
| A.电池工作时,A极为负极 |
| B.该电池用完后可随意丢弃 |
| C.电池工作时,化学能完全转化成电能 |
D.电池工作时, |
您最近一年使用:0次
10 .  易溶于水,溶液呈中性,可用于制作替代氟利昂的绿色制冷剂,利用高浓度
易溶于水,溶液呈中性,可用于制作替代氟利昂的绿色制冷剂,利用高浓度 粗溶液合成
粗溶液合成 工艺流程如下。下列说法正确的是
工艺流程如下。下列说法正确的是
 易溶于水,溶液呈中性,可用于制作替代氟利昂的绿色制冷剂,利用高浓度
易溶于水,溶液呈中性,可用于制作替代氟利昂的绿色制冷剂,利用高浓度 粗溶液合成
粗溶液合成 工艺流程如下。下列说法正确的是
工艺流程如下。下列说法正确的是
| A.“还原”过程应加入过量BaS |
| B.“滤渣”中两种物质的物质的量相近 |
C. 晶体中存在4原子7电子构成的大 晶体中存在4原子7电子构成的大 键 键 |
D.“浓缩”过程需在 气流中进行 气流中进行 |
您最近一年使用:0次



