名校
解题方法
1 . 化学电源在生产生活中有着广泛的应用,请回答下列问题:
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
(2)为了探究化学反应中的能量变化,某同学设计了如下两个实验(如图)。有关反应一段时间后的实验现象,下列说法正确的是_______。
(3)请利用反应“Cu+2Ag+=Cu2++2Ag”设计一个化学电池(正极材料用碳棒),该电池的负极材料是_______ ,发生的电极反应是_______ ,电解质溶液是_______ 。
(4)正极上出现的现象是_______ 。
(5)若导线上转移电子1 mol,则生成银_______  。
。
(1)根据构成原电池的本质判断,下列化学(或离子)方程式正确且能设计成原电池的是_______(填字母,下同)。
A.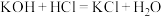 | B. |
C.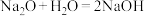 | D. |
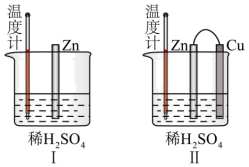
| A.图Ⅰ中温度计的示数高于图Ⅱ的示数 |
| B.图Ⅰ和图Ⅱ中温度计的示数相等,且均高于室温 |
| C.图Ⅰ和图Ⅱ的气泡均产生于锌棒表面 |
| D.图Ⅱ中产生气体的速率比Ⅰ慢 |
(4)正极上出现的现象是
(5)若导线上转移电子1 mol,则生成银
 。
。
您最近一年使用:0次
2 . 下列不属于取代反应的是
A.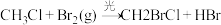 |
B.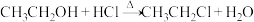 |
C.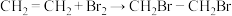 |
D.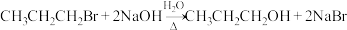 |
您最近一年使用:0次
名校
3 . NA是阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下22.4 L H2SO4中所含原子数为7NA |
| B.3 mol NO2与H2O完全反应时转移的电子数为2NA |
| C.11.2 LNO与11.2 LO2混合气体的分子数为NA |
| D.78 g Na2O2中含有的离子总数为3NA |
您最近一年使用:0次
名校
解题方法
4 . 下列说法正确的是
A.甲烷的球棍模型为 |
B. 和 和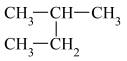 互为同系物 互为同系物 |
C.丙烷的空间填充模型为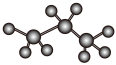 |
D.乙烷的结构简式为: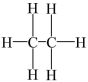 |
您最近一年使用:0次
名校
5 .  代表阿伏加德罗常数,下列说法不正确的是
代表阿伏加德罗常数,下列说法不正确的是
 代表阿伏加德罗常数,下列说法不正确的是
代表阿伏加德罗常数,下列说法不正确的是A.一定条件下,将 和 和 混合反应生成 混合反应生成 ,转移的电子总数为 ,转移的电子总数为 |
B. 中含有的氧氢键数为 中含有的氧氢键数为 |
C.常温下,71g氯气含有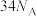 个电子 个电子 |
D.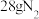 和 和 组成的混合气体中含有的原子数为 组成的混合气体中含有的原子数为 |
您最近一年使用:0次
名校
解题方法
6 . 归纳、演绎和模型等是化学学习的重要方法,回答下列问题。
元素的“价-类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价-类”二维图。
(1)Y的化学式为__________ 。
(2)根据“价-类”二维图预测,下列能与 反应且
反应且 表现氧化性的物质是
表现氧化性的物质是__________ (填序号), 与其反应的化学方程式是
与其反应的化学方程式是__________ 。
a. b.酸性
b.酸性 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液
(3)分析 的物质类别,写出它和少量NaOH溶液反应的离子方程式
的物质类别,写出它和少量NaOH溶液反应的离子方程式_______________ 。
(4)从 转化为X的化学方程式为
转化为X的化学方程式为________ ,由 制备X的过程中,一般用
制备X的过程中,一般用___________ 吸收 ,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
元素的“价-类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价-类”二维图。

(1)Y的化学式为
(2)根据“价-类”二维图预测,下列能与
 反应且
反应且 表现氧化性的物质是
表现氧化性的物质是 与其反应的化学方程式是
与其反应的化学方程式是a.
 b.酸性
b.酸性 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液(3)分析
 的物质类别,写出它和少量NaOH溶液反应的离子方程式
的物质类别,写出它和少量NaOH溶液反应的离子方程式(4)从
 转化为X的化学方程式为
转化为X的化学方程式为 制备X的过程中,一般用
制备X的过程中,一般用 ,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
,防止反应放出大量的热导致形成酸雾,降低吸收效率且腐蚀设备。
您最近一年使用:0次
名校
7 . 某化学兴趣小组用下图装置(部分夹持装置已略去)制取氨气并探究其性质。___________ (填化学式)。
(2)装置B中的干燥剂可以选用___________ 。
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是_______ 。
(4)当E装置中集满 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是_________ 。
(5)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。______________ ,证明氨气具有__________ (填“氧化性”或“还原性”)。
②若向a中通入标准状况下3.36L的氨气,理论上会得到铜的质量为__________ g。
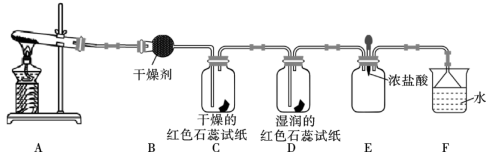
(2)装置B中的干燥剂可以选用
(3)气体通过C、D装置时,试纸颜色会发生变化的是D,原因是
(4)当E装置中集满
 时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是
时,挤压胶头滴管,滴入1~2滴浓盐酸,可观察到的现象是(5)用下图装置探究氨气与氧化铜的反应,验证氨气的性质及部分反应产物。

②若向a中通入标准状况下3.36L的氨气,理论上会得到铜的质量为
您最近一年使用:0次
名校
解题方法
8 . 下列离子方程式正确的是
A. 通入水中: 通入水中: |
B.Fe溶于过量的浓硝酸溶液中: |
C.用热NaOH溶液洗涤试管内壁的硫黄: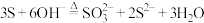 |
D.向 溶液通入足量 溶液通入足量 : :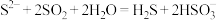 |
您最近一年使用:0次
名校
解题方法
9 . 某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如下表:
Ⅰ.合成苯甲酸甲酯粗产品
在圆底烧瓶中加入12.2g苯甲酸和20mL甲醇(密度约为0.79 ),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
(1)浓硫酸的作用是_______________ 。
(2)甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。________ (填“甲”或“乙”),理由是________________ 。
(3)反应物 应过量,理由是
应过量,理由是________________ 。
Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请写出流程图中操作方法的名称。_______________ ;操作Ⅱ________________ 。
(5)以上流程图中加入 溶液后,放入分液漏斗中振荡,静置,要得到有机层,要先打开分液漏斗上口的玻璃塞,再旋开
溶液后,放入分液漏斗中振荡,静置,要得到有机层,要先打开分液漏斗上口的玻璃塞,再旋开_______________ ,用锥形瓶接收下层液体,待下层液体刚好流尽时关闭活塞,将有机层(上层)从______________ 倒入指定容器中。
(6)通过计算,苯甲酸甲酯的产率为___________ 。
物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
沸点/℃ | 64.7 | 249 | 199.6 |
在圆底烧瓶中加入12.2g苯甲酸和20mL甲醇(密度约为0.79
 ),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。
),再小心加入3mL浓硫酸,混匀后,投入几块碎瓷片,小心加热使反应完全,得苯甲酸甲酯粗产品。(1)浓硫酸的作用是
(2)甲和乙两位同学分别设计了如图所示的两套实验室合成苯甲酸甲酯的装置(夹持仪器和加热仪器均已略去)。
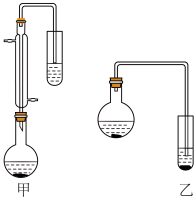
(3)反应物
 应过量,理由是
应过量,理由是Ⅱ.粗产品的精制
(4)苯甲酸甲酯粗产品中往往含有少量甲醇、苯甲酸和水等,现拟用下列流程图进行精制,请写出流程图中操作方法的名称。
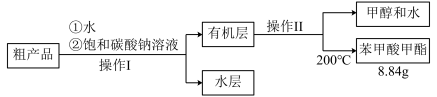
(5)以上流程图中加入
 溶液后,放入分液漏斗中振荡,静置,要得到有机层,要先打开分液漏斗上口的玻璃塞,再旋开
溶液后,放入分液漏斗中振荡,静置,要得到有机层,要先打开分液漏斗上口的玻璃塞,再旋开(6)通过计算,苯甲酸甲酯的产率为
您最近一年使用:0次
名校
10 . 回答下列问题:
(1)磷酸亚铁锂电池的新能源汽车对减少二氧化碳排放和大气污染具有重要意义。工业上用 、
、 、LiCl及苯胺
、LiCl及苯胺 为原料制磷酸亚铁锂电池材料。
为原料制磷酸亚铁锂电池材料。 核外电子排布式为
核外电子排布式为_________________________ , 的空间构型为
的空间构型为_____________ ; 中P的杂化轨道类型是
中P的杂化轨道类型是___________ ;O、P、Cl原子的半径最大的是___________ ,苯胺中碳和氮第一电离能较大的是___________ 。(填元素符号)
(2)Cu与Cl形成的一种化合物的立方晶胞如图所示。_________ ,已知晶胞参数a=0.542nm,此晶体的密度为_______________  。(写出计算式,不要求计算结果。阿伏加德罗常数为
。(写出计算式,不要求计算结果。阿伏加德罗常数为 )
)
②该化合物难溶于水但易溶于氨水,其原因是_____________ 。此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_____________ 。
(1)磷酸亚铁锂电池的新能源汽车对减少二氧化碳排放和大气污染具有重要意义。工业上用
 、
、 、LiCl及苯胺
、LiCl及苯胺 为原料制磷酸亚铁锂电池材料。
为原料制磷酸亚铁锂电池材料。 核外电子排布式为
核外电子排布式为 的空间构型为
的空间构型为 中P的杂化轨道类型是
中P的杂化轨道类型是(2)Cu与Cl形成的一种化合物的立方晶胞如图所示。
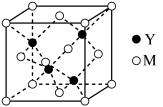
 。(写出计算式,不要求计算结果。阿伏加德罗常数为
。(写出计算式,不要求计算结果。阿伏加德罗常数为 )
)②该化合物难溶于水但易溶于氨水,其原因是
您最近一年使用:0次



