解题方法
1 . 下列实验操作及现象与对应结论不匹配的是
| 实验操作 | 现象 | 结论 | |
| A | 加热麦芽糖和稀硫酸的混合溶液,冷却后加入NaOH溶液至碱性,再加入银氨溶液,加热 | 有银镜产生 | 水解产物中一定含有还原糖 |
| B | 将TiCl4液体和FeCl3固体分别暴露在潮湿空气中 | 只有前者会冒“白烟” | 水解程度:TiCl4>FeCl3 |
| C | 向0.1mol/LNaOH溶液滴入MgSO4溶液至不再有沉淀产生,再滴加0.1mol/LCuSO4溶液 | 先有白色沉淀生成,后变为浅蓝色沉淀 |  |
| D | 在硬质试管中对石蜡油加强热,将产生的气体通入酸性KMnO4溶液中 | 酸性KMnO4溶液褪色 | 气体中含有不饱和烃 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2 . 某抗氧化剂Z可由如图反应制得:
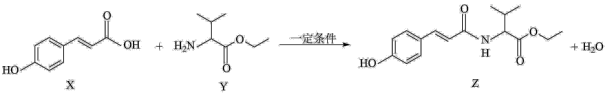
| A.Y中元素的电负性:O>C>H |
| B.X和Y均含有1个手性碳原子 |
| C.X可以发生加聚反应,也可以发生缩聚反应 |
D.一定条件下,1mol Z与足量 水溶液反应,最多消耗3mol 水溶液反应,最多消耗3mol |
您最近一年使用:0次
名校
3 . 2020年9月22日,中国政府在第75届联合国大会上提出:“中国将提高国家自主贡献力度,采取更有力的政策和措施。二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。” 碳中和也叫碳补偿(Carbon Offset),是现代人为减缓全球变暖所作的努力之一。碳中和的实现方式包括两种:一是通过植树造林等方式增加CO2的吸收量,二是通过技术手段减少CO2的排放量。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) ⇌ CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)⇌ CO(g)+H2O(g) △H1=+41kJ·mol-1
②CO(g)+2H2(g) ⇌ CH3OH(g) △H2= —99kJ·mol-1
(1)总反应的
_______ kJ·mol-1;
(2)氢氧燃料电池具有启动快,效率高等优点,若电解质为酸性,氢氧燃料电池的正极反应为_______
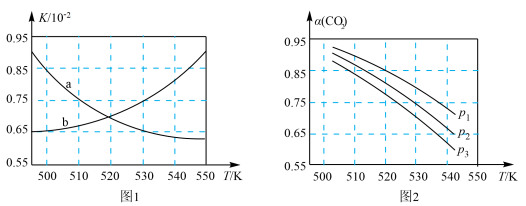
(3)图1中能正确反映平衡常数K随温度变化关系的曲线为_______ (填曲线标记字母),体系中的CO2平衡转化率(a)与温度和压强的关系如图2所示,则图2中的压强由大到小为_______ 。_______ (用含a的式子表示)。
Ⅱ. 和
和 的催化重整对温室气体的减排具有重要意义,其反应为:
的催化重整对温室气体的减排具有重要意义,其反应为: 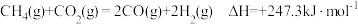 。回答下列问题:
。回答下列问题:
(5)该反应体系的熵值变化为_______ (填“增加”或“减小”);根据公式△G=△H—T△S判断:此反应在_______ (填“低温”或“高温”)条件下可以自发进行。
(6)其它条件相同,在不同催化剂(A、B)作用下,反应 进行相同时间后,
进行相同时间后, 的产率随反应温度的变化如图3所示。
的产率随反应温度的变化如图3所示。_______ ,在催化剂A、B作用下,它们反应活化能分别用 、
、 表示,则
表示,则
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(7)将原料 和
和 按等物质的量充入密闭容器中,保持体系压强为
按等物质的量充入密闭容器中,保持体系压强为 发生反应:
发生反应: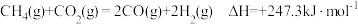 。达到平衡时,
。达到平衡时, 体积分数与温度的关系如图4所示,则在
体积分数与温度的关系如图4所示,则在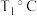 、
、 下,达平衡时
下,达平衡时 转化率=
转化率=_______ 。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) ⇌ CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)⇌ CO(g)+H2O(g) △H1=+41kJ·mol-1
②CO(g)+2H2(g) ⇌ CH3OH(g) △H2= —99kJ·mol-1
(1)总反应的

(2)氢氧燃料电池具有启动快,效率高等优点,若电解质为酸性,氢氧燃料电池的正极反应为
(3)图1中能正确反映平衡常数K随温度变化关系的曲线为
Ⅱ.
 和
和 的催化重整对温室气体的减排具有重要意义,其反应为:
的催化重整对温室气体的减排具有重要意义,其反应为: 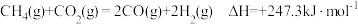 。回答下列问题:
。回答下列问题:(5)该反应体系的熵值变化为
(6)其它条件相同,在不同催化剂(A、B)作用下,反应
 进行相同时间后,
进行相同时间后, 的产率随反应温度的变化如图3所示。
的产率随反应温度的变化如图3所示。 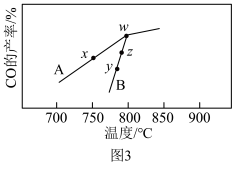
 、
、 表示,则
表示,则
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(7)将原料
 和
和 按等物质的量充入密闭容器中,保持体系压强为
按等物质的量充入密闭容器中,保持体系压强为 发生反应:
发生反应: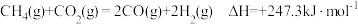 。达到平衡时,
。达到平衡时, 体积分数与温度的关系如图4所示,则在
体积分数与温度的关系如图4所示,则在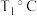 、
、 下,达平衡时
下,达平衡时 转化率=
转化率=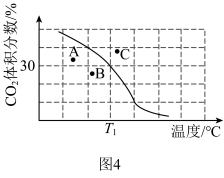
您最近一年使用:0次
名校
解题方法
4 . 下列离子方程式正确的是
A.向Na2SiO3溶液中通入过量CO2: |
B.将等物质的量浓度的 和NH4HSO4溶液以体积比 和NH4HSO4溶液以体积比 混合: 混合: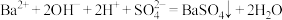 |
C.FeO溶于稀HNO3溶液: |
D.向AlCl3溶液中滴加过量NaOH溶液: |
您最近一年使用:0次
昨日更新
|
204次组卷
|
2卷引用:湖南省名校联考联合体2023-2024学年高一下学期5月期中联合考试化学试题
名校
5 . ClO-结合H+ 弱于CO ,下列反应的离子方程式
,下列反应的离子方程式正确 的是
 ,下列反应的离子方程式
,下列反应的离子方程式A.向次氯酸钠溶液中通入少量二氧化碳气体: |
B.K2CO3水解:CO + 2H2O ⇌ H2CO3 + 2OH- + 2H2O ⇌ H2CO3 + 2OH- |
C.用惰性电极电解饱和 溶液:2Cl- + 2H2O = H2↑ + Cl2↑ + 2OH- 溶液:2Cl- + 2H2O = H2↑ + Cl2↑ + 2OH- |
D. 溶液中加入过量浓氨水: 溶液中加入过量浓氨水: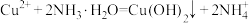 |
您最近一年使用:0次
名校
6 . 多巴胺是一种神经传导物质,会传递兴奋及开心的信息,其部分合成路线如下图,下列说法正确 的是
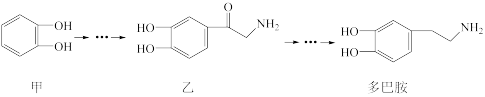
A.多巴胺的分子式为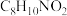 |
| B.甲分子的核磁共振氢谱有4组峰 |
C.甲能与 发生加成反应,且1mol甲最多能消耗2molH2 发生加成反应,且1mol甲最多能消耗2molH2 |
| D.多巴胺分子中含两种官能团,分别是酚羟基和氨基 |
您最近一年使用:0次
名校
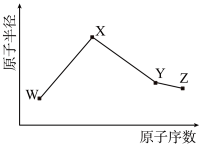
7 . W、X、Y、Z是元素周期表中的四种短周期元素,其相关信息及原子半径与原子序数的关系如表所示。请回答下列问题:
(1)W与X形成的含有共价键的常见化合物的电子式为_______ 。
(2)Y的价层电子排布式_______ 。
(3)Z的简单氢化物沸点比同主族上一周期元素简单氢化物沸点要_______ (填“高”或“低”)
(4)CuS晶胞中 的位置如图1所示,
的位置如图1所示, 位于顶点和面心,
位于顶点和面心, 位于
位于 所构成的四面体中心,晶胞侧视图如图2所示。
所构成的四面体中心,晶胞侧视图如图2所示。 距离最近的
距离最近的 数目为
数目为_______ 。
② CuS的晶胞参数为apm,阿伏加德罗常数的值为 ,则CuS晶体的密度为
,则CuS晶体的密度为_______  。
。
| 元素 | 相关信息 | 原子半径与原子序数的关系 |
| W | 其一种核素的质量数为18,中子数为10 |
|
| X | 其原子与电子排布式为1s22s22p6的原子的核外电子数相差1 | |
| Y | 其单质是一种常见的半导体材料 | |
| Z | 电负性在同周期元素中最大 |
(1)W与X形成的含有共价键的常见化合物的电子式为
(2)Y的价层电子排布式
(3)Z的简单氢化物沸点比同主族上一周期元素简单氢化物沸点要
(4)CuS晶胞中
 的位置如图1所示,
的位置如图1所示, 位于顶点和面心,
位于顶点和面心, 位于
位于 所构成的四面体中心,晶胞侧视图如图2所示。
所构成的四面体中心,晶胞侧视图如图2所示。
 距离最近的
距离最近的 数目为
数目为② CuS的晶胞参数为apm,阿伏加德罗常数的值为
 ,则CuS晶体的密度为
,则CuS晶体的密度为 。
。
您最近一年使用:0次
名校
解题方法
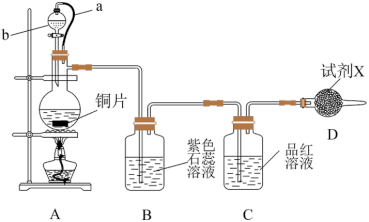
8 . 某校化学兴趣小组设计如图装置,实验探究浓硫酸与铜的反应。
___________ ,试剂X的名称是___________ 。
(2)橡皮管a的作用是___________ 。
(3)装置B中的现象是___________ ,装置C可检验SO2的性质为___________ 。
(4)实验结束后,小组成员发现烧瓶中的灰白固体中有少量黑色固体,将固体加入至水中后,发现白色固体溶解,而黑色固体不溶,便推测黑色固体可能是难溶于水及酸的CuS或 。于是设计如下实验进行进一步探究:
。于是设计如下实验进行进一步探究:___________ (填化学式)
②写出黑色固体X与足量 反应生成Y和Z的化学方程式
反应生成Y和Z的化学方程式___________ 。
(2)橡皮管a的作用是
(3)装置B中的现象是
(4)实验结束后,小组成员发现烧瓶中的灰白固体中有少量黑色固体,将固体加入至水中后,发现白色固体溶解,而黑色固体不溶,便推测黑色固体可能是难溶于水及酸的CuS或
 。于是设计如下实验进行进一步探究:
。于是设计如下实验进行进一步探究:
②写出黑色固体X与足量
 反应生成Y和Z的化学方程式
反应生成Y和Z的化学方程式
您最近一年使用:0次
名校
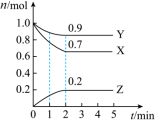
9 . 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的物质的量随时间的变化曲线如图所示:___________
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为v(Z)=___________
(3)2min反应达到平衡时体系内的压强比起始时的压强___________ (填“增大”、“减小”或“无变化”,下同),平衡时混合气体密度和起始时相比___________ 。
(4)下列措施能减小反应速率的是___________。
(5)X的平衡转化率为___________
(6)恒温条件下,对于可逆反应:CO(g)+2H2(g) CH3OH(g),在体积固定的密闭容器中进行,达到平衡状态的标志的是___________
CH3OH(g),在体积固定的密闭容器中进行,达到平衡状态的标志的是___________
(7)某合成氨速率方程为:v=kc(N2)cX(H2)cY(NH3),根据表中数据,Y=___________
(2)反应从开始至2分钟,用Z的浓度变化表示的平均反应速率为v(Z)=
(3)2min反应达到平衡时体系内的压强比起始时的压强
(4)下列措施能减小反应速率的是___________。
| A.升高温度 | B.选择高效的催化剂 | C.恒容时充入氩气 | D.恒压时充入氩气 |
(6)恒温条件下,对于可逆反应:CO(g)+2H2(g)
 CH3OH(g),在体积固定的密闭容器中进行,达到平衡状态的标志的是___________
CH3OH(g),在体积固定的密闭容器中进行,达到平衡状态的标志的是___________| A.单位时间内生成nmolCH3OH的同时消耗2nmolH2 |
| B.混合气体的密度不再改变的状态 |
| C.混合气体的压强不再改变的状态 |
| D.混合气体的平均摩尔质量不再改变 |
| 实验 | c(N2)/mol·L-1 | c(H2)/mol·L-1 | c(NH3)/mol·L-1 | v/mol·L-1·s-1 |
| 1 | m | n | p | q |
| 2 | 2m | n | p | 2q |
| 3 | m | n | 0.1p | 10q |
| 4 | m | 2n | p | 2.828q |
您最近一年使用:0次
名校
解题方法
10 . Ⅰ.化学反应与能量变化对人类生产、生活有重要的意义。回答下列问题:
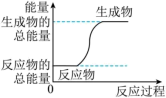
(1)下列化学反应中的能量变化关系与图示相符合的是___________。
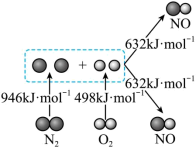
Ⅱ.汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示:___________ (填“吸收”或“放出”)___________ kJ热量,该反应的反应物的总能量___________ (填“大于”“等于”或“小于”)生成物的总能量。
Ⅲ.2023年6月9~11日,世界动力电池大会在宜宾举行,宜宾在电池研发、制造领域走在世界前列。利用原电池原理,人们研制出很多结构和性能各异的化学电池。回答下列问题:
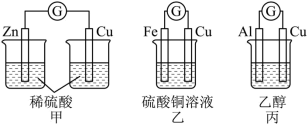
(3)某化学小组设计出如下图所示的甲、乙、丙三套装置。___________ 装置(填“甲”、“乙”或“丙”),该装置中Cu电极的电极反应式为___________ 。
(4)铅酸蓄电池放电时发生反应: 。该电池的负极材料为
。该电池的负极材料为___________ (填化学式)
(5)氢氧燃料电池的简易装置如下图所示。___________ (填“正极”或“负极”)。
②若线路中转移2mol电子,则该燃料电池理论上消耗的气体b在标准状况下的体积为___________ L。
(1)下列化学反应中的能量变化关系与图示相符合的是___________。
A.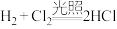 | B.天然气的燃烧 |
C. | D. |
Ⅱ.汽车发动机工作时会引发N2和O2反应,生成NOx等污染大气,其中生成NO的能量变化如图所示:
Ⅲ.2023年6月9~11日,世界动力电池大会在宜宾举行,宜宾在电池研发、制造领域走在世界前列。利用原电池原理,人们研制出很多结构和性能各异的化学电池。回答下列问题:
(3)某化学小组设计出如下图所示的甲、乙、丙三套装置。
(4)铅酸蓄电池放电时发生反应:
 。该电池的负极材料为
。该电池的负极材料为(5)氢氧燃料电池的简易装置如下图所示。
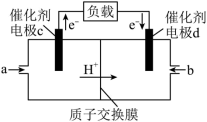
②若线路中转移2mol电子,则该燃料电池理论上消耗的气体b在标准状况下的体积为
您最近一年使用:0次