真题
1 .  是一种高活性的人工固氮产物,其合成反应为
是一种高活性的人工固氮产物,其合成反应为 ,晶胞如图所示,下列说法错误的是
,晶胞如图所示,下列说法错误的是
 是一种高活性的人工固氮产物,其合成反应为
是一种高活性的人工固氮产物,其合成反应为 ,晶胞如图所示,下列说法错误的是
,晶胞如图所示,下列说法错误的是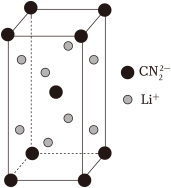
A.合成反应中,还原剂是 和C 和C |
B.晶胞中含有的 个数为4 个数为4 |
C.每个 周围与它最近且距离相等的 周围与它最近且距离相等的 有8个 有8个 |
D. 为V型结构 为V型结构 |
您最近一年使用:0次
真题
解题方法
2 . 丙烯腈( )是一种重要的化工原料。工业上以
)是一种重要的化工原料。工业上以 为载气,用
为载气,用 作催化剂生产
作催化剂生产 的流程如下:
的流程如下:
②反应釜Ⅰ中发生的反应:
ⅰ: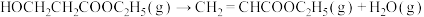

③反应釜Ⅱ中发生的反应:
ⅱ:

ⅲ: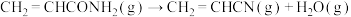

④在此生产条件下,酯类物质可能发生水解。
回答下列问题:
(1)总反应

_______ (用含 、
、 、和
、和 的代数式表示);
的代数式表示);
(2)进料混合气中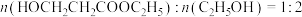 ,出料中四种物质(
,出料中四种物质( 、
、 、
、 、
、 )的流量,(单位时间内出料口流出的物质的量)随时间变化关系如图:
)的流量,(单位时间内出料口流出的物质的量)随时间变化关系如图: 的曲线是
的曲线是_______ (填“a”“b”或“c”);
②反应釜Ⅰ中加入 的作用是
的作用是_______ 。
③出料中没有检测到 的原因是
的原因是_______ 。
④反应 后,a、b、c曲线对应物质的流量逐渐降低的原因是
后,a、b、c曲线对应物质的流量逐渐降低的原因是_______ 。
(3)催化剂 再生时会释放
再生时会释放 ,可用氨水吸收获得
,可用氨水吸收获得 。现将一定量的
。现将一定量的 固体(含
固体(含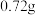 水)置于密闭真空容器中,充入
水)置于密闭真空容器中,充入 和
和 ,其中
,其中 的分压为
的分压为 ,在
,在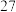 ℃下进行干燥。为保证
℃下进行干燥。为保证 不分解,
不分解, 的分压应不低于
的分压应不低于_______  (已知
(已知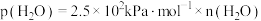
 分解的平衡常数
分解的平衡常数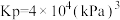 );
);
(4)以 为原料,稀硫酸为电解液,Sn作阴极,用电解的方法可制得
为原料,稀硫酸为电解液,Sn作阴极,用电解的方法可制得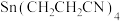 ,其阴极反应式
,其阴极反应式_______ 。
 )是一种重要的化工原料。工业上以
)是一种重要的化工原料。工业上以 为载气,用
为载气,用 作催化剂生产
作催化剂生产 的流程如下:
的流程如下:
②反应釜Ⅰ中发生的反应:
ⅰ:
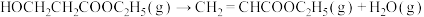

③反应釜Ⅱ中发生的反应:
ⅱ:


ⅲ:
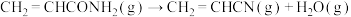

④在此生产条件下,酯类物质可能发生水解。
回答下列问题:
(1)总反应


 、
、 、和
、和 的代数式表示);
的代数式表示);(2)进料混合气中
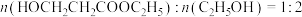 ,出料中四种物质(
,出料中四种物质( 、
、 、
、 、
、 )的流量,(单位时间内出料口流出的物质的量)随时间变化关系如图:
)的流量,(单位时间内出料口流出的物质的量)随时间变化关系如图:
 的曲线是
的曲线是②反应釜Ⅰ中加入
 的作用是
的作用是③出料中没有检测到
 的原因是
的原因是④反应
 后,a、b、c曲线对应物质的流量逐渐降低的原因是
后,a、b、c曲线对应物质的流量逐渐降低的原因是(3)催化剂
 再生时会释放
再生时会释放 ,可用氨水吸收获得
,可用氨水吸收获得 。现将一定量的
。现将一定量的 固体(含
固体(含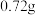 水)置于密闭真空容器中,充入
水)置于密闭真空容器中,充入 和
和 ,其中
,其中 的分压为
的分压为 ,在
,在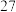 ℃下进行干燥。为保证
℃下进行干燥。为保证 不分解,
不分解, 的分压应不低于
的分压应不低于 (已知
(已知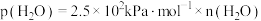
 分解的平衡常数
分解的平衡常数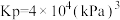 );
);(4)以
 为原料,稀硫酸为电解液,Sn作阴极,用电解的方法可制得
为原料,稀硫酸为电解液,Sn作阴极,用电解的方法可制得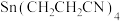 ,其阴极反应式
,其阴极反应式
您最近一年使用:0次
真题
3 . 组成核酸的基本单元是核苷酸,下图是核酸的某一结构片段,下列说法错误的是

| A.脱氧核糖核酸(DNA)和核糖核酸(RNA)结构中的碱基相同,戊糖不同 |
| B.碱基与戊糖缩合形成核苷,核苷与磷酸缩合形成核苷酸,核苷酸缩合聚合得到核酸 |
| C.核苷酸在一定条件下,既可以与酸反应,又可以与碱反应 |
| D.核酸分子中碱基通过氢键实现互补配对 |
您最近一年使用:0次
真题
4 . 常温下 ,向
,向 溶液中缓慢滴入相同浓度的
溶液中缓慢滴入相同浓度的 溶液,混合溶液中某两种离子的浓度随加入
溶液,混合溶液中某两种离子的浓度随加入 溶液体积的变化关系如图所示,下列说法错误的是
溶液体积的变化关系如图所示,下列说法错误的是
 ,向
,向 溶液中缓慢滴入相同浓度的
溶液中缓慢滴入相同浓度的 溶液,混合溶液中某两种离子的浓度随加入
溶液,混合溶液中某两种离子的浓度随加入 溶液体积的变化关系如图所示,下列说法错误的是
溶液体积的变化关系如图所示,下列说法错误的是
A.水的电离程度: |
B.M点: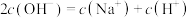 |
C.当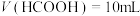 时, 时, |
D.N点: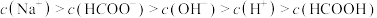 |
您最近一年使用:0次
真题
5 . 铜阳极泥(含有Au、 、
、 、
、 等)是一种含贵金属的可再生资源,回收贵金属的化工流程如下:
等)是一种含贵金属的可再生资源,回收贵金属的化工流程如下: 时,可忽略该离子的存在;
时,可忽略该离子的存在;
②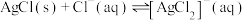
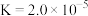 ;
;
③ 易从溶液中结晶析出;
易从溶液中结晶析出;
④不同温度下 的溶解度如下:
的溶解度如下:
回答下列问题:
(1)Cu属于_______ 区元素,其基态原子的价电子排布式为_______ ;
(2)“滤液1”中含有 和
和 ,“氧化酸浸”时
,“氧化酸浸”时 反应的离子方程式为
反应的离子方程式为_______ ;
(3)“氧化酸浸”和“除金”工序抣需加入一定量的 :
:
①在“氧化酸浸”工序中,加入适量 的原因是
的原因是_______ 。
②在“除金”工序溶液中, 浓度不能超过
浓度不能超过_______  。
。
(4)在“银转化”体系中, 和
和 浓度之和为
浓度之和为 ,两种离子分布分数
,两种离子分布分数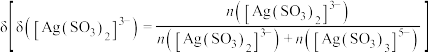 随
随 浓度的变化关系如图所示,若
浓度的变化关系如图所示,若 浓度为
浓度为 ,则
,则 的浓度为
的浓度为_______  。
。_______ (填化学式);在连续生产的模式下,“银转化”和“银还原”工序需在 ℃左右进行,若反应温度过高,将难以实现连续生产,原因是
℃左右进行,若反应温度过高,将难以实现连续生产,原因是_______ 。
 、
、 、
、 等)是一种含贵金属的可再生资源,回收贵金属的化工流程如下:
等)是一种含贵金属的可再生资源,回收贵金属的化工流程如下:
 时,可忽略该离子的存在;
时,可忽略该离子的存在;②
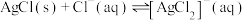
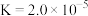 ;
;③
 易从溶液中结晶析出;
易从溶液中结晶析出;④不同温度下
 的溶解度如下:
的溶解度如下:温度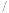 ℃ ℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 14.4 | 26.1 | 37.4 | 33.2 | 29.0 |
(1)Cu属于
(2)“滤液1”中含有
 和
和 ,“氧化酸浸”时
,“氧化酸浸”时 反应的离子方程式为
反应的离子方程式为(3)“氧化酸浸”和“除金”工序抣需加入一定量的
 :
:①在“氧化酸浸”工序中,加入适量
 的原因是
的原因是②在“除金”工序溶液中,
 浓度不能超过
浓度不能超过 。
。(4)在“银转化”体系中,
 和
和 浓度之和为
浓度之和为 ,两种离子分布分数
,两种离子分布分数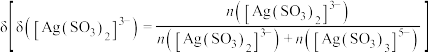 随
随 浓度的变化关系如图所示,若
浓度的变化关系如图所示,若 浓度为
浓度为 ,则
,则 的浓度为
的浓度为 。
。
 ℃左右进行,若反应温度过高,将难以实现连续生产,原因是
℃左右进行,若反应温度过高,将难以实现连续生产,原因是
您最近一年使用:0次
6 . 某种离子型铁的氧化物晶胞如图所示,它由A、B两种正方体单元构成,且两种正方体单元中氧离子的空间位置相同。通过Li+嵌入或脱嵌该晶胞的棱心和体心,可将该晶体设计为纳米硅基锂电池的正极材料 (m、n为正整数),已知:脱嵌率=
(m、n为正整数),已知:脱嵌率=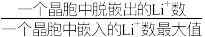 ×100%。
×100%。
 (m、n为正整数),已知:脱嵌率=
(m、n为正整数),已知:脱嵌率=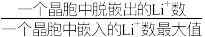 ×100%。
×100%。
| A.当Li+嵌入晶胞体心和所有棱心时,该锂电池正极材料的化学式为LiFe6O8 |
| B.若该锂电池正极材料中n(Fe2+):n(Fe3+)=5:7,则Li+的脱嵌率为75% |
C.该锂电池充电时阳极发生的反应为 |
| D.该锂电池放电时,每转移2mol e-,正极材料增重14g |
您最近一年使用:0次
7 . 根据我国农药毒性分级标准,精喹禾灵(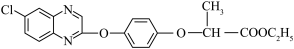 )属于低毒除草剂,作用速度快,药效稳定,不易受温度及湿度等环境条件的影响。其合成路线之一如下:
)属于低毒除草剂,作用速度快,药效稳定,不易受温度及湿度等环境条件的影响。其合成路线之一如下:
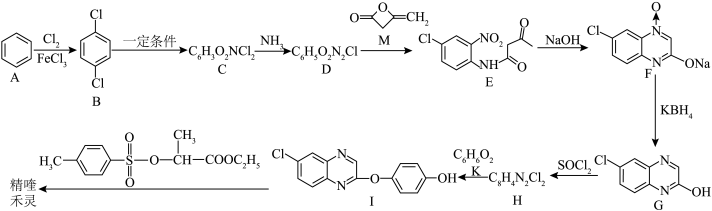
 属于间位定位基,
属于间位定位基,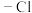 属于邻、对位定位基。
属于邻、对位定位基。回答下列问题:
(1)B→C的反应试剂及条件是
(2)D中含氧官能团的名称为
(3)K的结构简式为
(4)H→I的反应过程中,当H过量时可能会得到某一副产物,生成该副产物的化学方程式为
(5)化合物X的相对分子质量比D大14,则满足下列条件的X有
①含有
 和
和 ,且
,且 直接连在苯环上;②苯环上侧链数目小于4。
直接连在苯环上;②苯环上侧链数目小于4。其中核磁共振氢谱有4组吸收峰的X的结构简式为
(6)参考上述合成路线,设计以
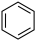 和M为原料,合成
和M为原料,合成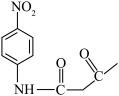 的路线
的路线
您最近一年使用:0次
名校
解题方法
8 . 下列离子方程式与所给事实相符的是
A.向水杨酸溶液中加入碳酸氢钠: |
B.碱性锌锰电池工作时正极反应: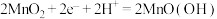 |
C.将少量 通入NaClO溶液中: 通入NaClO溶液中: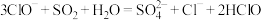 |
D.向乙二醇溶液中加入足量酸性高锰酸钾溶液: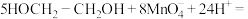  |
您最近一年使用:0次
名校
解题方法
9 . 有关下列2种有机物的说法不正确 的是
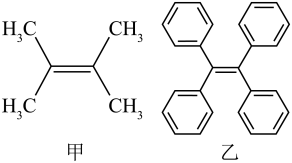
| A.甲、乙分子中官能团相同,两者互为同系物 |
| B.乙分子中所有碳原子可能处于同一平面上 |
C.甲使溴的四氯化碳溶液褪色和使酸性 溶液褪色的原理不同 溶液褪色的原理不同 |
| D.乙的一氯代物有3种(不考虑立体异构) |
您最近一年使用:0次
10 . 硫酸铝是一种具有广泛用途的重要化工产品,以高岭土(含 、
、 、少量
、少量 等)为原料制备硫酸铝晶体[
等)为原料制备硫酸铝晶体[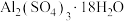 ]的实验流程如图所示。
]的实验流程如图所示。
(1)为加快酸溶速率,可采取的措施_______ (写出一条,合理即可)。
(2)滤渣1经过处理可作为制备水玻璃( 水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式
水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式_______ 。
(3)加入试剂除铁前,滤液1中的阳离子除了 、
、 外还有的阳离子是
外还有的阳离子是_______ (填离子符号)。滤渣2主要成分为 ,由于条件控制不当,常使
,由于条件控制不当,常使 中混有
中混有 影响其回收利用,用离子方程式表示除去
影响其回收利用,用离子方程式表示除去 的原理
的原理_______ 。
(4)向滤液1中加入的试剂可以是 ,试结合平衡移动原理说明其原因
,试结合平衡移动原理说明其原因_______ 。
(5)已知常温时:Ksp[Fe(OH)3] =1×10-37.4、Kw=1×10-14;当溶液中Fe3+浓度低于10-5mol/L时即认为Fe3+沉淀完全,实验中为确保Fe3+完全沉淀需控制PH不低于_______ (保留小数点一位)。
(6)某兴趣小组为了测定晶体中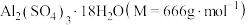 的质量分数,进行如下实验:
的质量分数,进行如下实验:
①准确称取1.00g晶体样品,溶于一定量水中;
②滴入 EDTA溶液,与
EDTA溶液,与 反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与
反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与 以物质的量之比1:1反应,假设杂质不与EDTA反应)。
以物质的量之比1:1反应,假设杂质不与EDTA反应)。
则晶体中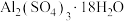 的质量分数是
的质量分数是_______ 。
 、
、 、少量
、少量 等)为原料制备硫酸铝晶体[
等)为原料制备硫酸铝晶体[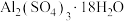 ]的实验流程如图所示。
]的实验流程如图所示。
(1)为加快酸溶速率,可采取的措施
(2)滤渣1经过处理可作为制备水玻璃(
 水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式
水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式(3)加入试剂除铁前,滤液1中的阳离子除了
 、
、 外还有的阳离子是
外还有的阳离子是 ,由于条件控制不当,常使
,由于条件控制不当,常使 中混有
中混有 影响其回收利用,用离子方程式表示除去
影响其回收利用,用离子方程式表示除去 的原理
的原理(4)向滤液1中加入的试剂可以是
 ,试结合平衡移动原理说明其原因
,试结合平衡移动原理说明其原因(5)已知常温时:Ksp[Fe(OH)3] =1×10-37.4、Kw=1×10-14;当溶液中Fe3+浓度低于10-5mol/L时即认为Fe3+沉淀完全,实验中为确保Fe3+完全沉淀需控制PH不低于
(6)某兴趣小组为了测定晶体中
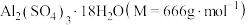 的质量分数,进行如下实验:
的质量分数,进行如下实验:①准确称取1.00g晶体样品,溶于一定量水中;
②滴入
 EDTA溶液,与
EDTA溶液,与 反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与
反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与 以物质的量之比1:1反应,假设杂质不与EDTA反应)。
以物质的量之比1:1反应,假设杂质不与EDTA反应)。则晶体中
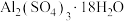 的质量分数是
的质量分数是
您最近一年使用:0次



