名校
1 . 以下说法错误的是
| A.苯的邻二氯代物只有一种证明苯没有单双键交替的结构 |
| B.甲苯使高锰酸钾溶液褪色说明苯环对甲基有影响 |
C.CH3CHBrCH2CH3与 的醇溶液共热反应有机产物有2种(不考虑顺反异构) 的醇溶液共热反应有机产物有2种(不考虑顺反异构) |
| D.甲苯在一定条件下发生硝化反应产物只有TNT一种 |
您最近一年使用:0次
7日内更新
|
296次组卷
|
2卷引用:陕西省咸阳市武功县普集高级中学2023-2024学年高二下学期6月月考化学试题
解题方法
2 . 某工厂通过如下装置处理两个车间的废气(电极均为惰性电极),既处理了污染物,又变废为宝。下列说法正确的是
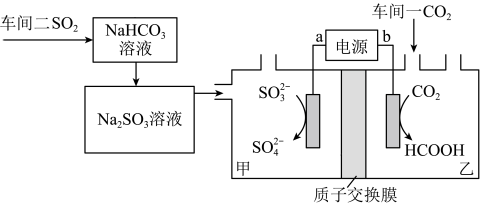
A.电极电势: |
B.工作时 由乙池移向甲池 由乙池移向甲池 |
C.通电一段时间后甲区域的 增大 增大 |
D.阴极反应式: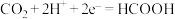 |
您最近一年使用:0次
名校
解题方法
3 . 亚砷酸C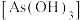 ,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数
,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数 与pH的关系如图所示,分布系数
与pH的关系如图所示,分布系数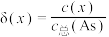 。下列说法错误的是
。下列说法错误的是
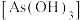 ,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数
,是一种无机化合物.室温下,调节某亚砷酸溶液的pH,体系中含As物种的组分分布系数 与pH的关系如图所示,分布系数
与pH的关系如图所示,分布系数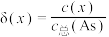 。下列说法错误的是
。下列说法错误的是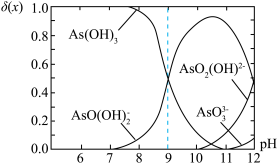
A. |
B. 时,水电离的 时,水电离的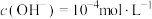 |
C.等物质的量浓度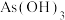 和 和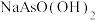 混合溶液中 混合溶液中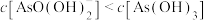 |
D.当溶液 后,体系中 后,体系中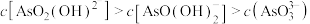 |
您最近一年使用:0次
2024-06-16更新
|
119次组卷
|
2卷引用:2024届陕西省部分学校高三下学期5月份高考适应性考试理科综合试题-高中化学
名校
4 . 根据原电池原理,人们研制出了性能各异的化学电池。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:__________ 。负极材料是__________ ,负极反应式为____________________ 。
②该电池工作时,下列说法错误的是__________ (填字母)。
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯__________ (填“会”或“不会”)亮,原因是____________________________________________________________ 。
(2)某锂-空气电池的总反应为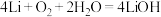 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示: 发生
发生__________ (填“氧化”或“还原”)反应。
②锂离子向电池__________ (填“正”或“负”)极移动。
③石墨电极__________ (填“参与”或“不参与”)电极反应。
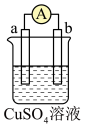
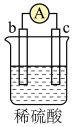
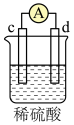
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
由上表可判断a、b、c、d四种金属的活动性由大到小排列为__________ (填字母)。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:

②该电池工作时,下列说法错误的是
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯
(2)某锂-空气电池的总反应为
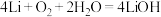 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示:
 发生
发生②锂离子向电池
③石墨电极
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
实验装置 |
|
|
|
|
部分实验现象 | b极质量增大 | 外电路电流 从a流向d | c极上有气泡产生 | d极溶解 |
您最近一年使用:0次
名校
解题方法
5 . 蛋白质是生命活动的主要物质基础。下列说法错误的是
| A.蛋白质与氨基酸类似,也是两性分子 |
| B.加热牛奶和蛋清混合物制作双皮奶,该过程涉及蛋白质的变性 |
| C.食物中的蛋白质可在蛋白酶的作用下水解生成氨基酸 |
D.蛋白质中加入 溶液产生盐析现象 溶液产生盐析现象 |
您最近一年使用:0次
6 . 有机物M是新型苯二氮卓类镇静剂,其合成路线如下:
(1)G中所含官能团名称为___________ 。
(2)已知B的分子式为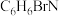 ,写出B的结构简式:
,写出B的结构简式:___________ ,其化学名称为___________ 。
(3)K的结构简式为___________ ,J→K的反应类型为___________ 。
(4)F+G→H分两步进行,第1步为加成反应,第2步为消去反应。写出第1步反应的化学方程式:___________ 。
(5)E的芳香族同分异构体中,符合下列条件的有种(不考虑立体异构体,不考虑 环状化合物)。
环状化合物)。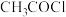 )、苯和甲胺(
)、苯和甲胺(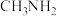 )为原料,设计制备
)为原料,设计制备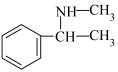 的合成路线:
的合成路线:___________ (其他无机试剂任选)。

(1)G中所含官能团名称为
(2)已知B的分子式为
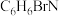 ,写出B的结构简式:
,写出B的结构简式:(3)K的结构简式为
(4)F+G→H分两步进行,第1步为加成反应,第2步为消去反应。写出第1步反应的化学方程式:
(5)E的芳香族同分异构体中,符合下列条件的有种(不考虑立体异构体,不考虑
 环状化合物)。
环状化合物)。①分子中含有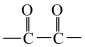 ;②核磁共振氢谱有四组峰。
;②核磁共振氢谱有四组峰。
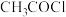 )、苯和甲胺(
)、苯和甲胺(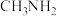 )为原料,设计制备
)为原料,设计制备 的合成路线:
的合成路线:
您最近一年使用:0次
7 . 由 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:
反应I:
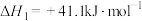
反应II:
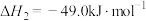
(1)已知:相关共价键的键能数据如表。
试计算:断开 中的化学键所需要提供的最低能量为
中的化学键所需要提供的最低能量为___________ 。
(2)对反应I来说,若该反应能自发进行,则该反应的熵变
___________ 0(填“>”或“<”)。若该反应速率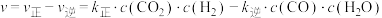 ,其中
,其中 、
、 分别为正反应、逆反应的速率常数,
分别为正反应、逆反应的速率常数, 为气体的浓度。若降低温度,
为气体的浓度。若降低温度,
___________ (填“增大”“减小”或“不变”)。
(3)在T℃时,向容积为 的恒容密闭容器中投入
的恒容密闭容器中投入 和
和 ,此时容器内的总压为
,此时容器内的总压为 ,发生反应I、反应II。
,发生反应I、反应II。
①下列能说明反应I、反应II达到平衡状态的是___________ (填字母)。
a.
b.容器内气体的密度不再变化
c. 和
和 的物质的量之比不再变化
的物质的量之比不再变化
d. 的体积分数不再变化
的体积分数不再变化
②实验测得平衡时 或CO的选择性随温度的变化如图所示。
或CO的选择性随温度的变化如图所示。 的选择性
的选择性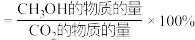 、CO的选择性
、CO的选择性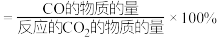 。
。
其中,表示平衡时 的选择性的是曲线
的选择性的是曲线___________ (填“i”或“ii”);为同时提高 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性,应选择的反应条件为
的选择性,应选择的反应条件为___________ (填标号)。
a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
③若在上述条件下,反应经5min后达平衡, 的平衡转化率为50%,CO的选择性为20%。则在0~5min内
的平衡转化率为50%,CO的选择性为20%。则在0~5min内
___________  (保留2位小数),反应II的平衡常数
(保留2位小数),反应II的平衡常数
___________ (列出计算式即可)。
 催化加氢制
催化加氢制 的反应体系中,发生的主要反应如下:
的反应体系中,发生的主要反应如下:反应I:

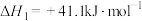
反应II:

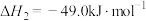
(1)已知:相关共价键的键能数据如表。
| 共价键 |  |  |  |  |
键能 | 436.0 | 413.4 | 351 | 462.8 |
 中的化学键所需要提供的最低能量为
中的化学键所需要提供的最低能量为(2)对反应I来说,若该反应能自发进行,则该反应的熵变

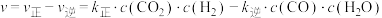 ,其中
,其中 、
、 分别为正反应、逆反应的速率常数,
分别为正反应、逆反应的速率常数, 为气体的浓度。若降低温度,
为气体的浓度。若降低温度,
(3)在T℃时,向容积为
 的恒容密闭容器中投入
的恒容密闭容器中投入 和
和 ,此时容器内的总压为
,此时容器内的总压为 ,发生反应I、反应II。
,发生反应I、反应II。①下列能说明反应I、反应II达到平衡状态的是
a.

b.容器内气体的密度不再变化
c.
 和
和 的物质的量之比不再变化
的物质的量之比不再变化 d.
 的体积分数不再变化
的体积分数不再变化②实验测得平衡时
 或CO的选择性随温度的变化如图所示。
或CO的选择性随温度的变化如图所示。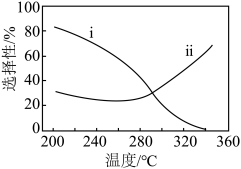
 的选择性
的选择性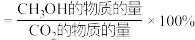 、CO的选择性
、CO的选择性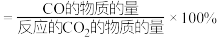 。
。其中,表示平衡时
 的选择性的是曲线
的选择性的是曲线 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性,应选择的反应条件为
的选择性,应选择的反应条件为a.低温、低压 b.高温、高压 c.高温、低压 d.低温、高压
③若在上述条件下,反应经5min后达平衡,
 的平衡转化率为50%,CO的选择性为20%。则在0~5min内
的平衡转化率为50%,CO的选择性为20%。则在0~5min内
 (保留2位小数),反应II的平衡常数
(保留2位小数),反应II的平衡常数
您最近一年使用:0次
8 . 氮化镁用途广泛,常用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其他元素的氮化物时作为催化剂。第一次成功合成立方氮化硼时,使用的催化剂就是氮化镁。实验室可用如图装置制取 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。___________ 。
(2)装置C中氧化铜的作用是氧化氨气制取 ,其反应的化学方程式为
,其反应的化学方程式为___________ 。
(3)装置D的作用是___________ 。
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是___________ 。
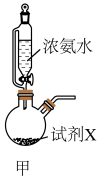
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为___________ ,固体试剂X可以为___________ (填字母)。
(6)实验室还可用 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为___________ 。___________ 。
 并与金属镁反应制取氮化镁(已知氮化镁易水解)。
并与金属镁反应制取氮化镁(已知氮化镁易水解)。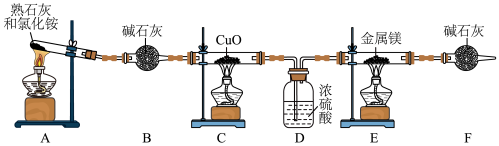
(2)装置C中氧化铜的作用是氧化氨气制取
 ,其反应的化学方程式为
,其反应的化学方程式为(3)装置D的作用是
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是
(5)用如图甲装置可快速制取上述实验所需的氨气,其中盛浓氨水的仪器名称为
(6)实验室还可用
 固体与浓
固体与浓 溶液共热制取
溶液共热制取 ,装置如图乙所示。该反应的离子方程式为
,装置如图乙所示。该反应的离子方程式为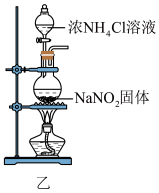
您最近一年使用:0次
名校
9 . 低品质能源利用是指对热值较低、含杂物较高等特点的一类能源的利用。如图所示装置,可同时利用低温废热和含铜废液,并达到对含铜废液富集和产生电能的目的。起始时电极均为泡沫铜且质量相等,含铜废液的浓度为0.1 ,以2.5
,以2.5
 溶液作为电解质溶液,向M极区液体中加入2
溶液作为电解质溶液,向M极区液体中加入2 氨水开始反应。下列说法正确的是
氨水开始反应。下列说法正确的是
 ,以2.5
,以2.5
 溶液作为电解质溶液,向M极区液体中加入2
溶液作为电解质溶液,向M极区液体中加入2 氨水开始反应。下列说法正确的是
氨水开始反应。下列说法正确的是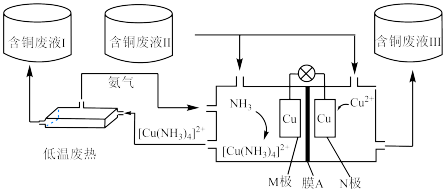
| A.向M极区液体中加入氨水可使M极电势高于N极电势 |
B.含铜废液Ⅰ、Ⅲ中的 均高于含铜废液Ⅱ中的 均高于含铜废液Ⅱ中的 |
| C.电子由M极经导线移向N极 |
| D.电极质量差为6.4g时,电路中通过0.2mol电子 |
您最近一年使用:0次
2024-06-09更新
|
298次组卷
|
5卷引用:2024届陕西省安康市高新中学、安康中学高新分校高三下学期模拟预测(三)理综试题-高中化学
解题方法
10 . 某兴趣小组在实验室模拟侯氏制碱法制备 ,部分实验装置如图所示,下列说法正确的是
,部分实验装置如图所示,下列说法正确的是
 ,部分实验装置如图所示,下列说法正确的是
,部分实验装置如图所示,下列说法正确的是
| A.实验过程中向启普发生器中添加液体时,可以取下Ⅰ处胶塞加入 |
B.所用试剂有稀硫酸、浓硫酸、 、饱和食盐水、 、饱和食盐水、 、 、 、蒸馏水 、蒸馏水 |
| C.开始实验时,应先打开活塞Ⅱ,再打开活塞Ⅲ |
D.试剂d为冰水,以降低 的溶解度,促进晶体的析出 的溶解度,促进晶体的析出 |
您最近一年使用:0次
2024-06-08更新
|
115次组卷
|
2卷引用:2024届陕西省安康市高新中学、安康中学高新分校高三下学期模拟预测(三)理综试题-高中化学