10-11高三上·江苏盐城·期中
名校
1 . 重铬酸钾是工业生产和实验室的重要氧化剂,工业上常用铬铁矿(主要成份为FeO·Cr2O3)为原料生产,实验室模拟工业法用铬铁矿制K2Cr2O7的主要工艺如下,涉及的主要反应是:6FeO·Cr2O3+24NaOH+7KClO3 12Na2CrO4+3Fe2O3+7KCl+12H2O
12Na2CrO4+3Fe2O3+7KCl+12H2O

试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:___________ 。
(2)操作③的目的是什么,用简要的文字说明:____________________________ 。
(3)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:_______ 。
(4)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)
①判断达到滴定终点的依据是:________________ ;
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中重铬酸钾的纯度(设整个过程中其它杂质不参与反应)____________ 。
 12Na2CrO4+3Fe2O3+7KCl+12H2O
12Na2CrO4+3Fe2O3+7KCl+12H2O
试回答下列问题:
(1)在反应器①中,有Na2CrO4生成,同时Fe2O3转变为NaFeO2,杂质SiO2、Al2O3与纯碱反应转变为可溶性盐,写出氧化铝与碳酸钠反应的化学方程式:
(2)操作③的目的是什么,用简要的文字说明:
(3)操作④中,酸化时,CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
(4)称取重铬酸钾试样2.5000g配成250mL溶液,取出25.00mL于碘量瓶中,加入10mL2mol/LH2SO4和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200mol/LNa2S2O3标准溶液滴定(I2+2S2O32-=2I-+S4O62-)
①判断达到滴定终点的依据是:
②若实验中共用去Na2S2O3标准溶液40.00mL,则所得产品中重铬酸钾的纯度(设整个过程中其它杂质不参与反应)
您最近一年使用:0次
名校
解题方法
2 . 某化学小组对 溶液与
溶液与 溶液的反应进行探究。
溶液的反应进行探究。
(一)配制溶液
(1)配制 溶液前需检验固体是否变质,其操作方法为:取少量样品于试管中,加适量蒸馏水溶解,再加入
溶液前需检验固体是否变质,其操作方法为:取少量样品于试管中,加适量蒸馏水溶解,再加入___________ ,若无白色沉淀生成,则 未变质。
未变质。
(2)用离子方程式结合适当文字解释:配制氯化铁溶液时,先将氯化铁固体溶于稀盐酸,再稀释到所需浓度的原因___________ 。
(二)预测实验
(3)该小组同学预测 溶液与
溶液与 溶液混合时,溶液颜色由棕黄色变成浅绿色,他们预测的依据为(用离子方程式表示):
溶液混合时,溶液颜色由棕黄色变成浅绿色,他们预测的依据为(用离子方程式表示):___________ 。
(三)实施实验
向2mL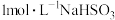 溶液中逐滴加入0.5mL
溶液中逐滴加入0.5mL 溶液
溶液
(4)查阅资料:溶液中 、
、 、
、 三种微粒会形成红色物质并存在如下转化:
三种微粒会形成红色物质并存在如下转化:
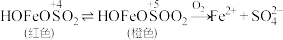
①用离子方程式解释0~1min的实验现象___________ 。
②从反应速率和化学平衡两个角度解释1~30min的实验现象___________ 。
(5)小组同学认为没有观察到预期的实验现象,是因为混合产生气体的反应干扰了氧化还原反应的发生,该同学通过如下实验证明了猜想的正确性。已知铁氰化钾溶液可与 反应生成蓝色沉淀。
反应生成蓝色沉淀。
①分析实验Ⅰ中电流计指针不偏转(没有形成原电池)的原因是___________ 。
②实验Ⅱ中右侧烧杯发生的电极反应式为___________ 。
 溶液与
溶液与 溶液的反应进行探究。
溶液的反应进行探究。(一)配制溶液
(1)配制
 溶液前需检验固体是否变质,其操作方法为:取少量样品于试管中,加适量蒸馏水溶解,再加入
溶液前需检验固体是否变质,其操作方法为:取少量样品于试管中,加适量蒸馏水溶解,再加入 未变质。
未变质。(2)用离子方程式结合适当文字解释:配制氯化铁溶液时,先将氯化铁固体溶于稀盐酸,再稀释到所需浓度的原因
(二)预测实验
(3)该小组同学预测
 溶液与
溶液与 溶液混合时,溶液颜色由棕黄色变成浅绿色,他们预测的依据为(用离子方程式表示):
溶液混合时,溶液颜色由棕黄色变成浅绿色,他们预测的依据为(用离子方程式表示):(三)实施实验
向2mL
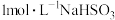 溶液中逐滴加入0.5mL
溶液中逐滴加入0.5mL 溶液
溶液| 装置 | 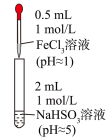 |
| 反应时间 | 实验现象 |
| 0~1min | 产生红褐色沉淀,有刺激性气味气体逸出 |
| 1~30min | 沉淀迅速溶解形成红色溶液,随后溶液逐渐变为橙色,之后几乎无色 |
| 30min后 | 与空气接触部分的上层溶液又变为浅红色,随后逐渐变为浅橙色 |
 、
、 、
、 三种微粒会形成红色物质并存在如下转化:
三种微粒会形成红色物质并存在如下转化: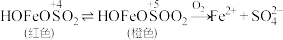
①用离子方程式解释0~1min的实验现象
②从反应速率和化学平衡两个角度解释1~30min的实验现象
(5)小组同学认为没有观察到预期的实验现象,是因为混合产生气体的反应干扰了氧化还原反应的发生,该同学通过如下实验证明了猜想的正确性。已知铁氰化钾溶液可与
 反应生成蓝色沉淀。
反应生成蓝色沉淀。| 装置 |  | |
| 实验步骤 | 操作 | 实验现象 |
| Ⅰ | 向烧杯中装好溶液、连接好装置、闭合开关 | 灵敏电流表指针未发生偏转 |
| Ⅱ | 向左侧烧杯中滴加少量饱和 溶液 溶液 | 灵敏电流表指针向左侧偏转 |
| Ⅲ | 向左侧烧杯中再滴加少量铁氰化钾溶液 | 左侧烧杯中产生蓝色沉淀,灵敏电流表指针向左侧偏转幅度更大 |
②实验Ⅱ中右侧烧杯发生的电极反应式为
您最近一年使用:0次
名校
解题方法
3 . 钛在医疗领域的使用非常广泛,如制人造关节、头盖、主动心瓣等。 是制备金属钛的重要中间体。某小组同学利用如图装置在实验室制备
是制备金属钛的重要中间体。某小组同学利用如图装置在实验室制备 (夹持装置略去)。
(夹持装置略去)。
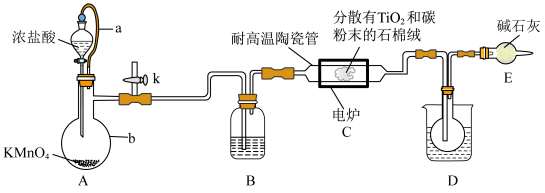
已知:HCl与 不发生反应;装置C中除生成
不发生反应;装置C中除生成 外,同时还生成一种有毒气态氧化物和少量副产物
外,同时还生成一种有毒气态氧化物和少量副产物 ,其它相关信息如表所示:
,其它相关信息如表所示:
请回答下列问题:
(1)装置A中导管a的作用为_______ ,装置B中所盛试剂为_______ 。
(2)组装好仪器后,部分实验步骤如下:
a.装入药品 b.打开分液漏斗活塞 c.检查装置气密性 d.关闭分液漏斗活塞 e.停止加热,充分冷却 f.加热装置C中陶瓷管
从上述选项选择合适操作(不重复使用)并排序:_______ →_______ →b→_______ →_______ →_______ 。
(3)陶瓷管加热至900℃,管中主要发生的化学反应方程式为_______ 。
(4)欲分离D装置中收集的液态混合物,所采用的操作名称是_______ 。
(5)下列说法不正确的是_______ 。
A.通入氯气之前,最好先从k处通入氮气,否则实验会失败
B.石棉线载体是为了增大气体与 、碳粉的接触面积,以加快反应速率
、碳粉的接触面积,以加快反应速率
C.装置D中的烧杯中可加入冰水,便于收集到纯的液态
D.装置E可防止空气中的水蒸气进入装置D的圆底烧瓶中使 变质
变质
E.该装置有缺陷,通过装置E后的气体不可直接排放到空气中
(6) 可制备纳米
可制备纳米 :以
:以 为载体,用
为载体,用 和水蒸气反应生成
和水蒸气反应生成 ,再控制温度生成纳米
,再控制温度生成纳米 ,测定纳米
,测定纳米 组成,方法如下:
组成,方法如下:
步骤一:取样品2.100g用稀硫酸充分溶解得到 ,再用足量铝将
,再用足量铝将 还原为
还原为 过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,定容得待测液。
过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,定容得待测液。
步骤二:取待测液25.00mL于锥形瓶中,加几滴KSCN溶液作指示剂,用0.1000mol/L的 标准溶液滴定,将
标准溶液滴定,将 氧化为
氧化为 ,三次滴定消耗标准溶液的平均值为24.00mL。
,三次滴定消耗标准溶液的平均值为24.00mL。
①滴定终点的判断方法是_______ 。
②通过分析、计算,该样品的组成为_______ 。
 是制备金属钛的重要中间体。某小组同学利用如图装置在实验室制备
是制备金属钛的重要中间体。某小组同学利用如图装置在实验室制备 (夹持装置略去)。
(夹持装置略去)。
已知:HCl与
 不发生反应;装置C中除生成
不发生反应;装置C中除生成 外,同时还生成一种有毒气态氧化物和少量副产物
外,同时还生成一种有毒气态氧化物和少量副产物 ,其它相关信息如表所示:
,其它相关信息如表所示:| 熔点/℃ | 沸点/℃ | 密度 | 水溶性 | |
 | -24 | 136.4 | 1.7 | 易水解生成白色沉淀,能溶于有机溶剂 |
 | -23 | 76.8 | 1.6 | 难溶于水 |
(1)装置A中导管a的作用为
(2)组装好仪器后,部分实验步骤如下:
a.装入药品 b.打开分液漏斗活塞 c.检查装置气密性 d.关闭分液漏斗活塞 e.停止加热,充分冷却 f.加热装置C中陶瓷管
从上述选项选择合适操作(不重复使用)并排序:
(3)陶瓷管加热至900℃,管中主要发生的化学反应方程式为
(4)欲分离D装置中收集的液态混合物,所采用的操作名称是
(5)下列说法不正确的是
A.通入氯气之前,最好先从k处通入氮气,否则实验会失败
B.石棉线载体是为了增大气体与
 、碳粉的接触面积,以加快反应速率
、碳粉的接触面积,以加快反应速率C.装置D中的烧杯中可加入冰水,便于收集到纯的液态

D.装置E可防止空气中的水蒸气进入装置D的圆底烧瓶中使
 变质
变质E.该装置有缺陷,通过装置E后的气体不可直接排放到空气中
(6)
 可制备纳米
可制备纳米 :以
:以 为载体,用
为载体,用 和水蒸气反应生成
和水蒸气反应生成 ,再控制温度生成纳米
,再控制温度生成纳米 ,测定纳米
,测定纳米 组成,方法如下:
组成,方法如下:步骤一:取样品2.100g用稀硫酸充分溶解得到
 ,再用足量铝将
,再用足量铝将 还原为
还原为 过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,定容得待测液。
过滤并洗涤,将所得滤液和洗涤液合并注入250mL容量瓶,定容得待测液。步骤二:取待测液25.00mL于锥形瓶中,加几滴KSCN溶液作指示剂,用0.1000mol/L的
 标准溶液滴定,将
标准溶液滴定,将 氧化为
氧化为 ,三次滴定消耗标准溶液的平均值为24.00mL。
,三次滴定消耗标准溶液的平均值为24.00mL。①滴定终点的判断方法是
②通过分析、计算,该样品的组成为
您最近一年使用:0次
解题方法
4 . 过氧化钠因吸收空气里的二氧化碳和水而变质,某兴趣小组对久置的过氧化钠样品M进行实验探究。
实验I:甲同学设计下图所示装置探究样品M的变质情况。___________ 。
(2)装置C中的溶液是___________ ,能代替C的试剂是___________ 。
(3)若B中___________ ,D中___________ ,则样品M部分变质。
实验Ⅱ:乙同学用氯化钡溶液作为检验试剂进行实验。
(4)根据产生白色沉淀,乙同学认为样品M已变质,该反应的离子方程式为___________ 。
资料显示, 能与
能与 、NaOH溶液反应生成白色不溶物
、NaOH溶液反应生成白色不溶物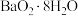 。据此,丙同学对乙同学的检验结果提出质疑并进行实验。
。据此,丙同学对乙同学的检验结果提出质疑并进行实验。
实验Ⅲ:取少量纯净的过氧化钠固体溶于蒸馏水,先加入过量稀硫酸,再滴入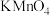 溶液。实验证明
溶液。实验证明 与水反应有
与水反应有 生成。
生成。
(5)滴入 溶液后观察到的现象是
溶液后观察到的现象是________ ,此反应的离子方程式为________ 。
丙同学利用如图装置进行实验,排除了 的干扰。
的干扰。
(6)请补充完整上述实验的操作过程:___________ 。
实验I:甲同学设计下图所示装置探究样品M的变质情况。
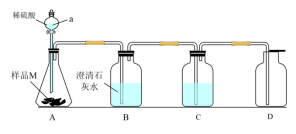
(2)装置C中的溶液是
(3)若B中
实验Ⅱ:乙同学用氯化钡溶液作为检验试剂进行实验。
(4)根据产生白色沉淀,乙同学认为样品M已变质,该反应的离子方程式为
资料显示,
 能与
能与 、NaOH溶液反应生成白色不溶物
、NaOH溶液反应生成白色不溶物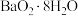 。据此,丙同学对乙同学的检验结果提出质疑并进行实验。
。据此,丙同学对乙同学的检验结果提出质疑并进行实验。实验Ⅲ:取少量纯净的过氧化钠固体溶于蒸馏水,先加入过量稀硫酸,再滴入
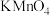 溶液。实验证明
溶液。实验证明 与水反应有
与水反应有 生成。
生成。(5)滴入
 溶液后观察到的现象是
溶液后观察到的现象是丙同学利用如图装置进行实验,排除了
 的干扰。
的干扰。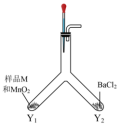
(6)请补充完整上述实验的操作过程:
您最近一年使用:0次
名校
5 . 吊白块( ,
,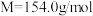 )在工业中有广泛应用;吊白块在酸性环境下、100℃即发生分解释放出HCHO。实验室制备吊白块的方案如下:
)在工业中有广泛应用;吊白块在酸性环境下、100℃即发生分解释放出HCHO。实验室制备吊白块的方案如下:
 的制备:如图,在广口瓶中加入一定量
的制备:如图,在广口瓶中加入一定量 和水,振荡溶解,缓慢通入
和水,振荡溶解,缓慢通入 ,至广口瓶中液体pH约为4,制得
,至广口瓶中液体pH约为4,制得 溶液。
溶液。

(1)装置I中产生气体的化学反应方程式为_______ ;II中多孔球泡的作用是_______ 。
(2)实验室检测 晶体在空气中是否发生氧化变质的实验方案是
晶体在空气中是否发生氧化变质的实验方案是_______ 。
吊白块的制备:如图,向仪器A中加入上述 溶液、稍过量的锌粉和一定量甲醛,在80~90℃下,反应约3h,冷却过滤。
溶液、稍过量的锌粉和一定量甲醛,在80~90℃下,反应约3h,冷却过滤。

(3)仪器A的名称为_______ ;用恒压漏斗代替普通滴液漏斗滴加甲醛的优点是_______ 。
(4)将仪器A中的反应温度恒定在80~90℃的目的是_______ 。
吊白块纯度的测定:将0.5000g吊白块样品置于蒸馏烧瓶中,加入10%磷酸10mL,立即通入100℃水蒸气;吊白块分解并释放出甲醛,用含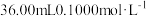 酸性
酸性 吸收甲醛(不考虑
吸收甲醛(不考虑 的有影响,
的有影响, ),再用
),再用 的草酸标准溶液滴定酸性
的草酸标准溶液滴定酸性 ,再重复实验2次,平均消耗草酸溶液的体积为30.00mL。
,再重复实验2次,平均消耗草酸溶液的体积为30.00mL。
(5)吊白块样品的纯度为_______ %(保留思维有效数字);若 标准溶液久置释放出
标准溶液久置释放出 而变质,会导致测量结果
而变质,会导致测量结果_______ (填“偏高”、“偏低”或“无影响”)
 ,
,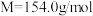 )在工业中有广泛应用;吊白块在酸性环境下、100℃即发生分解释放出HCHO。实验室制备吊白块的方案如下:
)在工业中有广泛应用;吊白块在酸性环境下、100℃即发生分解释放出HCHO。实验室制备吊白块的方案如下: 的制备:如图,在广口瓶中加入一定量
的制备:如图,在广口瓶中加入一定量 和水,振荡溶解,缓慢通入
和水,振荡溶解,缓慢通入 ,至广口瓶中液体pH约为4,制得
,至广口瓶中液体pH约为4,制得 溶液。
溶液。
(1)装置I中产生气体的化学反应方程式为
(2)实验室检测
 晶体在空气中是否发生氧化变质的实验方案是
晶体在空气中是否发生氧化变质的实验方案是吊白块的制备:如图,向仪器A中加入上述
 溶液、稍过量的锌粉和一定量甲醛,在80~90℃下,反应约3h,冷却过滤。
溶液、稍过量的锌粉和一定量甲醛,在80~90℃下,反应约3h,冷却过滤。
(3)仪器A的名称为
(4)将仪器A中的反应温度恒定在80~90℃的目的是
吊白块纯度的测定:将0.5000g吊白块样品置于蒸馏烧瓶中,加入10%磷酸10mL,立即通入100℃水蒸气;吊白块分解并释放出甲醛,用含
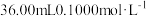 酸性
酸性 吸收甲醛(不考虑
吸收甲醛(不考虑 的有影响,
的有影响, ),再用
),再用 的草酸标准溶液滴定酸性
的草酸标准溶液滴定酸性 ,再重复实验2次,平均消耗草酸溶液的体积为30.00mL。
,再重复实验2次,平均消耗草酸溶液的体积为30.00mL。(5)吊白块样品的纯度为
 标准溶液久置释放出
标准溶液久置释放出 而变质,会导致测量结果
而变质,会导致测量结果
您最近一年使用:0次
名校
解题方法
6 . 下列有关实验、现象、及结论等叙述正确的有
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向某溶液加入稀硫酸,有淡黄色沉淀和刺激性气味的气体,该溶液中一定含有S2O32-
④向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
⑤向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑥取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
①向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀,X具有强氧化性
②将稀盐酸滴入硅酸钠溶液中,充分振荡,有白色沉淀产生,非金属性:Cl>Si
③向某溶液加入稀硫酸,有淡黄色沉淀和刺激性气味的气体,该溶液中一定含有S2O32-
④向X溶液加新制氯水,再加入少量KSCN溶液,溶液变为红色,X溶液中一定含有Fe2+
⑤向饱和NaHCO3溶液中滴加硼酸,无气泡产生,酸性:硼酸<碳酸
⑥取少量Fe(NO3)2样品溶于稀硫酸,滴入KSCN溶液,溶液变红色,证明样品已变质
| A.1条 | B.2条 | C.3条 | D.4条 |
您最近一年使用:0次
2019-12-10更新
|
996次组卷
|
3卷引用:福建泉州实验中学、惠安一中、安溪一中、养正中学2021-2022高三上学期期中考试化学试题
7 . 高铁酸钾(K2FeO4)是一新型、高效、无毒的多功能水处理剂。
【资料】K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4。
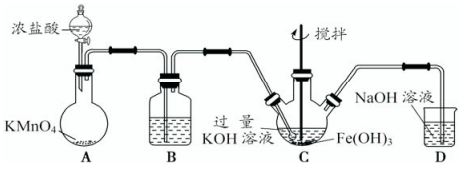
①A为制取氯气发生装置,其中盛放浓盐酸的仪器名称为___________ 。
②除杂装置B中的试剂为___________ 。
③C为制备K2FeO4装置,KOH溶液过量的原因是___________ 。
④D为尾气处理装置,发生反应的离子方程式为___________ 。
(2)探究K2FeO4的性质。取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计以下方案:
①由方案I中溶液变红可知a中含有___________ 。该离子的产生___________ (填“能”或“不能”)判断一定是由K2FeO4被Cl-还原而形成的。
②方案Ⅱ用KOH溶液洗涤的目的是___________ 。方案Ⅱ得出氧化性:Cl2___________ FeO42-(填“>”或“<”)
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:_______ FeO42-+______H+===_______O2↑+________Fe3++________(配平及完成上述离子方程式)________ 。现取C中洗涤并干燥后样品的质量10g,加入稀硫酸,收集到0.672L气体(标准状况下)。则样品中高铁酸钾的质量分数约为___________ 。(计算结果保留到0.1%)
【资料】K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4。

①A为制取氯气发生装置,其中盛放浓盐酸的仪器名称为
②除杂装置B中的试剂为
③C为制备K2FeO4装置,KOH溶液过量的原因是
④D为尾气处理装置,发生反应的离子方程式为
(2)探究K2FeO4的性质。取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl-而产生Cl2,设计以下方案:
| 方案I | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色。 |
| 方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生。 |
②方案Ⅱ用KOH溶液洗涤的目的是
(3)使用时经常通过测定高铁酸钾的纯度来判断其是否变质。K2FeO4在硫酸溶液中反应如下:_______ FeO42-+______H+===_______O2↑+________Fe3++________(配平及完成上述离子方程式)
您最近一年使用:0次
2019-02-05更新
|
1427次组卷
|
3卷引用:【市级联考】福建省南平市2019届高三上学期第一次质量检查理科综合化学试题
【市级联考】福建省南平市2019届高三上学期第一次质量检查理科综合化学试题(已下线)2019年高考总复习巅峰冲刺-专题08 常见无机物及其应用应试策略2020届二轮复习 氧化还原反应 专题卷(全国通用)
8 . 下列有关实验的说法正确的是
| A.测定中和反应反应热实验中,为了充分反应,应将NaOH溶液缓缓倒入盐酸中 |
| B.配制FeCl3溶液时,将FeCl3晶体溶解在较浓的盐酸中,再加蒸馏水稀释到所需浓度 |
| C.用盐酸滴定NaOH溶液时,左手控制酸式滴定管活塞,右手振荡锥形瓶,眼睛注视滴定管内液面 |
| D.检验Fe(NOs)2晶体是否变质时,将Fe(NO3)2样品溶于稀H2SO4后,再滴加KSCN溶液 |
您最近一年使用:0次
名校
9 . 苯巴比妥是一种巴比妥类的镇静剂及安眠药,其合成路线如下所示(部分试剂和产物已略去):
(1)A B的反应试剂与条件为
B的反应试剂与条件为________ ,E含有的官能团名称为________ 。
(2)D的化学名称为________ 。
(3)F 苯巴比妥的化学方程式为
苯巴比妥的化学方程式为________ 。
(4)符合下列条件的苯巴比妥的同分异构体共有________ 种。
①分子中有2个苯环 ②既能与NaOH溶液反应也能与盐酸反应 ③核磁共振氢谱共5组峰
(5)苯巴比妥钠(结构为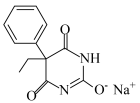 )是苯巴比妥的钠盐,两者均有镇静安眠的疗效。请从结构—性质—用途的角度分析以下原因:
)是苯巴比妥的钠盐,两者均有镇静安眠的疗效。请从结构—性质—用途的角度分析以下原因:
①苯巴比妥钠比苯巴比妥更适用于静脉注射:________
②苯巴比妥钠的水溶液易变质,需制成粉针剂(将药物与试剂混合后,经消毒干燥形成的粉状物品)保存:________ 。
(6)乙基巴比妥也是一种常用镇静剂,可用 和
和 等为原料合成,参照上述合成路线,在方框内写出相应的有机物,在箭头上下方写出适当的反应条件,将合成路线补充完整
等为原料合成,参照上述合成路线,在方框内写出相应的有机物,在箭头上下方写出适当的反应条件,将合成路线补充完整_______ 。

已知:ⅰ.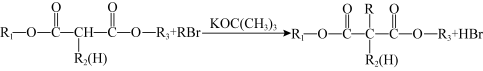
ⅱ.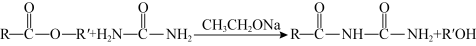
(1)A
 B的反应试剂与条件为
B的反应试剂与条件为(2)D的化学名称为
(3)F
 苯巴比妥的化学方程式为
苯巴比妥的化学方程式为(4)符合下列条件的苯巴比妥的同分异构体共有
①分子中有2个苯环 ②既能与NaOH溶液反应也能与盐酸反应 ③核磁共振氢谱共5组峰
(5)苯巴比妥钠(结构为
 )是苯巴比妥的钠盐,两者均有镇静安眠的疗效。请从结构—性质—用途的角度分析以下原因:
)是苯巴比妥的钠盐,两者均有镇静安眠的疗效。请从结构—性质—用途的角度分析以下原因:①苯巴比妥钠比苯巴比妥更适用于静脉注射:
②苯巴比妥钠的水溶液易变质,需制成粉针剂(将药物与试剂混合后,经消毒干燥形成的粉状物品)保存:
(6)乙基巴比妥也是一种常用镇静剂,可用
 和
和 等为原料合成,参照上述合成路线,在方框内写出相应的有机物,在箭头上下方写出适当的反应条件,将合成路线补充完整
等为原料合成,参照上述合成路线,在方框内写出相应的有机物,在箭头上下方写出适当的反应条件,将合成路线补充完整
您最近一年使用:0次
名校
10 . 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解,易吸水,溶于水后与水反应生成碳酸氢铵和一水合氨:NH2COONH4+2H2O NH4HCO3+NH3·H2O。可用作肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,反应的方程式:2NH3(g)+CO2(g)
NH4HCO3+NH3·H2O。可用作肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,反应的方程式:2NH3(g)+CO2(g) NH2COONH4(s)ΔH<0。
NH2COONH4(s)ΔH<0。
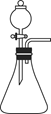
(1)如图所示装置制取氨气,你所选择的试剂是_______________ 。
(2)制备氨基甲酸铵的装置如图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。
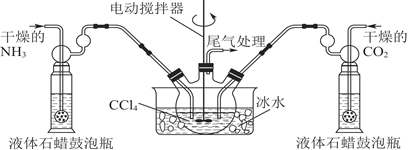
注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因__________________________ 。
液体石蜡鼓泡瓶的作用是____________________________ 。
②从反应后的混合物中分离出产品的实验方法是_______________ (填写操作名称)。 为了得到干燥产品,应采取的方法是_______________ (填写选项序号)。
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
③尾气处理装置如图所示。
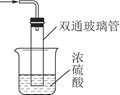
浓硫酸的作用:____________ 、________________ 。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.1730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500 g。则样品中氨基甲酸铵的物质的量分数为________ 。
[Mr(NH2COONH4)=78,Mr(NH4HCO3)=79,Mr(CaCO3)=100]
 NH4HCO3+NH3·H2O。可用作肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,反应的方程式:2NH3(g)+CO2(g)
NH4HCO3+NH3·H2O。可用作肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,反应的方程式:2NH3(g)+CO2(g) NH2COONH4(s)ΔH<0。
NH2COONH4(s)ΔH<0。(1)如图所示装置制取氨气,你所选择的试剂是

(2)制备氨基甲酸铵的装置如图所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。

注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因
液体石蜡鼓泡瓶的作用是
②从反应后的混合物中分离出产品的实验方法是
a.常压加热烘干 b.高压加热烘干 c.真空40 ℃以下烘干
③尾气处理装置如图所示。

浓硫酸的作用:
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.1730g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500 g。则样品中氨基甲酸铵的物质的量分数为
[Mr(NH2COONH4)=78,Mr(NH4HCO3)=79,Mr(CaCO3)=100]
您最近一年使用:0次
2016-12-09更新
|
121次组卷
|
2卷引用:2016届福建省泉州市南桥、荷山、南安等五校高三上12月联考化学试卷



