解题方法
1 .  加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
(1)由 加氢生成
加氢生成 的反应为
的反应为
①若 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
___________ 
②若在一定温度下的容积固定的密闭容器中进行该反应,则可以提高 平衡转化率的措施有
平衡转化率的措施有___________ (写出两种)。
③下列说法可以证明该反应已达到平衡状态的是___________ (填字母)。
a.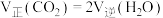 b.
b. 的物质的量分数不再改变
的物质的量分数不再改变
c.容器内气体密度不再改变 d. 和
和 的浓度之比为1:2
的浓度之比为1:2
e.混合气的平均摩尔质量不再变化 f.单位时间内生成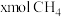 的同时又消耗
的同时又消耗
④ 催化加氢合成
催化加氢合成 过程中,
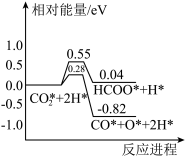
过程中, 活化的可能途径如有图所示,CO是
活化的可能途径如有图所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是___________ 。
(2)一定条件下 与
与 也可以生成
也可以生成 ,某温度下在容积为2L的恒容密闭容器中充入
,某温度下在容积为2L的恒容密闭容器中充入 和一定量
和一定量 发生反应:
发生反应: 。
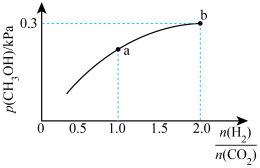
。 的平衡分压与起始投料比
的平衡分压与起始投料比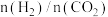 的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
___________ 。b点时,再充入 和
和 ,使两者分压均增大0.2kPa,则此时平衡
,使两者分压均增大0.2kPa,则此时平衡___________ (填“正向”、“逆向”或“不”)移动。
(3)一定条件下 与
与 还可以生成甲酸,方程式为
还可以生成甲酸,方程式为
 。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体,
。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体, 除了能分解成
除了能分解成 和
和 ,还能分解为CO和
,还能分解为CO和 ,反应为:
,反应为:
 ,则此平衡体系中CO或
,则此平衡体系中CO或 的选择性和HCOOH的转化率随温度变化曲线如图所示。
的选择性和HCOOH的转化率随温度变化曲线如图所示。

提示:CO(或氢气)的选择性
图中随着温度升高,HCOOH的转化率增大,请解释CO的选择性下降可能的原因:___________ ;400°C时 的体积分数为
的体积分数为___________ 。
 加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。
加氢是对温室气体的有效转化,也是生成再生能源与化工原料重要途径。(1)由
 加氢生成
加氢生成 的反应为
的反应为
①若
 为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热
为标准摩尔生成焓,其定义为标准状态下,由稳定相态的单质生成1mol该物质的焓变。则该反应的反应热

| 物质 |  |  |  |  |
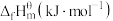 |  | 0 | 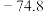 | 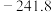 |
 平衡转化率的措施有
平衡转化率的措施有③下列说法可以证明该反应已达到平衡状态的是
a.
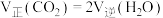 b.
b. 的物质的量分数不再改变
的物质的量分数不再改变c.容器内气体密度不再改变 d.
 和
和 的浓度之比为1:2
的浓度之比为1:2e.混合气的平均摩尔质量不再变化 f.单位时间内生成
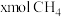 的同时又消耗
的同时又消耗
④
 催化加氢合成
催化加氢合成 过程中,
过程中, 活化的可能途径如有图所示,CO是
活化的可能途径如有图所示,CO是 活化的优势中间体,原因是
活化的优势中间体,原因是
(2)一定条件下
 与
与 也可以生成
也可以生成 ,某温度下在容积为2L的恒容密闭容器中充入
,某温度下在容积为2L的恒容密闭容器中充入 和一定量
和一定量 发生反应:
发生反应: 。
。 的平衡分压与起始投料比
的平衡分压与起始投料比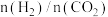 的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
的变化关系如图所示,已知b点对应投料比的起始压强为1.5kPa,则
 和
和 ,使两者分压均增大0.2kPa,则此时平衡
,使两者分压均增大0.2kPa,则此时平衡
(3)一定条件下
 与
与 还可以生成甲酸,方程式为
还可以生成甲酸,方程式为
 。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体,
。恒定压强为100kPa时,向密闭容器中充入一定量的HCOOH气体, 除了能分解成
除了能分解成 和
和 ,还能分解为CO和
,还能分解为CO和 ,反应为:
,反应为:
 ,则此平衡体系中CO或
,则此平衡体系中CO或 的选择性和HCOOH的转化率随温度变化曲线如图所示。
的选择性和HCOOH的转化率随温度变化曲线如图所示。
提示:CO(或氢气)的选择性

图中随着温度升高,HCOOH的转化率增大,请解释CO的选择性下降可能的原因:
 的体积分数为
的体积分数为
您最近一年使用:0次
2 . 三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O(M=491g/mol)是一种感光剂和高效的污水处理剂。
I.某研究小组同学查阅资料发现K3[Fe(C2O4)3]·3H2O加热后会分解产生CO和CO2,于是设计了如下实验进行验证。请回答:
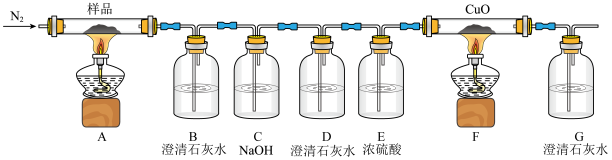
(1)C中NaOH溶液的作用为___________ ;D中澄清石灰水作用为___________ 。
(2)证明有CO产生的现象为___________ 。
(3)该装置还存在的缺陷是___________ 。
II.制备K3[Fe(C2O4)3]·3H2O的途径如下,请回答下列问题:
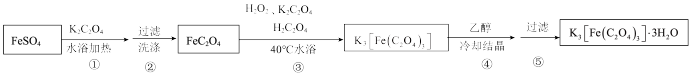
研究小组通过查阅资料得知:
a.K3[Fe(C2O4)3]·3H2O对光敏感,易溶于水,难溶于乙醇;
b.很多草酸盐(例如CaC2O4、BaC2O4)难溶于水,但能溶解于稀硝酸。
(4)步骤③中,控制水浴温度不能超过40℃的原因为___________ 。
(5)研究小组的同学对K3[Fe(C2O4)3]组成有两种看法,分别为:
甲同学:K3[Fe(C2O4)3]由K+、Fe3+、 构成;
构成;
乙同学:K3[Fe(C2O4)3]由K+、[Fe(C2O4)3]3-构成。
请设计实验,验证哪位同学的说法是正确的:___________ 。
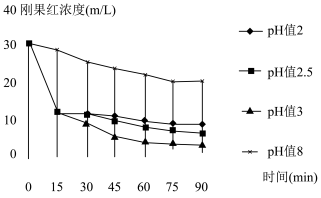
(6)K3[Fe(C2O4)3]联合H2O2体系可用于降解染料,一定浓度的该混合溶液,在不同pH条件下降解刚果红的效率如图所示,在实际应用过程中,应选择pH=___________ 。
(7)关于制备流程,下列说法正确的是___________。
(8)制得的K3[Fe(C2O4)3]·3H2O含少量FeC2O4·2H2O,为测定其纯度,进行如下实验:
步骤I:称取5.000g三草酸合铁酸钾晶体,配制成1.000L溶液,固体完全溶解。
步骤II:取20.00mL溶液,与0.1000molL-酸性KMnO4溶液反应,消耗2.46mL。
步骤III:另取20.00mL溶液,加入过量铜粉,过滤,洗涤,将滤液和洗涤液合并。
步骤IV:将合并液与0.1000mol/L酸性KMnO4溶液反应,消耗2.86mL。
已知 与
与 的反应为(未配平):
的反应为(未配平): +
+ +H+→CO2↑+Mn2++H2O
+H+→CO2↑+Mn2++H2O
①写出Fe2+与酸性KMnO4溶液反应的离子方程式:___________ 。
②研究小组制得的K3[Fe(C2O4)3]·3H2O纯度为___________ 。
I.某研究小组同学查阅资料发现K3[Fe(C2O4)3]·3H2O加热后会分解产生CO和CO2,于是设计了如下实验进行验证。请回答:

(1)C中NaOH溶液的作用为
(2)证明有CO产生的现象为
(3)该装置还存在的缺陷是
II.制备K3[Fe(C2O4)3]·3H2O的途径如下,请回答下列问题:

研究小组通过查阅资料得知:
a.K3[Fe(C2O4)3]·3H2O对光敏感,易溶于水,难溶于乙醇;
b.很多草酸盐(例如CaC2O4、BaC2O4)难溶于水,但能溶解于稀硝酸。
(4)步骤③中,控制水浴温度不能超过40℃的原因为
(5)研究小组的同学对K3[Fe(C2O4)3]组成有两种看法,分别为:
甲同学:K3[Fe(C2O4)3]由K+、Fe3+、
 构成;
构成;乙同学:K3[Fe(C2O4)3]由K+、[Fe(C2O4)3]3-构成。
请设计实验,验证哪位同学的说法是正确的:
(6)K3[Fe(C2O4)3]联合H2O2体系可用于降解染料,一定浓度的该混合溶液,在不同pH条件下降解刚果红的效率如图所示,在实际应用过程中,应选择pH=

(7)关于制备流程,下列说法正确的是___________。
| A.步骤①为复分解反应,步骤③为氧化还原反应 |
| B.步骤②判断沉淀是否洗涤干净,可以取少量最后一次洗涤液,加入氯化钡溶液,观察是否有白色沉淀产生 |
| C.步骤④,加入乙醇目的在于降低K3[Fe(C2O4)3]的溶解度,使其结晶析出 |
| D.步骤④⑤可以在日光下进行 |
(8)制得的K3[Fe(C2O4)3]·3H2O含少量FeC2O4·2H2O,为测定其纯度,进行如下实验:
步骤I:称取5.000g三草酸合铁酸钾晶体,配制成1.000L溶液,固体完全溶解。
步骤II:取20.00mL溶液,与0.1000molL-酸性KMnO4溶液反应,消耗2.46mL。
步骤III:另取20.00mL溶液,加入过量铜粉,过滤,洗涤,将滤液和洗涤液合并。
步骤IV:将合并液与0.1000mol/L酸性KMnO4溶液反应,消耗2.86mL。
已知
 与
与 的反应为(未配平):
的反应为(未配平): +
+ +H+→CO2↑+Mn2++H2O
+H+→CO2↑+Mn2++H2O①写出Fe2+与酸性KMnO4溶液反应的离子方程式:
②研究小组制得的K3[Fe(C2O4)3]·3H2O纯度为
您最近一年使用:0次
3 . 下列关于各图的说法错误的是
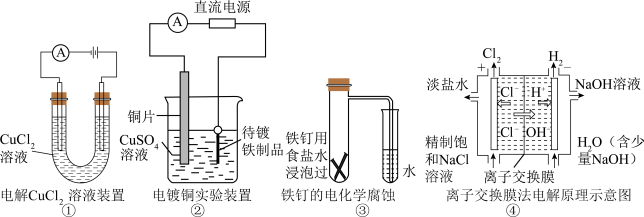

| A.①中阳极处能产生使湿润的淀粉-KI试纸变蓝的气体 |
| B.②中待镀铁制品应与电源负极相连而形成铜镀层 |
| C.③中可证明铁发生了析氢腐蚀 |
D.④中的离子交换膜可以避免生成的 与NaOH溶液反应 与NaOH溶液反应 |
您最近一年使用:0次
2023-10-22更新
|
753次组卷
|
6卷引用:福建省厦门外国语学校2023-2024学年高二上学期期中考试化学试题
名校
解题方法
4 . 近年来,锂介导的氮还原已被证明是一种有前途的电化学合成氨的方法,其电合成氨装置如图所示,下列说法错误的是
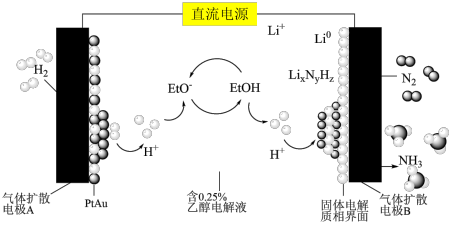

| A.电极A的电势高于电极B |
| B.阴极电极反应式为N2+2Li++4H++6e—=2LiNH2 |
| C.由图可知该装置反应前后,理论上乙醇的浓度不变 |
| D.理论上若电解液传导6molH+,最多生成标准状况下33.6LNH3 |
您最近一年使用:0次
2023-06-18更新
|
663次组卷
|
5卷引用:福建省厦门大学附属科技中学2023-2024学年高二上学期第一次月考化学试题
福建省厦门大学附属科技中学2023-2024学年高二上学期第一次月考化学试题安徽省合肥一六八中学2023届高三下学期最后一卷理科综合化学试题(已下线)专题05 电化学原理的综合应用(一题多问)(已下线)考点19 电解池(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第七章单元测试卷
名校
5 . 某实验小组利用下图装置探究H2C2O4溶液与酸性KMnO4溶液的反应(夹持装置略去)。

查阅资料:①H2C2O4为二元弱酸。
②溶液浓度越大,越不利于气体的扩散。
(1)H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为___________ 。
(2)仪器A的名称为___________ 。
(3)检查装置气密性的方法为___________ 。
(4)若以单位时间内生成的气体体积作为反应速率的观测指标,则量筒中的试剂为___________。
(5)探究H2C2O4溶液与酸性KMnO4溶液的浓度对反应速率的影响,实验数据如下表所示:
①c1=___________ 。
②某同学从实验1和2的褪色时间分析出实验2的反应速率小于实验1,请分析该结论是否正确,并说明原因:___________ 。
③结合实验数据,下列说法错误的是___________ 。(填标号)
A.其他条件不变时,c(H2C2O4)浓度越高,反应速率越快
B.其他条件不变时,当c(H2C2O4)为0.8mol·L-1,褪色时间一定介于163s至360s之间
C.实验5中v(H2C2O4)=0.15mol·L-1·min-1
D.其他条件不变时,当c(H2C2O4)>0.9mol·L-1,溶液浓度增大,不利于CO2扩散,可能导致褪色时间延长
(6)H2C2O4溶液与酸性KMnO4溶液生成的Mn2+对该反应有催化作用。请以实验1为对照组,设计实验方案证明Mn2+的催化作用___________ 。

查阅资料:①H2C2O4为二元弱酸。
②溶液浓度越大,越不利于气体的扩散。
(1)H2C2O4溶液与酸性KMnO4溶液反应的离子方程式为
(2)仪器A的名称为
(3)检查装置气密性的方法为
(4)若以单位时间内生成的气体体积作为反应速率的观测指标,则量筒中的试剂为___________。
| A.饱和NaHCO3溶液 | B.饱和NaCl溶液 | C.水 | D.饱和Na2CO3溶液 |
| 实验 序号 | KMnO4溶液 | H2C2O4溶液 | H2SO4溶液 | 褪色时间 | ||
| c/(mol·L-1) | V/mL | c/(mol·L-1) | V/mL | c/(mol·L-1) | t/s | |
| 1 | 0.005 | 4.0 | 0.2 | 2.0 | 0.120 | 307 |
| 2 | 0.020 | 4.0 | 0.2 | 2.0 | 0.120 | 545 |
| 3 | 0.010 | 4.0 | 0.5 | 2.0 | 0.120 | 201 |
| 4 | 0.010 | 4.0 | 0.7 | 2.0 | 0.120 | 163 |
| 5 | 0.010 | 4.0 | 0.9 | 2.0 | 0.120 | 360 |
| 6 | 0.010 | 4.0 | 1.0 | 2.0 | c1 | 512 |
②某同学从实验1和2的褪色时间分析出实验2的反应速率小于实验1,请分析该结论是否正确,并说明原因:
③结合实验数据,下列说法错误的是
A.其他条件不变时,c(H2C2O4)浓度越高,反应速率越快
B.其他条件不变时,当c(H2C2O4)为0.8mol·L-1,褪色时间一定介于163s至360s之间
C.实验5中v(H2C2O4)=0.15mol·L-1·min-1
D.其他条件不变时,当c(H2C2O4)>0.9mol·L-1,溶液浓度增大,不利于CO2扩散,可能导致褪色时间延长
(6)H2C2O4溶液与酸性KMnO4溶液生成的Mn2+对该反应有催化作用。请以实验1为对照组,设计实验方案证明Mn2+的催化作用
您最近一年使用:0次
2023-07-12更新
|
428次组卷
|
2卷引用:福建省厦门市2022-2023学年高一下学期期末考试化学试题
6 . 实验室可用浓硫酸与铜在加热条件下制备 ,实验装置如图。回答下列问题:
,实验装置如图。回答下列问题:
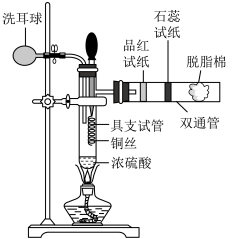
已知:①浓硫酸的沸点约为338℃。
② 、
、 均为黑色沉淀,不溶于稀盐酸与稀硫酸。
均为黑色沉淀,不溶于稀盐酸与稀硫酸。
③ 显黄绿色。
显黄绿色。
(1)制备 的化学方程式为
的化学方程式为_______ 。
(2)脱脂棉应蘸有_______ (填化学式)溶液。
(3)加热具支试管中的硫酸至沸腾,伸入铜丝,5s后观察到石蕊试纸变红,10s后观察到溶液颜色为蓝色,20s后观察到品红试纸褪色,5min后溶液蓝色逐渐变浅,同时底部生成灰白色沉淀。
①灰白色沉淀的主要成分为_______ ,该沉淀的生成体现了浓硫酸的_______ (填标号)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
②某同学认为硫酸蒸气也能使石蕊试纸变红,因此不能说明反应生成了 ,设计实验证明该猜想:
,设计实验证明该猜想:_______ 。
③为避免硫酸蒸气对反应的干扰,应如何改进实验装置:_______ 。
(4)反应过程中还观察到铜丝表面附着少量黑色物质(主要成分为 、
、 ),一些文献中认为
),一些文献中认为 是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在
是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在 ,为验证该说法,设计实验如下:
,为验证该说法,设计实验如下:
①实验Ⅱ应加入_______ HCl溶液。
②上述实验表明, 与酸的反应受到
与酸的反应受到 浓度、
浓度、_______ 、_______ 等因素的影响。
③产生实验Ⅲ现象的原因是_______ 。
④设计实验证明铜丝表面附着的黑色物质是否含有
_______ 。
 ,实验装置如图。回答下列问题:
,实验装置如图。回答下列问题:
已知:①浓硫酸的沸点约为338℃。
②
 、
、 均为黑色沉淀,不溶于稀盐酸与稀硫酸。
均为黑色沉淀,不溶于稀盐酸与稀硫酸。③
 显黄绿色。
显黄绿色。(1)制备
 的化学方程式为
的化学方程式为(2)脱脂棉应蘸有
(3)加热具支试管中的硫酸至沸腾,伸入铜丝,5s后观察到石蕊试纸变红,10s后观察到溶液颜色为蓝色,20s后观察到品红试纸褪色,5min后溶液蓝色逐渐变浅,同时底部生成灰白色沉淀。
①灰白色沉淀的主要成分为
A.酸性 B.氧化性 C.吸水性 D.脱水性
②某同学认为硫酸蒸气也能使石蕊试纸变红,因此不能说明反应生成了
 ,设计实验证明该猜想:
,设计实验证明该猜想:③为避免硫酸蒸气对反应的干扰,应如何改进实验装置:
(4)反应过程中还观察到铜丝表面附着少量黑色物质(主要成分为
 、
、 ),一些文献中认为
),一些文献中认为 是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在
是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在 ,为验证该说法,设计实验如下:
,为验证该说法,设计实验如下:| 实验组别 | 实验 | 现象 |
| Ⅰ | 取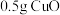 黑色粉末加入 黑色粉末加入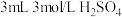 (过量)溶液中,充分振荡 (过量)溶液中,充分振荡 | 溶液显淡蓝色,放置1天后,蓝色变深,仍有大量黑色粉末未溶解 |
| Ⅱ | 取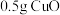 黑色粉末加入_______HCl(过量)溶液中,充分振荡 黑色粉末加入_______HCl(过量)溶液中,充分振荡 | 快速溶解,溶液显黄绿色 |
| Ⅲ | 取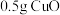 黑色粉末加入 黑色粉末加入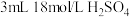 (过量)溶液中,充分振荡 (过量)溶液中,充分振荡 | 黑色粉末不溶解,溶液不变色 |
| Ⅳ | 将实验Ⅲ的溶液加热至沸腾 | 黑色粉末部分溶解,仍有较多黑色固体,溶液显淡蓝色 |
②上述实验表明,
 与酸的反应受到
与酸的反应受到 浓度、
浓度、③产生实验Ⅲ现象的原因是
④设计实验证明铜丝表面附着的黑色物质是否含有

您最近一年使用:0次
7 . 实验室可以浓硫酸与铜在加热条件下制备 ,实验装置如图。回答下列问题:
,实验装置如图。回答下列问题:

已知:①浓硫酸的沸点约为338℃。
② 、
、 均为黑色沉淀,不溶于稀盐酸与稀硫酸。
均为黑色沉淀,不溶于稀盐酸与稀硫酸。
③ 显黄绿色。
显黄绿色。
(1)制备 的化学方程式为
的化学方程式为_______ 。
(2)脱脂棉应蘸有_______ (填化学式)溶液。
(3)加热具支试管中的硫酸至沸腾,伸入铜丝,5s后观察到石蕊试纸变红,10s后观察到溶液变为蓝色,20s后观察到品红试纸褪色,5min后溶液蓝色逐渐变浅,同时底部生成灰白色沉淀。
①灰白色沉淀的主要成分为_______ ,该沉淀的生成体现了浓硫酸的_______ (填标号)。
A. 酸性 B. 氧化性 C. 吸水性 D. 脱水性
②某同学认为硫酸蒸气也能使石蕊试纸变红,因此不能说明反应生成了 ,设计实验证明该猜想:
,设计实验证明该猜想:_______ 。
③为避免硫酸蒸气对反应的干扰,应如何改进实验装置:_______ 。
(4)反应过程中还观察到铜丝表面附着少量黑色物质(主要成分为 、
、 ),一些文献中认为
),一些文献中认为 是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在
是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在 ,为验证该说法,设计实验如下:
,为验证该说法,设计实验如下:
①实验Ⅱ应加入_______  溶液。
溶液。
②上述实验表明, 与酸的反应受到
与酸的反应受到 浓度、
浓度、_______ 、_______ 等因素的影响。
③产生实验Ⅲ现象的原因是_______ 。
④设计实验证明铜丝表面附着的黑色物质是否含有
_______ 。
 ,实验装置如图。回答下列问题:
,实验装置如图。回答下列问题:
已知:①浓硫酸的沸点约为338℃。
②
 、
、 均为黑色沉淀,不溶于稀盐酸与稀硫酸。
均为黑色沉淀,不溶于稀盐酸与稀硫酸。③
 显黄绿色。
显黄绿色。(1)制备
 的化学方程式为
的化学方程式为(2)脱脂棉应蘸有
(3)加热具支试管中的硫酸至沸腾,伸入铜丝,5s后观察到石蕊试纸变红,10s后观察到溶液变为蓝色,20s后观察到品红试纸褪色,5min后溶液蓝色逐渐变浅,同时底部生成灰白色沉淀。
①灰白色沉淀的主要成分为
A. 酸性 B. 氧化性 C. 吸水性 D. 脱水性
②某同学认为硫酸蒸气也能使石蕊试纸变红,因此不能说明反应生成了
 ,设计实验证明该猜想:
,设计实验证明该猜想:③为避免硫酸蒸气对反应的干扰,应如何改进实验装置:
(4)反应过程中还观察到铜丝表面附着少量黑色物质(主要成分为
 、
、 ),一些文献中认为
),一些文献中认为 是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在
是碱性氧化物,很容易和酸反应,所以黑色物质中不可能存在 ,为验证该说法,设计实验如下:
,为验证该说法,设计实验如下:| 实验组别 | 实验 | 现象 |
| Ⅰ | 取 黑色粉末加入 黑色粉末加入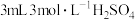 (过量)溶液中,充分振荡 (过量)溶液中,充分振荡 | 溶液显淡蓝色,放置1天后,蓝色变深,仍有大量黑色粉末未溶解 |
| Ⅱ | 取 黑色粉末加入_______ 黑色粉末加入_______ (过量)溶液中,充分振荡 (过量)溶液中,充分振荡 | 快速溶解,溶液显黄绿色 |
| Ⅲ | 取 黑色粉末加入 黑色粉末加入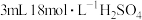 (过量)溶液中,充分振荡 (过量)溶液中,充分振荡 | 黑色粉末不溶解,溶液不变色 |
| Ⅳ | 将实验Ⅲ的溶液加热至沸腾 | 黑色粉末部分溶解,仍有较多黑色固体,溶液显淡蓝色 |
 溶液。
溶液。②上述实验表明,
 与酸的反应受到
与酸的反应受到 浓度、
浓度、③产生实验Ⅲ现象的原因是
④设计实验证明铜丝表面附着的黑色物质是否含有

您最近一年使用:0次
解题方法
8 . 自然界中有多种铁矿石,如磁铁矿(Fe3O4)、赤铁矿(Fe2O3)和菱铁矿(FeCO3)等。铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(设杂质中不含铁元素和氧元素,且杂质不与稀硫酸反应)。某研究性学习小组对某铁矿石中铁的价态和氧化物的化学式进行探究。
【提出假设】
假设1:铁矿石中只含+3价铁;
假设2:铁矿石中只含+2价铁;
假设3:____ 。
【查阅资料】2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
【定性研究】
实验(一)
取铁矿石样品粉碎,盛装于烧杯中,加入适量的X溶液,微热,充分溶解后将滤液分成四份:
①向第一份溶液中滴加少量KSCN溶液;
②向第二份溶液中滴加适量高锰酸钾溶液;
③向第三份溶液中滴加少量KSCN溶液,再滴加适量双氧水溶液;
④向第四份溶液中滴加适量氢氧化钠溶液。
(1)上述X溶液是____ (填“稀硝酸”、“稀硫酸”或“浓盐酸”);上述方案中,一定能证明铁矿石中含+2价铁的方案是____ (填序号)。
【定量研究】
实验(二)铁矿石中含氧量的测定:
①按图组装仪器,检查装置的气密性;
②将5.0g铁矿石放入硬质玻璃管中,其他装置中的药品如图所示(夹持装置已略去);
③A中开始反应,不断地缓缓向后续装置中通入氢气,待D装置出口处氢气验纯后,点燃C处酒精灯;
④充分反应后,撤掉酒精灯,再持续通入氢气直至完全冷却。

(2)按上述方案进行多次实验,假设各项操作都正确,但最终测得结果都偏高,请你提出改进方案的建议:____ 。如果拆去B装置,测得结果可能会___ (填“偏高”、“偏低”或“无影响”)。
(3)改进方案后,测得反应后D装置增重1.35g,则铁矿石中氧的百分含量为____ 。
若将H2换成CO,则还需补充____ 装置。有同学认为,不测定D装置的净增质量,通过测定物理量____ ,也能达到实验目的。
实验(三)铁矿石中含铁量的测定:

(4)步骤④中煮沸的作用是____ 。
(5)步骤⑤中用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还有___ 。
(6)下列有关步骤⑥的说法中正确的是___ (填序号)。
a.因为碘水为黄色,所以滴定过程中不需要加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不能用待装液润洗
e.滴定过程中,眼睛应注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(7)若滴定过程中消耗0.5000mol•L-1的KI溶液20.00mL,则铁矿石中铁的百分含量为____ 。综合实验(二)的结果,可以推算出该铁矿石中铁的氧化物的化学式为____ 。
【提出假设】
假设1:铁矿石中只含+3价铁;
假设2:铁矿石中只含+2价铁;
假设3:
【查阅资料】2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
【定性研究】
实验(一)
取铁矿石样品粉碎,盛装于烧杯中,加入适量的X溶液,微热,充分溶解后将滤液分成四份:
①向第一份溶液中滴加少量KSCN溶液;
②向第二份溶液中滴加适量高锰酸钾溶液;
③向第三份溶液中滴加少量KSCN溶液,再滴加适量双氧水溶液;
④向第四份溶液中滴加适量氢氧化钠溶液。
(1)上述X溶液是
【定量研究】
实验(二)铁矿石中含氧量的测定:
①按图组装仪器,检查装置的气密性;
②将5.0g铁矿石放入硬质玻璃管中,其他装置中的药品如图所示(夹持装置已略去);
③A中开始反应,不断地缓缓向后续装置中通入氢气,待D装置出口处氢气验纯后,点燃C处酒精灯;
④充分反应后,撤掉酒精灯,再持续通入氢气直至完全冷却。

(2)按上述方案进行多次实验,假设各项操作都正确,但最终测得结果都偏高,请你提出改进方案的建议:
(3)改进方案后,测得反应后D装置增重1.35g,则铁矿石中氧的百分含量为
若将H2换成CO,则还需补充
实验(三)铁矿石中含铁量的测定:

(4)步骤④中煮沸的作用是
(5)步骤⑤中用到的玻璃仪器除烧杯、玻璃棒、胶头滴管外,还有
(6)下列有关步骤⑥的说法中正确的是
a.因为碘水为黄色,所以滴定过程中不需要加指示剂
b.滴定过程中可利用淀粉溶液作为指示剂
c.滴定管用蒸馏水洗涤后可以直接装液
d.锥形瓶不能用待装液润洗
e.滴定过程中,眼睛应注视滴定管中液面变化
f.滴定结束后,30s内溶液不恢复原来的颜色,再读数
(7)若滴定过程中消耗0.5000mol•L-1的KI溶液20.00mL,则铁矿石中铁的百分含量为
您最近一年使用:0次
9 . 下列说法中正确的是( )
| A.某溶液加入AgNO3溶液产生了白色沉淀,证明该溶液中一定含有Cl— |
| B.某溶液加入BaCl2溶液产生白色沉淀,再加入稀HNO3,沉淀不消失,证明原溶液中一定存在SO42— |
| C.某化合物在焰色反应实验中出现黄色的火焰,则该化合物一定是钠盐 |
| D.某溶液与NaOH溶液共热,产生使湿润红色石蕊试纸变蓝气体,说明原溶液中存在NH4+ |
您最近一年使用:0次
2019-10-15更新
|
1027次组卷
|
11卷引用:福建省永泰县第一中学2019-2020学年高一上学期期中考试化学试题
福建省永泰县第一中学2019-2020学年高一上学期期中考试化学试题江苏省苏州市吴江区汾湖中学2019-2020学年高一上学期第一次月考化学试题江苏省苏州市吴江区吴江平望中学2020-2021学年高一上学期阶段性测试(一)化学试题江苏省扬州市宝应县2021-2022学年高一上学期期中检测化学试题江苏省徐州市沛县2022-2023学年高一上学期第一次学情调化学试题江苏省连云港市海州区四校2022-2023学年高一上学期期中考试化学试题天津市第二十中学2022-2023学年高一下学期3月月考化学试题江苏省连云港市东海县石榴高级中学2021-2022学年高一上学期第一次学情测试化学试卷四川省泸县第一中学2023-2024学年高一上学期10月月考化学试题江苏省徐州市第七中学2023-2024学年高一上学期9月月考化学试题江苏省扬州市广陵区红桥高级中学2023-2024学年高一上学期期中考试化学试卷
名校
10 . 进行下列实验,相关说法正确的是
A.图 :蒸干NH4Cl饱和溶液制备NH4Cl晶体 :蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
B.图: 形成美丽的红色喷泉,证明HCl极易溶于水 形成美丽的红色喷泉,证明HCl极易溶于水 |
C.图: 配制一定物质的量浓度的NaOH溶液,定容时如图则所配NaOH溶液浓度偏低 配制一定物质的量浓度的NaOH溶液,定容时如图则所配NaOH溶液浓度偏低 |
D.图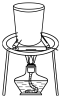 :所示装置用于除去碳酸氢钠固体中的少量碳酸钠 :所示装置用于除去碳酸氢钠固体中的少量碳酸钠 |
您最近一年使用:0次
2017-11-01更新
|
496次组卷
|
5卷引用:福建省惠安惠南中学2019届高三上学期期中考试化学试题



