1 . 由乙醇制备溴乙烷的装置如图所示。有关溴乙烷的制备实验,下列说法中错误的是
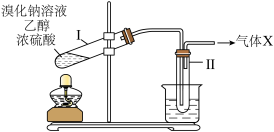
| A.药品的添加顺序为乙醇、浓硫酸、溴化钠溶液 |
| B.实验过程中,在试管Ⅱ中可观察到无色油状液体生成 |
| C.若检验出气体X中含水,可证明该制备反应为取代反应 |
| D.实验结束,先拆除试管Ⅱ,再熄灭酒精灯 |
您最近一年使用:0次
解题方法
2 . 利用淀粉和石蜡油合成有机溶剂 和化工原料
和化工原料 的工艺如图所示。
的工艺如图所示。
(1) 的名称为
的名称为______ ;C中官能团的名称为______ 。
(2)Ⅳ的反应类型为______ 。
(3)D是A的同系物,且相对分子量比A小,D的结构简式为_____ ,Ⅲ的化学方程式为______ 。
(4)下列关于有机物 的说法正确的是
的说法正确的是______ (填标号)。
a.在 的催化下可被
的催化下可被 氧化 b.所有原子在同一个平面上
氧化 b.所有原子在同一个平面上
c. 最多可消耗
最多可消耗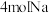 d.与
d.与 互为同分异构体
互为同分异构体
(5)为了验证反应Ⅰ并检验产物,某活动小组进行如图实验。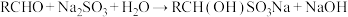
(ⅱ)有机物A与 溶液不反应
溶液不反应
①能证明生成了有机物B的实验现象为______ 。
②装置④中总反应的化学方程式为______ 。
 和化工原料
和化工原料 的工艺如图所示。
的工艺如图所示。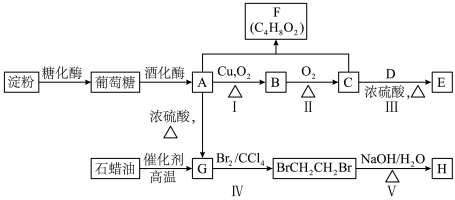

(1)
 的名称为
的名称为(2)Ⅳ的反应类型为
(3)D是A的同系物,且相对分子量比A小,D的结构简式为
(4)下列关于有机物
 的说法正确的是
的说法正确的是a.在
 的催化下可被
的催化下可被 氧化 b.所有原子在同一个平面上
氧化 b.所有原子在同一个平面上c.
 最多可消耗
最多可消耗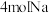 d.与
d.与 互为同分异构体
互为同分异构体(5)为了验证反应Ⅰ并检验产物,某活动小组进行如图实验。
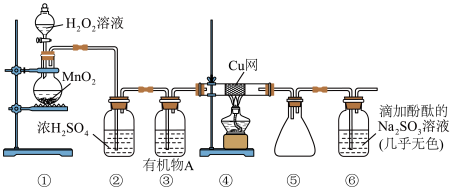
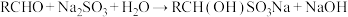
(ⅱ)有机物A与
 溶液不反应
溶液不反应①能证明生成了有机物B的实验现象为
②装置④中总反应的化学方程式为
您最近一年使用:0次
名校
解题方法
3 .  甲溶液可能含有
甲溶液可能含有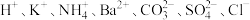 中的若干种。取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。下列说法中错误的是
中的若干种。取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。下列说法中错误的是
已知: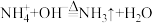
 甲溶液可能含有
甲溶液可能含有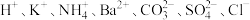 中的若干种。取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。下列说法中错误的是
中的若干种。取该溶液进行连续实验,过程如图(所加试剂均过量,气体全部逸出)。下列说法中错误的是已知:
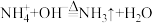
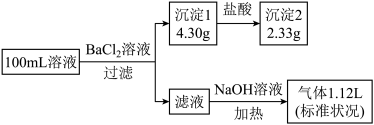
A.原溶液一定不存在 、 、 ,可能存在 ,可能存在 ,可通过焰色试验来检验 ,可通过焰色试验来检验 |
B.原溶液一定存在 ,且 ,且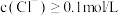 |
C.沉淀1转化为沉淀2时,放出的气体标况下的体积为 |
D.若滤液中先加 溶液,产生白色沉淀,再加足量稀硝酸沉淀不溶解,能证明原溶液中含有 溶液,产生白色沉淀,再加足量稀硝酸沉淀不溶解,能证明原溶液中含有 |
您最近一年使用:0次
2024-07-16更新
|
100次组卷
|
2卷引用:福建省三明市宁化第一中学2024-2025学年高三上学期暑期检测 化学试题
名校
4 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4.回答下列问题:
(1)W在周期表中的位置是___________ 。
(2)ZYX的电子式为___________ ,Z2Y2中含有的化学键类型为___________ 。
(3)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是___________ (用元素的离子符号表示)。
(4)下列说法能证明非金属性Q强于R的是___________ 。(填字母)。
a.简单阴离子的还原性:
b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:
d.Q的单质能从H2R溶液中置换出R单质
(5)W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的化学方程式为___________ 。
(1)W在周期表中的位置是
(2)ZYX的电子式为
(3)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(4)下列说法能证明非金属性Q强于R的是
a.简单阴离子的还原性:

b.简单氢化物热稳定性:Q>R
c.氧化物对应的水化物的酸性:

d.Q的单质能从H2R溶液中置换出R单质
(5)W的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
5 . 氮及其化合物的价类二维图如图所示,下列有关说法正确的是
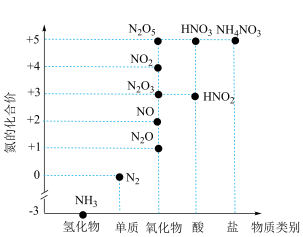
A. 受热易分解,可用作氮肥 受热易分解,可用作氮肥 |
B. 生成 生成 的过程属于氮的固定 的过程属于氮的固定 |
C.“雷雨发庄稼”的原理为: 盐 盐 |
D.向浓HNO3中投入红热的木炭,产生红棕色气体,证明木炭可与浓HNO3反应生成 |
您最近一年使用:0次
名校
6 . 下表是元素周期表的一部分,a~i分别代表9种元素,请回答:_______ (填元素符号)。
(2)b的最高价氧化物的结构式是_____ ,e的最高价氧化物对应水化物的电子式是_______ 。
(3)c、d、e、f中形成的简单离子半径由大到小的顺序是_______ (填离子符号)。
(4)元素g、h的最高价氧化物对应水化物中酸性较强的是______ (填化学式)。
(5)元素c、e可形成既含离子键又含非极性共价键的化合物,该化合物的化学式是_______ 。
(6)下列说法能证明金属性i强于f的是______ (填序号)。
A.i的简单阳离子的氧化性更弱
B.i的氢氧化物水溶液的导电性更强
C.i的单质与水反应更剧烈

(2)b的最高价氧化物的结构式是
(3)c、d、e、f中形成的简单离子半径由大到小的顺序是
(4)元素g、h的最高价氧化物对应水化物中酸性较强的是
(5)元素c、e可形成既含离子键又含非极性共价键的化合物,该化合物的化学式是
(6)下列说法能证明金属性i强于f的是
A.i的简单阳离子的氧化性更弱
B.i的氢氧化物水溶液的导电性更强
C.i的单质与水反应更剧烈
您最近一年使用:0次
2024-03-31更新
|
118次组卷
|
2卷引用:福建省莆田第十五中学2023-2024学年高一下学期第一次月考化学试题
名校
7 . 图a~c分别为氯化钠在不同状态下的导电实验(X、Y 均表示石墨电极)微观示意图。下列说法错误的是
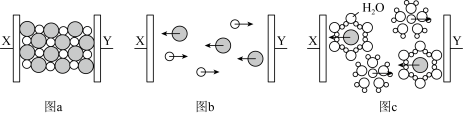
A.图示中 代表的离子的电子式为 代表的离子的电子式为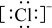 |
| B.图a中放入的是氯化钠固体,该条件下氯化钠不导电 |
| C.图b和图c中发生的变化完全相同,都是工业上生产钠的方法 |
| D.图b能证明氯化钠固体含有离子键 |
您最近一年使用:0次
2024-03-31更新
|
62次组卷
|
2卷引用:福建省三明市第一中学2023-2024学年高一下学期期中考试化学试题(选考)
名校
解题方法
8 . 下列说法不正确 的是
| A.常温下,测定0.1mol·L-1醋酸溶液的pH可证明醋酸是弱电解质 |
| B.等体积pH=2的两种酸分别与足量的铁反应,单位时间内酸性较强的酸与铁反应速率更快 |
| C.由反应NaR+CO2(少量)+H2O=HR+NaHCO3可知:Ka1(H2CO3)>Ka(HR)>Ka2(H2CO3) |
| D.室温下,pH=2的醋酸溶液和pH=12的氢氧化钠溶液等体积混合,混合溶液显酸性 |
您最近一年使用:0次
名校
解题方法
9 . 已知冰醋酸能与Cl2在I2催化下发生反应生成ClCH2COOH和HCl。对实验过程进行监测,发现反应过程中出现了C―I键,下列有关说法错误的是
| A.实验中C―I键的产生,可通过红外光谱结果证明 |
B.ClCH2COOH中存在 键 键 |
| C.C―I键比C―Cl键更易形成,且键能更大 |
D. 与 与 的空间构型相似 的空间构型相似 |
您最近一年使用:0次
名校
解题方法
10 . 用如图实验装置进行探究实验(b~d均为浸有相应试液的棉花),下列说法错误的是
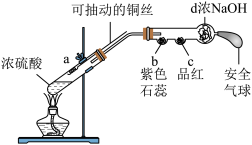

| A.上下移动a中铜丝可控制气体产生的量 |
| B.由b处变红色证明SO2为酸性氧化物 |
| C.由b、c处均褪色证明SO2具有漂白性 |
| D.安全气球的主要作用是收集SO2 |
您最近一年使用:0次



