解题方法
1 . 下列化学用语表示正确的是
A.苯的结构式: | B.氟化氢的电子式: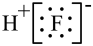 |
C. 的结构示意图: 的结构示意图: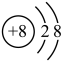 | D.氢氧化钠的电离方程式: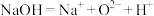 |
您最近一年使用:0次
解题方法
2 . 下列物质属于共价化合物的是
A.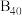 | B.NaOH | C.KF | D. |
您最近一年使用:0次
3 . 下列物质属于天然高分子化合物的是
| A.麦芽糖 | B.天然气 | C.聚乙烯 | D.蛋白质 |
您最近一年使用:0次
4 . 下列ETH天文研究所报告,组成太阳的气体中存在 和
和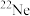 ,下列关于
,下列关于 和
和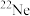 的说法正确的是
的说法正确的是
 和
和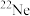 ,下列关于
,下列关于 和
和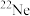 的说法正确的是
的说法正确的是A. 和 和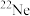 的中子数相同 的中子数相同 | B. 和 和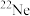 的核电荷数不同 的核电荷数不同 |
C. 和 和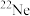 的质量数相同 的质量数相同 | D. 和 和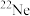 的电子数相同 的电子数相同 |
您最近一年使用:0次
5 . 下列物质的俗名和化学式相对应的是
A.纯碱—— | B.绿矾—— |
C.石膏—— | D.明矾——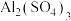 |
您最近一年使用:0次
解题方法
6 . 舍勒发现氯气是在1774年,当他使软锰矿与浓盐酸混合并加热时,产生了一种黄绿色的气体,发生的反应为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。氢气在氯气中燃烧为放热反应,下列说法正确的是
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。氢气在氯气中燃烧为放热反应,下列说法正确的是
 MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。氢气在氯气中燃烧为放热反应,下列说法正确的是
MnCl2+Cl2↑+2H2O,这种气体有强烈的刺激性气味。舍勒制备出氯气以后,把它溶解在水里,发现这种水溶液对纸张、蔬菜和花都具有永久性的漂白作用;他还发现氯气能与金属、非金属、碱等发生化学反应。氢气在氯气中燃烧为放热反应,下列说法正确的是| A.断开Cl-Cl键放出能量 | B.形成H-Cl键吸收能量 |
| C.燃烧都是放热反应 | D.反应物的总能量小于生成物的总能量 |
您最近一年使用:0次
解题方法
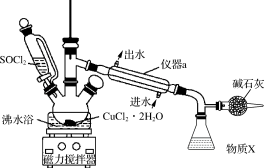
7 . 氯化铜在工农业生产中具有重要的用途。某化学兴趣小组设计如图所示装置,用CuCl2·2H2O晶体和SOCl2获取无水CuCl2,并回收过量的SOCl2。回答下列问题:
②三颈烧瓶中发生反应的化学方程式是CuCl2·2H2O+2SOCl2 CuCl2+2SO2↑+4HCl↑。
CuCl2+2SO2↑+4HCl↑。
(1)仪器a的名称是_______ ,锥形瓶中得到的物质X的化学式为_______ 。
(2)碱石灰中含有CaO和NaOH,碱石灰的作用是_______
(3)某同学用“间接碘量法”测定无水CuCl2样品中铜元素的百分含量,过程如下:取0.2800g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL(滴定反应为I2+2S2O =S4O
=S4O +2I-)。
+2I-)。
①滴定到终点时溶液中的颜色变化是_______
②该试样中铜元素的百分含量为_______ 。
②三颈烧瓶中发生反应的化学方程式是CuCl2·2H2O+2SOCl2
 CuCl2+2SO2↑+4HCl↑。
CuCl2+2SO2↑+4HCl↑。(1)仪器a的名称是
(2)碱石灰中含有CaO和NaOH,碱石灰的作用是
(3)某同学用“间接碘量法”测定无水CuCl2样品中铜元素的百分含量,过程如下:取0.2800g试样溶于水,加入过量KI固体,充分反应,生成白色CuI沉淀。滴入几滴淀粉溶液作指示剂,用0.1000mol·L-1Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液20.00mL(滴定反应为I2+2S2O
 =S4O
=S4O +2I-)。
+2I-)。①滴定到终点时溶液中的颜色变化是
②该试样中铜元素的百分含量为
您最近一年使用:0次
解题方法
8 . 利用废旧镀锌铁皮制备Fe3O4胶体粒子的流程如下:
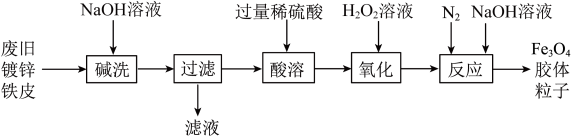
| A.Fe3O4俗称铁红 |
| B.“碱洗”的主要目的是除去镀锌铁皮表面的油污 |
| C.“酸溶”反应的离子方程式为Fe+2H+=Fe2++H2↑ |
D.“氧化”后溶液中所存在的离子为:H+、Fe3+、SO |
您最近一年使用:0次
9 . 下列有机反应方程式书写正确且属于取代反应是
| A.CH2=CH2+Br2→CH2BrCH2Br |
B.CH3CH2OH + CH3COOH 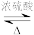 CH3COOC2H5+H2O CH3COOC2H5+H2O |
C.CH4+Cl2 CH2Cl2+H2 CH2Cl2+H2 |
D.2CH3CH2OH+O2 2CH3CHO+2H2O 2CH3CHO+2H2O |
您最近一年使用:0次
解题方法
10 . 下列指定反应的离子方程式正确的是
A.碳酸氢钠和过量氢氧化钙反应:HCO +Ca2++OH-= CaCO3↓+H2O +Ca2++OH-= CaCO3↓+H2O |
B.用稀硝酸与铜反应:Cu+4H++ 2NO = Cu2++2NO2↑+2H2O = Cu2++2NO2↑+2H2O |
| C.氯气溶于水:Cl2+H2O=2H++Cl-+ClO- |
| D.H2SO4溶液与氨水反应:H++OH-=H2O |
您最近一年使用:0次



