解题方法
1 . 已知SO2、Cl2和水的反应为SO2+Cl2+2H2O=H2SO4+2HCl,下列说法正确的是
A.硫酸的电离方程式:H2SO4=H +SO +SO | B. 、 、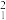 H和 H和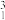 H互为同位素 H互为同位素 |
C.中子数为20的氯原子: | D.SO2属于电解质 |
您最近一年使用:0次
2 . 下列物质互为同分异构体的一组是
A.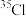 和 和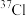 | B.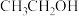 和 和 |
C. 和 和 | D. 和 和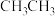 |
您最近一年使用:0次
2024-04-09更新
|
292次组卷
|
3卷引用:2024年江苏省徐州市沛县汉台高级中学学业水平考试化学试题
3 . 在水溶液中能大量共存的一组离子是
A.Na+、Ba2+、Cl-、 | B.Pb2+、Hg2+、S2-、 |
C. 、H+、 、H+、 、 、 | D.Ca2+、Al3+、Br-、 |
您最近一年使用:0次
名校
解题方法
4 . 连二亚硫酸钠(Na2S2O4)俗称保险粉,广泛应用于纺织业和造纸业。利用碱性NaBH4溶液或Zn还原含硫化合物是制备Na2S2O4常用方法。
已知:①Na2S2O4在水溶液可以发生歧化反应(只有S元素化合价的升降),受热易分解。
②NaBH4是一种强还原剂,酸性或受热条件下易与水反应产生氢气,在碱性溶液中比较稳定。
③生成物的ΔG越大,表示在该条件下转化成该物质的可能性较大。溶液中部分含硫组分的ΔG如图所示。

Ⅰ.NaBH4碱性溶液还原法
(1)12%NaBH4碱性溶液配制:在烧杯中加入48g水,再向其中加入___________ (请完成溶液配制,所需试剂为40gNaOH固体及12gNaBH4固体)。
(2)溶有饱和SO2的NaHSO3溶液制备:利用如图所示装置来制备该溶液,判断制备完成的方法是___________ 。

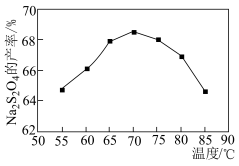
(3)将12%NaBH4碱性溶液与制备的NaHSO3溶液在无氧、水浴加热的条件下发生反应,相同时间内,Na2S2O4的产率随温度的变化如图所示,70℃后Na2S2O4的产率下降的原因是___________ 。Na2S2O4在水溶液中发生歧化反应的离子方程式为___________ 。
Ⅱ.锌粉还原法
已知:①Zn+2H2SO3 ZnS2O4(易溶于水)+2H2O;
ZnS2O4(易溶于水)+2H2O;
②二价锌在水溶液中的存在形式与pH的关系如图所示。
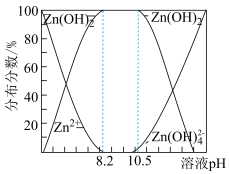
(4)请补充完整由锌粉制备Na2S2O4粗品的实验方案:向盛有水的烧杯中加入一定量的Zn粉,搅拌,___________ ,向滤液中加入氯化钠粉末至有大量晶体析出,过滤得到Na2S2O4粗品(实验中须使用的试剂:SO2、1mol·L-1NaOH溶液)。
已知:①Na2S2O4在水溶液可以发生歧化反应(只有S元素化合价的升降),受热易分解。
②NaBH4是一种强还原剂,酸性或受热条件下易与水反应产生氢气,在碱性溶液中比较稳定。
③生成物的ΔG越大,表示在该条件下转化成该物质的可能性较大。溶液中部分含硫组分的ΔG如图所示。

Ⅰ.NaBH4碱性溶液还原法
(1)12%NaBH4碱性溶液配制:在烧杯中加入48g水,再向其中加入
(2)溶有饱和SO2的NaHSO3溶液制备:利用如图所示装置来制备该溶液,判断制备完成的方法是

(3)将12%NaBH4碱性溶液与制备的NaHSO3溶液在无氧、水浴加热的条件下发生反应,相同时间内,Na2S2O4的产率随温度的变化如图所示,70℃后Na2S2O4的产率下降的原因是

Ⅱ.锌粉还原法
已知:①Zn+2H2SO3
 ZnS2O4(易溶于水)+2H2O;
ZnS2O4(易溶于水)+2H2O;②二价锌在水溶液中的存在形式与pH的关系如图所示。

(4)请补充完整由锌粉制备Na2S2O4粗品的实验方案:向盛有水的烧杯中加入一定量的Zn粉,搅拌,
您最近一年使用:0次
2024-02-22更新
|
347次组卷
|
2卷引用:江苏省南通市如东中学,如东一高等四校2023-2024学年高三上学期12月学情调研化学试题
名校
5 . 交警用经硫酸酸化处理的三氧化铬(CrO3)(与重铬酸钾原理类似)检查司机呼出的气体:2K2Cr2O7+3CH3CH2OH+8H2SO4=2Cr2(SO4)3+3CH3COOH+2K2SO4+11H2O,根据颜色的变化(橙黄变灰绿),可以判断司机是否酒后驾车。下列有关说法正确的是
| A.Cr3+价电子排布式为3d24s1 |
B.SO 空间结构为正四面体形 空间结构为正四面体形 |
| C.CH3COOH中碳原子杂化类型为sp杂化 |
D.基态硫原子核外价电子的轨道表示式为 |
您最近一年使用:0次
名校
6 . 某工厂采用如下工艺处理镍钴矿硫酸浸取液(含Ni2+、Co2+、Fe2+、Fe3+、Mg2+和Mn2+),实现镍、钴、镁元素的回收。
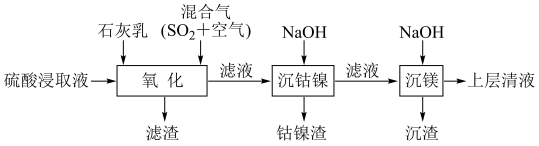
回答下列问题:
(1)在一定温度下,用硫酸浸取已粉碎的镍钴矿时,提高浸取速率的方法为___________ 。(答出一条即可)
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H2SO5),写出H2SO5的结构式:___________ 。
(3)“氧化”中,用石灰乳调节pH=4,Mn2+被H2SO5氧化为MnO2,该反应的离子方程式为___________ 。(H2SO5的电离第一步完全,第二步微弱)
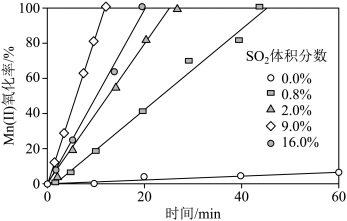
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如图。SO2体积分数为9%时,Mn(Ⅱ)氧化速率最大;继续增大SO2体积分数时,Mn(Ⅱ)氧化速率减小的原因是___________ 。
(5)将“钴镍渣”酸溶后,进行如下流程:
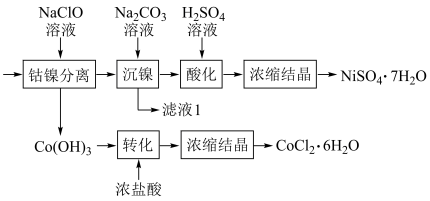
①写出“钴镍分离”时发生反应的离子方程式:___________ 。
②“镍钴分离”后溶液中c(Ni2+)=1.0mol·L-1,若“滤液1”中c(CO )=10-5mol·L-1,则沉镍率=
)=10-5mol·L-1,则沉镍率=___________ (要求写出计算过程)。[已知:Ksp(NiCO3)=1.0×10-7,沉镍率= ]
]

回答下列问题:
(1)在一定温度下,用硫酸浸取已粉碎的镍钴矿时,提高浸取速率的方法为
(2)“氧化”中,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H2SO5),写出H2SO5的结构式:
(3)“氧化”中,用石灰乳调节pH=4,Mn2+被H2SO5氧化为MnO2,该反应的离子方程式为
(4)“氧化”中保持空气通入速率不变,Mn(Ⅱ)氧化率与时间的关系如图。SO2体积分数为9%时,Mn(Ⅱ)氧化速率最大;继续增大SO2体积分数时,Mn(Ⅱ)氧化速率减小的原因是

(5)将“钴镍渣”酸溶后,进行如下流程:

①写出“钴镍分离”时发生反应的离子方程式:
②“镍钴分离”后溶液中c(Ni2+)=1.0mol·L-1,若“滤液1”中c(CO
 )=10-5mol·L-1,则沉镍率=
)=10-5mol·L-1,则沉镍率= ]
]
您最近一年使用:0次
名校
解题方法
7 . 下列有关物质的性质与用途具有对应关系的是
| A.Al(OH)3具有两性,可用作塑料制品的阻燃剂 |
| B.H2O2具有强氧化性,可用于杀菌消毒 |
| C.炭黑硬度大,可用于电极材料 |
| D.铜的金属活动性比铁弱,可在海轮外壳上装若干铜块以减缓其腐蚀速率 |
您最近一年使用:0次
名校
解题方法
8 . 关于氢能源制取和CO2减排和成为研究热点。
(一)热解H2S制H2.根据文献,将H2S和CH4的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
Ⅰ.2H2S(s) 2H2(g)+S2(g);ΔH1=170kJ·mol-1
2H2(g)+S2(g);ΔH1=170kJ·mol-1
Ⅱ.CH4(g)+S2(g) CS2(g)+2H2(g);ΔH2=64kJ·mol-1
CS2(g)+2H2(g);ΔH2=64kJ·mol-1
总反应:Ⅲ.2H2S(g)+CH4(g) CS2(g)+4H2(g)
CS2(g)+4H2(g)
投料按体积之比V(H2S)∶V(CH4)=2∶1,并用N2稀释;常压,不同温度下反应相同时间后,测得H2和CS2体积分数如下表:
(1)①已知ΔG=ΔH-TΔS,当ΔG<0时,反应Ⅲ能自发进行的条件是___________ 。
②在950~1150℃范围内(其他条件不变),S2(g)的体积分数随温度升高的变化是___________ (填“先升高后降低”或“先降低后升高”),分析原因:___________ 。
(二)我国科学家研究LiCO2电池,在获得能量的同时可以达到碳固定的目的。LiCO2电池中,Li为单质锂片。研究表明,该电池反应产物为碳酸锂和单质碳,且CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行。
Ⅰ.2CO2+2e-=C2O
Ⅱ.C2O =CO2+CO
=CO2+CO
Ⅲ.___________
Ⅳ.CO +2Li+=Li2CO3
+2Li+=Li2CO3
(2)写出步骤Ⅲ的离子方程式________ 。
(三)科研的工作者通过开发新型催化剂,利用太阳能电池将工业排放的CO2转化为HCOOH,实现碳减排的目标,如图所示。
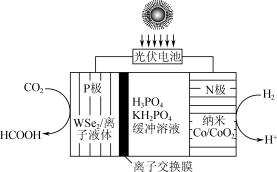
(3)①离子交换膜为质子交换膜,当消耗标准状况下11.2LH2时,P极电解液质量变化情况为___________ 。
②光伏电池中涉及NOCl光化学分解反应,在一定频率(ν)光的照射下机理如下:NOCl+hν→NOCl*、NOCl+NOCl*→2NO+Cl2,其中hν表示一个光子能量,NOCl*表示NOCl的激发态。可知,分解1mol的NOCl需要吸收___________ mol光子。
(四)已知反应CO2(g)+H2(g) HCOOH(g);ΔH<0。温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应CO2(g)+H2(g)
HCOOH(g);ΔH<0。温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应CO2(g)+H2(g) HCOOH(g) K=2。
HCOOH(g) K=2。
(4)实验测得v正=k正c(CO2)c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。温度为T2℃时,k正=1.8k逆,则T2℃>T1℃,请通过计算说明原因:___________ 。
(一)热解H2S制H2.根据文献,将H2S和CH4的混合气体导入石英管反应器热解(一边进料,另一边出料),发生如下反应:
Ⅰ.2H2S(s)
 2H2(g)+S2(g);ΔH1=170kJ·mol-1
2H2(g)+S2(g);ΔH1=170kJ·mol-1Ⅱ.CH4(g)+S2(g)
 CS2(g)+2H2(g);ΔH2=64kJ·mol-1
CS2(g)+2H2(g);ΔH2=64kJ·mol-1总反应:Ⅲ.2H2S(g)+CH4(g)
 CS2(g)+4H2(g)
CS2(g)+4H2(g)投料按体积之比V(H2S)∶V(CH4)=2∶1,并用N2稀释;常压,不同温度下反应相同时间后,测得H2和CS2体积分数如下表:
| 温度/℃ | 950 | 1000 | 1050 | 1100 | 1150 |
| H2/V(%) | 0.5 | 1.5 | 3.6 | 5.5 | 8.5 |
| CS2/V(%) | 0.0 | 0.0 | 0.1 | 0.4 | 1.8 |
(1)①已知ΔG=ΔH-TΔS,当ΔG<0时,反应Ⅲ能自发进行的条件是
②在950~1150℃范围内(其他条件不变),S2(g)的体积分数随温度升高的变化是
(二)我国科学家研究LiCO2电池,在获得能量的同时可以达到碳固定的目的。LiCO2电池中,Li为单质锂片。研究表明,该电池反应产物为碳酸锂和单质碳,且CO2电还原后与锂离子结合形成碳酸锂按以下4个步骤进行。
Ⅰ.2CO2+2e-=C2O

Ⅱ.C2O
 =CO2+CO
=CO2+CO
Ⅲ.___________
Ⅳ.CO
 +2Li+=Li2CO3
+2Li+=Li2CO3(2)写出步骤Ⅲ的离子方程式
(三)科研的工作者通过开发新型催化剂,利用太阳能电池将工业排放的CO2转化为HCOOH,实现碳减排的目标,如图所示。

(3)①离子交换膜为质子交换膜,当消耗标准状况下11.2LH2时,P极电解液质量变化情况为
②光伏电池中涉及NOCl光化学分解反应,在一定频率(ν)光的照射下机理如下:NOCl+hν→NOCl*、NOCl+NOCl*→2NO+Cl2,其中hν表示一个光子能量,NOCl*表示NOCl的激发态。可知,分解1mol的NOCl需要吸收
(四)已知反应CO2(g)+H2(g)
 HCOOH(g);ΔH<0。温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应CO2(g)+H2(g)
HCOOH(g);ΔH<0。温度为T1℃时,将等物质的量的CO2和H2充入体积为1L的密闭容器中发生反应CO2(g)+H2(g) HCOOH(g) K=2。
HCOOH(g) K=2。(4)实验测得v正=k正c(CO2)c(H2),v逆=k逆c(HCOOH),k正、k逆为速率常数。温度为T2℃时,k正=1.8k逆,则T2℃>T1℃,请通过计算说明原因:
您最近一年使用:0次
名校
9 . 化合物H(磷酸奥司他韦)适用于流感病毒的治疗,尤其对甲流效果明显,部分合成路线如下:
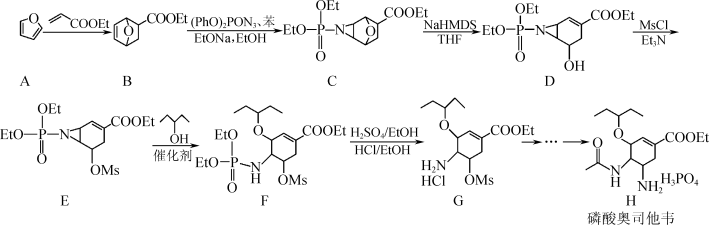
注:Et-:C2H5-;Ms-: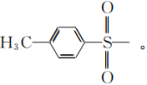
(1)H中含氧官能团的名称为醚键、___________ ;A→B的反应类型为___________ 。
(2)D→E反应中使用Et3N的作用为___________ 。
(3)E转化为F时有副产品M(与F互为同分异构体)生成,M的结构简式为___________ 。
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:___________ 。
①分子中含有3种不同化学环境的氢原子;
②不能与FeCl3发生显色反应;
③1mol该同分异构体能与活泼金属钠反应产生1.5molH2。
(5)写出以 、CH3CH2OH、(PhO)2PON3为原料制备
、CH3CH2OH、(PhO)2PON3为原料制备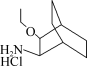 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。__________

注:Et-:C2H5-;Ms-:

(1)H中含氧官能团的名称为醚键、
(2)D→E反应中使用Et3N的作用为
(3)E转化为F时有副产品M(与F互为同分异构体)生成,M的结构简式为
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:
①分子中含有3种不同化学环境的氢原子;
②不能与FeCl3发生显色反应;
③1mol该同分异构体能与活泼金属钠反应产生1.5molH2。
(5)写出以
 、CH3CH2OH、(PhO)2PON3为原料制备
、CH3CH2OH、(PhO)2PON3为原料制备 的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
您最近一年使用:0次
10 . 下列设计的实验方案不能达到实验目的的是
| 选项 | 实验现象和操作 | 实验目的 |
| A | 向2mL0.1mol·L-1Na2S溶液中滴加0.1mol·L-1ZnSO4溶液至不再有沉淀产生,再滴加几滴0.1mol·L-1CuSO4溶液,出现黑色沉淀 | 验证Ksp(ZnS)>Ksp(CuS) |
| B | 向含有0.1mol的FeI2溶液中通入0.1molCl2,再加入淀粉溶液,溶液变蓝色 | 还原性:I->Fe2+ |
| C | 以Zn、Fe为电极,以酸化的3%NaCl溶液作电解质溶液,连接成原电池装置。过一段时间,从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴K3[Fe(CN)6]溶液,观察现象 | 探究金属的牺牲阳极保护法 |
| D | 向盛有2mL0.1mol·L-1K2Cr2O7溶液的试管中滴加5~10滴NaOH溶液,再继续滴加5~10滴6mol·L-1H2SO4溶液,观察现象 | 探究浓度对化学平衡的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



