1 . 三氧化砷,俗称砒霜,分子式As2O3,是最具商业价值的砷化合物及主要的砷化学开始物料。它也是最古老的毒物之一,无臭无味,外观为白色霜状粉末,故称砒霜。
(1)完成并配平下列化学方程式:___ As2O3+___ Zn+___ H2SO4→___ AsH3+___ ZnSO4+___
(2)As2O3在上述反应中显示出来的性质是___ 。
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.2molAsH3,则转移电子的物质的量为___ mol。
(4)砷化氢AsH3是一种很强的还原性,在室温下它能在空气中自然,其氧化产物是砒霜,写出该反应的化学方程式___ 。
(1)完成并配平下列化学方程式:
(2)As2O3在上述反应中显示出来的性质是
A.氧化性 B.还原性 C.酸性 D.碱性
(3)若生成0.2molAsH3,则转移电子的物质的量为
(4)砷化氢AsH3是一种很强的还原性,在室温下它能在空气中自然,其氧化产物是砒霜,写出该反应的化学方程式
您最近一年使用:0次
2020-03-21更新
|
336次组卷
|
4卷引用:沪科版化学拓展性课程4《离子互换反应和氧化还原反应》测试题
沪科版化学拓展性课程4《离子互换反应和氧化还原反应》测试题上海市六校联考2015-2016学年高三上学期期中考试化学试题2015届陕西省渭南市高三教学质量检测(一模)化学试卷(已下线)专题35 磷、砷及其化合物-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
2 . 绿矾(FeSO4·7H2O)可作还原剂、着色剂、制药等,在不同温度下易分解得各种铁的氧化物和硫的氧化物。已知SO3是一种无色晶体,熔点16.8℃,沸点44.8℃,氧化性及脱水性较浓硫酸强,能漂白某些有机染料,如品红等。回答下列问题:

(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是__________ ,甲组由此得出绿矾的分解产物中含有SO2。装置C的作用是______________ 。
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。乙对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中___________ 。(填字母)
A.不含SO2B.可能含SO2C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解气态产物的装置:
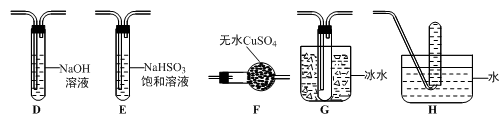
①丙组同学的实验装置中,依次连接的合理顺序为______________________ 。
②能证明绿矾分解产物中有O2的实验操作及现象是_______________________ 。
(4)为证明绿矾分解产物中含有三价铁,选用的实验仪器有试管、胶头滴管、_____________ ;选用的试剂为_____________ 。

(1)甲组同学按照上图所示的装置,通过实验检验绿矾的分解产物。装置B中可观察到的现象是
(2)乙组同学认为甲组同学的实验结论不严谨,认为需要补做实验。乙对甲组同学做完实验的B装置的试管加热,发现褪色的品红溶液未恢复红色,则可证明绿矾分解的产物中
A.不含SO2B.可能含SO2C.一定含有SO3
(3)丙组同学查阅资料发现绿矾受热分解还可能有O2放出,为此,丙组同学选用甲组同学的部分装置和下图部分装置设计出了一套检验绿矾分解气态产物的装置:

①丙组同学的实验装置中,依次连接的合理顺序为
②能证明绿矾分解产物中有O2的实验操作及现象是
(4)为证明绿矾分解产物中含有三价铁,选用的实验仪器有试管、胶头滴管、
您最近一年使用:0次
2017-02-17更新
|
2438次组卷
|
9卷引用:沪科版化学拓展性课程6《金属元素》测试题
解题方法
3 . 实验室可用如图装置制得氯气并与铝粉反应制备无水AlCl3。已知AlCl3在183°C升华,遇潮湿空气即反应产生大量白雾。请回答问题:
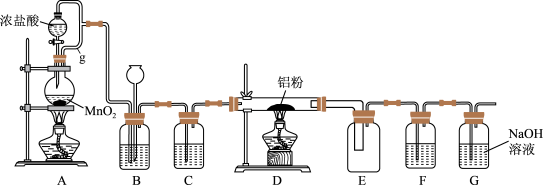
(1)A中反应的化学方程式为_________ ;HCl在反应中表现出的性质为______ (填:酸性、氧化性或还原性)。
(2)A中g管的作用是________ 。
(3)B中盛放饱和食盐水的作用是________ ;若D中生成的AlCl3凝华堵塞导管,B中可观察到的现象为________ 。
(4)C和F所装试剂相同,其中F的作用是___________ 。

(1)A中反应的化学方程式为
(2)A中g管的作用是
(3)B中盛放饱和食盐水的作用是
(4)C和F所装试剂相同,其中F的作用是
您最近一年使用:0次
2019-12-16更新
|
326次组卷
|
2卷引用:沪科版高二化学拓展性课程9《化学实验探究》测试题
9-10高二下·江苏盐城·期末
4 . 某化学兴趣小组进行如下实验:
实验① 向 晶体中滴加浓盐酸,产生黄绿色气体
晶体中滴加浓盐酸,产生黄绿色气体 ;
;
实验② 向 溶液中通入少量实验①中产生的
溶液中通入少量实验①中产生的 ,溶液变为黄色;
,溶液变为黄色;
实验③ 取实验②中生成的溶液滴在淀粉KI试纸上,试纸变为蓝色。
下列判断正确的是
实验① 向
 晶体中滴加浓盐酸,产生黄绿色气体
晶体中滴加浓盐酸,产生黄绿色气体 ;
;实验② 向
 溶液中通入少量实验①中产生的
溶液中通入少量实验①中产生的 ,溶液变为黄色;
,溶液变为黄色;实验③ 取实验②中生成的溶液滴在淀粉KI试纸上,试纸变为蓝色。
下列判断正确的是
A.上述实验证明氧化性: |
| B.上述实验中,共有两个氧化还原反应 |
C. 不能使湿润的淀粉KI试纸变蓝 不能使湿润的淀粉KI试纸变蓝 |
D.实验②证明 既有氧化性又有还原性 既有氧化性又有还原性 |
您最近一年使用:0次
2020-09-22更新
|
3193次组卷
|
60卷引用:沪科版高中化学拓展课程第4章《离子互换反应和氧化还原反应》检测题3
沪科版高中化学拓展课程第4章《离子互换反应和氧化还原反应》检测题32015届上海理工大学附中高三上学期月考化学试卷鲁教版高中化学必修1第三章《自然界中的元素》测试卷1(已下线)2010年江苏省盐城中学高二下学期期末考试化学试题(已下线)2010年江苏省南洋中学高二下学期期末考试化学试题(已下线)2010年浙江省杭州市七校高一上学期期中考试化学卷(已下线)2011年河南省卫辉市第一中学高一上学期期末质量检测化学试卷(已下线)2011届黑龙江省鸡西市第一中学高三第二次模拟考试化学试卷(已下线)2012届北京四中高三上学期期中测试化学试卷(已下线)2011-2012学年内蒙古巴彦淖尔市中学高一期中考试化学试卷(已下线)2012届陕西省西安市第一中学高三上学期期中考试化学试卷(已下线)2011-2012学年山东省临沂市高一上学期期末模块考试化学试卷(已下线)2011-2012学年内蒙古包头三十三中高一上学期期末考试化学试卷(已下线)2012-2013学年福建省莆田一中高一下学期第一学段考试化学试卷(已下线)2012-2013学年山东省临沂市重点高中高一上学期期末考试化学试卷(已下线)2013-2014学年内蒙古赤峰市元宝山区高一上学期期末化学试卷(已下线)2015届福建省安溪第八中学高三上学期期中质量检测化学试卷2014-2015山东省菏泽市高一上学期期末考试化学A试卷2016届广东省信宜市第一中学高三第一次段考理科综合化学试卷2015-2016学年江西省抚州市高一上学期期末化学试卷2015-2016学年广东省深圳市宝安中学高一上学期期末化学试卷2016-2017陕西西安长安区一中重点班高一12月考化学卷2016-2017学年江苏省泰州中学高一12月检测化学卷吉林省吉林市长春汽车经济开发区第六中学2016-2017学年高一下学期期末考试化学试题【全国校级联考】湖北省鄂西南三校合作体2017-2018学年高一下学期期中考试化学试题广西贵港市覃塘高级中学2018-2019学年高二上学期12月月考化学试题黑龙江省东宁市第一中学2018-2019学年高一下学期第一次月考化学试题云南省腾冲市第八中学2018-2019学年高一(理)下学期期中考试化学试题河南省安阳市第三十六中学2018-2019学年高二6月月考化学试题福建省莆田第八中学2018-2019学年高一下学期第二次月考化学试题重庆市云阳江口中学校2020届高三上学期第一次月考化学试题云南省石屏县二中2019-2020学年高二上学期开学考试化学试题甘肃省武威市第二中学2020届高三上学期10月月考化学试题辽宁省沈阳市城郊市重点联合体2019-2020学年高三上学期期中考试化学试题安徽省滁州市定远县育才学校2019-2020学年高二上学期期中考试(实验班)化学试题安徽省阜阳市第三中学2019-2020学年高一上学期期末考试化学试题云南省元谋县第一中学2019-2020学年高一上学期期末考试化学试题2019-2020学年高一上学期期末复习《新题速递·化学》12月(考点07-10)(已下线)【新东方】 2020-33福建省龙海市第二中学2019-2020学年高一下学期4月月考化学试题云南省昆明市寻甸县民族中学2019-2020学年高一下学期第一次月考化学试题山西省运城市芮城县2019-2020学年高二下学期期末调研测试化学试题(已下线)考点03 氧化还原反应-2020年【衔接教材·暑假作业】新高三一轮复习化学(已下线)第4讲 氧化还原反应-2021年高考化学一轮复习名师精讲练云南省云天化中学高中联盟学校2019~2020学年高一下学期期末考试化学试题山东省山东师范大学附属中学2019-2020学年高一上学期12月份月考化学试题(已下线)专题04 氧化还原反应(核心素养卷)——【新教材精创】2019-2020学年高中化学新教材知识讲学(已下线)小题必刷07 氧化还原反应概念及应用——2021年高考化学一轮复习小题必刷(通用版)人教版(2019)高一必修第一册 第三章 第一节 铁及其化合物鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第1节 铁的多样性高一必修第一册(鲁科2019)第2章 章末总结人教版(2019)高一必修第一册 第一章 物质及其变化 章末总结甘肃省天水市甘谷县第四中学2021届高三上学期第二次检测化学试题(已下线)内蒙古赤峰市宁城县2018-2019学年高一上学期期末考试化学试题北京清华大学附属中学2020-2021学年高一上学期期中考试化学试题江苏省南菁高级中学2020-2021学年高一上学期第一次阶段性检测考试化学试题2016-2017学年广东省仲元中学高一上学期期末考试化学试卷西北工业大学附属中学2022-2023学年高一上学期10月月考化学试题四川省宜宾市叙州区第二中学校2023-2024学年高一上学期10月月考化学试题北京市八一学校2023-2024学年高一上学期期中化学试卷
解题方法
5 . 有几种元素的微粒的最外电子层结构如图所示, 其中:
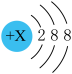
(1)某电中性微粒一般不和其他元素的原子反应, 这种微粒符号是_______ ;
(2)某微粒的盐溶液, 加入AgNO3溶液时会出现白色浑浊, 这种微粒符号是_____ ;
(3)某微粒氧化性甚弱, 但得到电子后还原性强, 且这种原子有一个单电子, 这种微粒的符号是_______ ;
(4)某微粒具有还原性, 且这种微粒失去 2 个电子即变为原子, 这种微粒的符号是___

(1)某电中性微粒一般不和其他元素的原子反应, 这种微粒符号是
(2)某微粒的盐溶液, 加入AgNO3溶液时会出现白色浑浊, 这种微粒符号是
(3)某微粒氧化性甚弱, 但得到电子后还原性强, 且这种原子有一个单电子, 这种微粒的符号是
(4)某微粒具有还原性, 且这种微粒失去 2 个电子即变为原子, 这种微粒的符号是
您最近一年使用:0次
6 . 下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)装置A是氯气的发生装置,请写出相应反应的化学方程式:__________ 。
(2)装置B中饱和食盐水的作用是___________ ;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:_______________ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是_________ 填字母编号)。
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是__________________________ ,该现象__________ (填“能”或“不能”)说明溴单质的氧化性强于碘,原因是____________ 。
(5)装置F的作用是__________________ ,其烧杯中的溶液不能选用下列中的_____ (填字母编号)。
a.饱和NaOH溶液b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液d.饱和Na2CO3溶液

(1)装置A是氯气的发生装置,请写出相应反应的化学方程式:
(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、II、III处依次放入物质的组合应是
| 编号 | I | II | III |
| a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
| c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
| d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是
(5)装置F的作用是
a.饱和NaOH溶液b.饱和Ca(OH)2溶液
c.饱和Na2SO3溶液d.饱和Na2CO3溶液
您最近一年使用:0次
名校
7 . 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
I.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
___ 与盐酸反应最剧烈;____ 与盐酸反应的速度最慢;___ 与盐酸反应产生的气体最多。
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由____ 。
II. 利用如图装置可验证同主族元素非金属性的变化规律。

(3)仪器B的名称为____ ,干燥管D的作用为___ 。
(4)若要证明非金属性Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液_____ (填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用____ 溶液吸收尾气。
(5)若要证明非金属性C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液____ (填现象),即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有_____ 溶液的洗气瓶除去。正交硫转化为单斜硫时,发生_____ (填“物理变化”或“化学变化”)。
I.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH碱性强于NH3·H2O,继而可以验证Na的金属性强于氮,你认为此设计是否合理?并说明理由
II. 利用如图装置可验证同主族元素非金属性的变化规律。

(3)仪器B的名称为
(4)若要证明非金属性Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C中溶液
(5)若要证明非金属性C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液,观察到C中溶液
您最近一年使用:0次
2019-04-19更新
|
261次组卷
|
2卷引用:沪科版化学拓展性课程1《原子结构与元素周期律》测试题
名校
解题方法
8 . 现有下列3个氧化还原反应:
① ;
;
②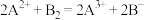 ;
;
③ ,
,
根据上述反应,判断下列结论中正确的是
①
 ;
;②
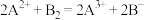 ;
;③
 ,
,根据上述反应,判断下列结论中正确的是
A.要除去含有 、 、 和 和 混合溶液中的 混合溶液中的 ,而不氧化 ,而不氧化 和 和 ,应加入 ,应加入 |
B.氧化性强弱顺序为: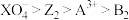 |
C. 是 是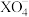 的氧化产物, 的氧化产物, 是B-的还原产物 是B-的还原产物 |
D.在溶液中不可能发生反应: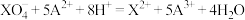 |
您最近一年使用:0次
2022-03-18更新
|
1350次组卷
|
19卷引用:沪科版高中化学拓展课程第4章《离子互换反应和氧化还原反应》检测题3
沪科版高中化学拓展课程第4章《离子互换反应和氧化还原反应》检测题3(已下线)第一章《物质及其变化》能力提升单元检测-【帮课堂】2022-2023学年高一化学必修第一册精品讲义(人教版2019)【校级联考】安徽省皖中名校联盟2019届高三上学期10月联考化学试题【全国百强校】黑龙江省大庆市铁人中学2018-2019学年高一上学期期中考试化学试题安徽省阜阳市第三中学2018-2019学年高一上学期小期末考试(期末模拟)化学试题【全国百强校】云南省昭通市水富市云天化中学2018-2019学年高二上学期期末考试化学试题【全国百强校】内蒙古自治区乌兰察布市集宁区第一中学2018-2019学年高一上学期期末考试化学试题黑龙江省哈尔滨师范大学附属中学2019-2020学年高一上学期期中考试化学试题辽宁省沈阳市第二十中学2019-2020学年高一上学期第一次月考化学试题(已下线)【浙江新东方】29(已下线)【浙江新东方】38浙江省宁波中学2021-2022学年高一上学期期中考试化学试题山西省晋城市第一中学(丹河校区)2022-2023学年高一上学期第二次调研考试化学试题重庆市杨家坪中学2022-2023学年高一上学期第一次月考化学试题(已下线)【2023】【高一下】【其他】【杭二中-期中复习卷】【高中化学】【邵威宏收集】黑龙江省七台河市勃利县高级中学2022-2023学年高二下学期期末考试化学试题河北省张家口市宣化第一中学2022-2023学年高一上学期12月月考化学试题黑龙江省大庆铁人中学2023-2024学年高一上学期10月月考化学试题安徽省合肥市第一中学2023-2024学年高一上学期期末考试化学试题
13-14高三·上海·阶段练习
9 . 某电镀铜厂有两种废水,分别含有CN-和Cr2O72-等有毒离子,拟用NaClO和Na2S2O3按照下列流程进行处理。

完成下列填空:
(1)HCN有剧毒,电子式是___ ,其分子属于___ (填“极性”、“非极性”)分子。
(2)选用最详尽描述核外电子运动状态的方式,来表示氮原子的最外层电子:___ ,氮原子核外有___ 种能量不同的电子。
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是___ 。
a.相同条件下水溶液的酸性:HClO3>H2SO3
b.稳定性:HCl>H2S
c.相同条件下水溶液的pH:Na2S>NaCl
d.还原性:S2->Cl-
(4)写出流程②的离子方程式:___ 。
(5)反应②中,每消耗1.5mol Cr2O72-转移电子的数目为___ 个。
(6)取少量待检水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,用平衡移动原理解释产生该现象的原因___ 。

完成下列填空:
(1)HCN有剧毒,电子式是
(2)选用最详尽描述核外电子运动状态的方式,来表示氮原子的最外层电子:
(3)下列事实能说明氯与硫两元素非金属性相对强弱的是
a.相同条件下水溶液的酸性:HClO3>H2SO3
b.稳定性:HCl>H2S
c.相同条件下水溶液的pH:Na2S>NaCl
d.还原性:S2->Cl-
(4)写出流程②的离子方程式:
(5)反应②中,每消耗1.5mol Cr2O72-转移电子的数目为
(6)取少量待检水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,用平衡移动原理解释产生该现象的原因
您最近一年使用:0次
名校
10 . 过氧化钙(CaO2·8H2O)是一种在水产养殖中广泛使用的供氧剂。
水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I−完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
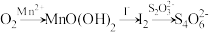
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:_____________ 。
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L−1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(以mg·L−1表示),写出计算过程_______ 。
水中溶解氧的测定方法如下:向一定量水样中加入适量MnSO4和碱性KI溶液,生成MnO(OH)2沉淀,密封静置;加入适量稀H2SO4,待MnO(OH)2与I−完全反应生成Mn2+和I2后,以淀粉作指示剂,用Na2S2O3标准溶液滴定至终点,测定过程中物质的转化关系如下:
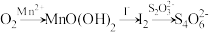
①写出O2将Mn2+氧化成MnO(OH)2的离子方程式:
②取加过一定量CaO2·8H2O的池塘水样100.00 mL,按上述方法测定水中溶解氧量,消耗0.01000 mol·L−1 Na2S2O3标准溶液13.50 mL。计算该水样中的溶解氧(以mg·L−1表示),写出计算过程
您最近一年使用:0次
2020-04-15更新
|
126次组卷
|
8卷引用:沪科版化学拓展性课程4《离子互换反应和氧化还原反应》测试题
沪科版化学拓展性课程4《离子互换反应和氧化还原反应》测试题河北省定州中学2018届高三(承智班)上学期第一次调研化学试题(已下线)2019高考备考一轮复习精品资料 第二章 化学物质及其变化第4讲 守恒思想在化学中的应用——守恒法解题技巧【教学案】2018-2019学年鲁科版高一化学必修一1.3化学中常用的物理量-物质的量练习题(已下线)2019高考备考二轮复习精品资料-专题2 化学常用计量(教学案)【全国百强校】福建省莆田市仙游县第一中学2018-2019学年高一下学期第一次月考(3月)化学试题安徽省萧城一中2020届高三第一次月考化学试题(已下线)专题十三 综合题中的滴定问题(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训



