名校
解题方法
1 . 某废水中含有 和
和 ,
, 浓度远大于
浓度远大于 。为研究废水中
。为研究废水中 处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。
处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。
平衡Ⅱ:
下列说法不正确的是
 和
和 ,
, 浓度远大于
浓度远大于 。为研究废水中
。为研究废水中 处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。
处理的最佳pH,取5份等量的废水,分别用30%的NaOH溶液调节pH至8.5、9、9.5、10、11,静置后,分析上层清液中铜元素的含量,实验结果如下图所示。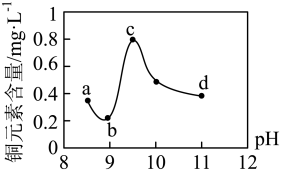

平衡Ⅱ:

下列说法不正确的是
A.废水中 处理的最佳pH约为9 处理的最佳pH约为9 |
B.b~c段:随pH升高,上层清液中 的浓度上升,平衡I正向移动 的浓度上升,平衡I正向移动 |
C.c~d段:随pH升高,上层清液中 和 和 的浓度均下降 的浓度均下降 |
| D.推测d点以后,随pH升高,上层清液中铜元素的含量可能上升 |
您最近一年使用:0次
名校
2 . 探究 与
与 对
对 分解的催化效率。
分解的催化效率。
(1)甲同学进行了如下的实验。
在两支试管中分别加入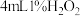 溶液,然后各滴加5滴
溶液,然后各滴加5滴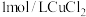 溶液和5滴
溶液和5滴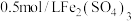 溶液。观察到两支试管中均只有极微量的气泡。
溶液。观察到两支试管中均只有极微量的气泡。
甲由此得出了结论: 与
与 对
对 分解的催化效率相似,且均不高。
分解的催化效率相似,且均不高。
乙同学认为甲的方案不太合理,做了如下的改进:
①乙认为甲方案不合理的理由有___________ (填选项符号)。
a. 溶液和
溶液和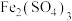 溶液的浓度不同
溶液的浓度不同
b.两种催化剂溶液中的阴离子不同
c. 溶液浓度过低
溶液浓度过低
②两支试管中产生气泡的速率先加快后又减慢的合理解释是:___________ 。
③根据实验结果,乙得出是结论是:___________ 。
(2)研究试管2中出现“溶液变为棕褐色,最后变为浅黄色”的原因。
乙同学查阅文献,发现是因为 会与
会与 发生如下反应生成棕褐色的
发生如下反应生成棕褐色的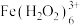 :
: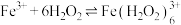 。结合化学反应原理解释“溶液颜色先变为棕褐色再变为黄色”的原因:
。结合化学反应原理解释“溶液颜色先变为棕褐色再变为黄色”的原因:___________ 。
(3)乙同学在翻阅资料时还发现 与
与 能发生反应生成无色的
能发生反应生成无色的

他又做了如下的实验:
在一支试管中加入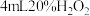 溶液,滴加几滴
溶液,滴加几滴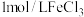 溶液,待出现大量气泡时,立即加入
溶液,待出现大量气泡时,立即加入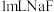 溶液,观察到溶液颜色立即由棕褐色褪为无色,且气泡立刻消失。
溶液,观察到溶液颜色立即由棕褐色褪为无色,且气泡立刻消失。
由此判断,下列说法正确的是___________ (填选项符号)。
a. 对
对 的分解几乎无催化作用
的分解几乎无催化作用
b.温度相同时,含相同浓度的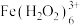 和
和 的溶液中
的溶液中 浓度后者的大
浓度后者的大
c.颜色由棕褐色褪为无色时反应的离子方程式是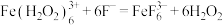
 与
与 对
对 分解的催化效率。
分解的催化效率。(1)甲同学进行了如下的实验。
在两支试管中分别加入
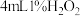 溶液,然后各滴加5滴
溶液,然后各滴加5滴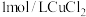 溶液和5滴
溶液和5滴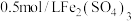 溶液。观察到两支试管中均只有极微量的气泡。
溶液。观察到两支试管中均只有极微量的气泡。甲由此得出了结论:
 与
与 对
对 分解的催化效率相似,且均不高。
分解的催化效率相似,且均不高。乙同学认为甲的方案不太合理,做了如下的改进:
| 试管1 | 试管2 | |
| 实验 | 在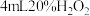 溶液中滴加5滴 溶液中滴加5滴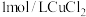 溶液 溶液 | 在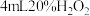 溶液中滴加5滴 溶液中滴加5滴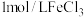 溶液 溶液 |
| 现象 | ⅰ.加入溶液后,产生气泡 ⅱ.生成气泡速率先加快后又减慢 ⅲ.整个过程中溶液始终保持浅蓝色。 ⅳ.且整个过程中产生气泡的速率低于试管2中。 | ⅰ.加入溶液后,试管内液体立即变为棕褐色,并产生气泡 ⅱ.生成气泡速率先加快后又减慢。 ⅲ.溶液棕褐色逐渐变浅,反应结束时变为浅黄色。 |
a.
 溶液和
溶液和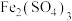 溶液的浓度不同
溶液的浓度不同b.两种催化剂溶液中的阴离子不同
c.
 溶液浓度过低
溶液浓度过低②两支试管中产生气泡的速率先加快后又减慢的合理解释是:
③根据实验结果,乙得出是结论是:
(2)研究试管2中出现“溶液变为棕褐色,最后变为浅黄色”的原因。
乙同学查阅文献,发现是因为
 会与
会与 发生如下反应生成棕褐色的
发生如下反应生成棕褐色的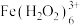 :
: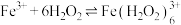 。结合化学反应原理解释“溶液颜色先变为棕褐色再变为黄色”的原因:
。结合化学反应原理解释“溶液颜色先变为棕褐色再变为黄色”的原因:(3)乙同学在翻阅资料时还发现
 与
与 能发生反应生成无色的
能发生反应生成无色的

他又做了如下的实验:
在一支试管中加入
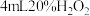 溶液,滴加几滴
溶液,滴加几滴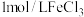 溶液,待出现大量气泡时,立即加入
溶液,待出现大量气泡时,立即加入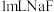 溶液,观察到溶液颜色立即由棕褐色褪为无色,且气泡立刻消失。
溶液,观察到溶液颜色立即由棕褐色褪为无色,且气泡立刻消失。由此判断,下列说法正确的是
a.
 对
对 的分解几乎无催化作用
的分解几乎无催化作用b.温度相同时,含相同浓度的
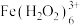 和
和 的溶液中
的溶液中 浓度后者的大
浓度后者的大c.颜色由棕褐色褪为无色时反应的离子方程式是
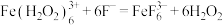
您最近一年使用:0次
名校
3 . 合成氨的发展体现了化学科学与技术的不断进步。
(1)1898年,化学家用氮气、碳化钙( )与水蒸气反应制备氨:
)与水蒸气反应制备氨:
ⅰ.碳化钙和氮气在1000℃的高温下产生氰氨化钙( );
);
ⅱ.氰氨化钙与水蒸气反应生成氨气。写出反应ⅱ的化学方程式:___________ 。
(2)20世纪初,以 和
和 为原料的工业合成氨方法研制成功。其反应为:
为原料的工业合成氨方法研制成功。其反应为:


①写出氮气的电子式___________ 。
② 的化学性质稳定,即使在高温、高压下,
的化学性质稳定,即使在高温、高压下, 和
和 的化合反应仍然进行得十分缓慢。从结构角度解释原因:
的化合反应仍然进行得十分缓慢。从结构角度解释原因:___________ 。
③压强对合成氨有较大影响。下图为不同压强下,以物质的量分数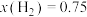 、
、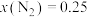 进料(组成1),反应达平衡时
进料(组成1),反应达平衡时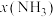 与温度的计算结果。
与温度的计算结果。
___________  (填“>”或“<”),简述理由:
(填“>”或“<”),简述理由:___________ 。
ⅱ.在 、
、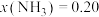 时,氮气的转化率为
时,氮气的转化率为___________ 。
(3)我国科学家研制出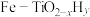 双催化剂,通过光辐射产生温差(如体系温度为495℃时,纳米Fe的温度为547℃,而
双催化剂,通过光辐射产生温差(如体系温度为495℃时,纳米Fe的温度为547℃,而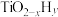 的温度为415℃),解决了温度对合成氨工业反应速率和平衡转化率影响矛盾的问题,其催化合成氨机理如图所示。
的温度为415℃),解决了温度对合成氨工业反应速率和平衡转化率影响矛盾的问题,其催化合成氨机理如图所示。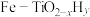 双催化剂双温催化合成氨具备优势的原因是
双催化剂双温催化合成氨具备优势的原因是___________ 。
(1)1898年,化学家用氮气、碳化钙(
 )与水蒸气反应制备氨:
)与水蒸气反应制备氨:ⅰ.碳化钙和氮气在1000℃的高温下产生氰氨化钙(
 );
);ⅱ.氰氨化钙与水蒸气反应生成氨气。写出反应ⅱ的化学方程式:
(2)20世纪初,以
 和
和 为原料的工业合成氨方法研制成功。其反应为:
为原料的工业合成氨方法研制成功。其反应为:

①写出氮气的电子式
②
 的化学性质稳定,即使在高温、高压下,
的化学性质稳定,即使在高温、高压下, 和
和 的化合反应仍然进行得十分缓慢。从结构角度解释原因:
的化合反应仍然进行得十分缓慢。从结构角度解释原因:③压强对合成氨有较大影响。下图为不同压强下,以物质的量分数
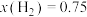 、
、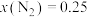 进料(组成1),反应达平衡时
进料(组成1),反应达平衡时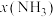 与温度的计算结果。
与温度的计算结果。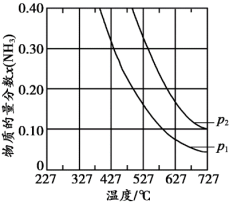

 (填“>”或“<”),简述理由:
(填“>”或“<”),简述理由:ⅱ.在
 、
、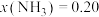 时,氮气的转化率为
时,氮气的转化率为(3)我国科学家研制出
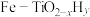 双催化剂,通过光辐射产生温差(如体系温度为495℃时,纳米Fe的温度为547℃,而
双催化剂,通过光辐射产生温差(如体系温度为495℃时,纳米Fe的温度为547℃,而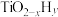 的温度为415℃),解决了温度对合成氨工业反应速率和平衡转化率影响矛盾的问题,其催化合成氨机理如图所示。
的温度为415℃),解决了温度对合成氨工业反应速率和平衡转化率影响矛盾的问题,其催化合成氨机理如图所示。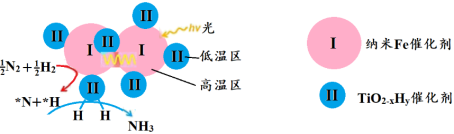
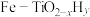 双催化剂双温催化合成氨具备优势的原因是
双催化剂双温催化合成氨具备优势的原因是
您最近一年使用:0次
名校
解题方法
4 . 氨气在工农业生产中有重要应用。
(1)①写出实验室制氨气的化学方程式:___________ 。
② 的稳定性比
的稳定性比
___________ (填写“强”或“弱”)。
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。___________ 。
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是___________ (写化学式,一种即可)。
③ 液滴中先出现白色沉淀,写出离子反应方程式
液滴中先出现白色沉淀,写出离子反应方程式___________ 。白色沉淀迅速变成灰绿色沉淀,过一段时间后变成红褐色,写出化学反应方程式___________ 。
(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸( ),反应的化学方程式为
),反应的化学方程式为___________ ,若反应中有0.3mol电子发生转移时,生成亚硝酸的质量为___________ g(小数点后保留两位有效数字)。
(4) 可以转化为其他含氮物质,下面为
可以转化为其他含氮物质,下面为 转化为
转化为 的流程。
的流程。
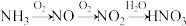
①写出 与
与 反应转化为NO的化学方程式
反应转化为NO的化学方程式___________ 。
② 转化为
转化为 的整个过程中,为提高氮原子的利用率,可采取的措施是
的整个过程中,为提高氮原子的利用率,可采取的措施是___________ 。
(1)①写出实验室制氨气的化学方程式:
②
 的稳定性比
的稳定性比
(2)如下图所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象。
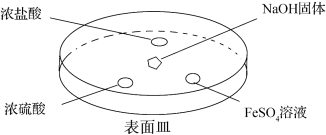
②浓硫酸液滴上方没有明显现象,一段时间后浓硫酸的液滴中有白色固体,该固体可能是
③
 液滴中先出现白色沉淀,写出离子反应方程式
液滴中先出现白色沉淀,写出离子反应方程式(3)在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(
 ),反应的化学方程式为
),反应的化学方程式为(4)
 可以转化为其他含氮物质,下面为
可以转化为其他含氮物质,下面为 转化为
转化为 的流程。
的流程。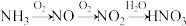
①写出
 与
与 反应转化为NO的化学方程式
反应转化为NO的化学方程式②
 转化为
转化为 的整个过程中,为提高氮原子的利用率,可采取的措施是
的整个过程中,为提高氮原子的利用率,可采取的措施是
您最近一年使用:0次
名校
解题方法
5 . 关于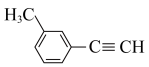 的说法正确的是
的说法正确的是
| A.能使酸性高锰酸钾溶液和溴水褪色,且反应原理相同 |
| B.分子中共平面的原子数目最多为14 |
| C.分子中有3种杂化轨道类型的碳原子 |
| D.与Cl2发生取代反应生成4种一氯代物 |
您最近一年使用:0次
6 . 用充有 的烧瓶进行“喷泉实验”,装置及现象如下图。下列关于该实验的分析正确的是
的烧瓶进行“喷泉实验”,装置及现象如下图。下列关于该实验的分析正确的是
 的烧瓶进行“喷泉实验”,装置及现象如下图。下列关于该实验的分析正确的是
的烧瓶进行“喷泉实验”,装置及现象如下图。下列关于该实验的分析正确的是
| A.加热红色溶液可观察到红色变浅或褪去 |
B.无色溶液变红证明 极易溶于水 极易溶于水 |
C.溶液变红的原因可用如下式子解释 |
D.产生“喷泉”证明 与 与 发生了反应 发生了反应 |
您最近一年使用:0次
名校
7 . 下列说法不正确的是
| A.沸点:对羟基苯甲醛>邻羟基苯甲醛 |
| B.键角:NH3>H2O |
| C.熔点:晶体硅>碳化硅>金刚石 |
| D.酸性:CCl3COOH>CHCl2COOH > CH3COOH |
您最近一年使用:0次
名校
解题方法
8 . 2011年中国研制的第四代隐形战机歼-20在成都首次公开试飞成功。隐形战机的核心材料是金属钛,我国探明储量世界第一、下列有关22Ti的说法不正确的是
| A.钛的原子序数为22 |
| B.钛位于元素周期表第四周期第IVB族 |
| C.基态钛原子核外电子排布式为1s22s22p63s23p63d4 |
| D.钛是d区元素 |
您最近一年使用:0次
名校
9 . A、B、C、D、E为常见的主族元素,根据下表信息回答问题。
(1)写出元素A的原子结构示意图___________ 。
(2)A、B最高价氧化物对应水化物的碱性强弱:___________ >___________ (填化学式),从原子结构角度解释原因___________ 。
(3)写出A、B最高价氧化物对应水化物二者反应的离子方程式________________ 。
(4)用电子式表示C和D形成化合物的过程:_______________ 。
(5)元素E在周期表中的位置___________ ,关于元素E及其化合物的推断中,正确的是___________ 。
a.E与D的最低负化合价相同 b.E的单质可与A和D形成的化合物的水溶液发生置换反应
c.最高价氧化物对应水化物的酸性:E>D d.氢化物稳定性:E<D
(6)D和E形成的化合物①具有氧化性,其中体现氧化性的元素是(写元素符号)___________ ,原因是________________ 。
(7)元素M与A同主族,比A多2个电子层,M与氧以2:1比例形成的化合物②的物质类别为___________ ,任意写出一个能体现②的类别通性的反应方程式_____________ 。
(8)第四周期ⅥA族的元素硒 是一种人体必需的元素,关于硒元素及其化合物的有关说法正确的是(选填序号)
是一种人体必需的元素,关于硒元素及其化合物的有关说法正确的是(选填序号)___________ 。
a.硒原子的半径比硫原子的大 b. 的稳定性比HCl的强
的稳定性比HCl的强
c. 能与NaOH溶液反应 d.
能与NaOH溶液反应 d. 可以使酸性高锰酸钾溶液褪色
可以使酸性高锰酸钾溶液褪色
| 元素 | 元素性质/原子结构信息 |
| A | 短周期元素原子半径最大(稀有气体不参与比较) |
| B | +3价阳离子的核外电子排布与氖原子相同 |
| C | 原子核外M电子层与K电子层的电子数相等 |
| D | 与A同周期,化合价有-1、+7等 |
| E | 原子结构示意图: |
(1)写出元素A的原子结构示意图
(2)A、B最高价氧化物对应水化物的碱性强弱:
(3)写出A、B最高价氧化物对应水化物二者反应的离子方程式
(4)用电子式表示C和D形成化合物的过程:
(5)元素E在周期表中的位置
a.E与D的最低负化合价相同 b.E的单质可与A和D形成的化合物的水溶液发生置换反应
c.最高价氧化物对应水化物的酸性:E>D d.氢化物稳定性:E<D
(6)D和E形成的化合物①具有氧化性,其中体现氧化性的元素是(写元素符号)
(7)元素M与A同主族,比A多2个电子层,M与氧以2:1比例形成的化合物②的物质类别为
(8)第四周期ⅥA族的元素硒
 是一种人体必需的元素,关于硒元素及其化合物的有关说法正确的是(选填序号)
是一种人体必需的元素,关于硒元素及其化合物的有关说法正确的是(选填序号)a.硒原子的半径比硫原子的大 b.
 的稳定性比HCl的强
的稳定性比HCl的强c.
 能与NaOH溶液反应 d.
能与NaOH溶液反应 d. 可以使酸性高锰酸钾溶液褪色
可以使酸性高锰酸钾溶液褪色
您最近一年使用:0次
名校
10 . 用以下三种途径来制取相同质量的硝酸铜:①铜与浓硝酸反应;②铜与稀硝酸反应;③铜与氧气反应生成CuO,CuO再与稀硝酸反应。下列有关叙述不正确的是
| A.①和②电子转移数之比为1∶3 | B.三种途径所消耗的铜的质量相等 |
| C.所消耗的硝酸的量:①>②>③ | D.对环境造成的危害,③最小 |
您最近一年使用:0次