名校
1 . 在硫酸工业中,使 氧化为
氧化为 的反应为
的反应为
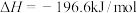 。下表列出了恒容密闭容器中,在不同温度和压强下,反应达到平衡时
。下表列出了恒容密闭容器中,在不同温度和压强下,反应达到平衡时 的转化率。下列说法错误的是
的转化率。下列说法错误的是
 氧化为
氧化为 的反应为
的反应为
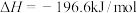 。下表列出了恒容密闭容器中,在不同温度和压强下,反应达到平衡时
。下表列出了恒容密闭容器中,在不同温度和压强下,反应达到平衡时 的转化率。下列说法错误的是
的转化率。下列说法错误的是平衡时 | |||||
0.1MPa | 0.5MPa | 1MPa | 5MPa | 10MPa | |
450℃ | 97.5 | 98.9 | 99.2 | 99.6 | 99.7 |
500℃ | 85.6 | 92.9 | 94.9 | 97.7 | 98.3 |
A.通入适当过量的氧气,既有利于提高反应速率,又有利于增大 的转化率 的转化率 |
B.尾气中的 需要回收循环利用,防止污染环境并提高原料的利用率 需要回收循环利用,防止污染环境并提高原料的利用率 |
| C.在实际生产中,应选择的条件是450℃,10MPa |
| D.在实际生产中,选定的温度为400-500℃,主要原因是考虑催化剂的活性最佳 |
您最近一年使用:0次
2024-02-08更新
|
132次组卷
|
2卷引用:辽宁省锦州市2023-2024学年高二上学期1月期末化学试题
2 . 已知: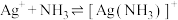
 ,
,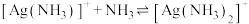
 。
。 、
、 、
、 的分布分数
的分布分数 与
与 关系如图所示,浓度单位为mol/L。{例如:分布分数
关系如图所示,浓度单位为mol/L。{例如:分布分数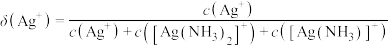 },下列说法正确的是
},下列说法正确的是

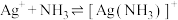
 ,
,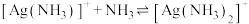
 。
。 、
、 、
、 的分布分数
的分布分数 与
与 关系如图所示,浓度单位为mol/L。{例如:分布分数
关系如图所示,浓度单位为mol/L。{例如:分布分数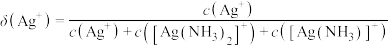 },下列说法正确的是
},下列说法正确的是
A.曲线c代表 的分布分数 的分布分数 |
B. 平衡常数 平衡常数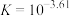 |
C.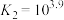 |
D.当 时, 时,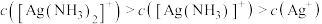 |
您最近一年使用:0次
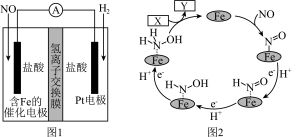
3 . 盐酸羟胺( )是一种常见的还原剂和显像剂,其化学性质类似
)是一种常见的还原剂和显像剂,其化学性质类似 。工业上采用图1装置进行制备,其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积的变化,下列说法正确的是
。工业上采用图1装置进行制备,其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积的变化,下列说法正确的是
 )是一种常见的还原剂和显像剂,其化学性质类似
)是一种常见的还原剂和显像剂,其化学性质类似 。工业上采用图1装置进行制备,其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积的变化,下列说法正确的是
。工业上采用图1装置进行制备,其电池装置中含Fe的催化电极反应机理如图2所示。不考虑溶液体积的变化,下列说法正确的是
| A.电子从含Fe的催化电极流出沿导线流入Pt电极 |
B.图2中,X为 和 和 ,Y为 ,Y为 |
| C.电池工作一段时间后,正极区溶液的pH减小 |
D.理论上,当有标准状况下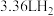 参与反应时,左室溶液质量增加3.3g 参与反应时,左室溶液质量增加3.3g |
您最近一年使用:0次
4 . 下列图像表达错误的是
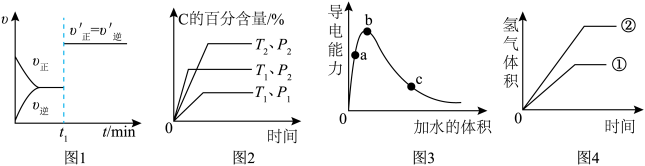

A.图1:对于反应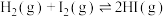 , , 时刻可能改变了压强或使用了催化剂 时刻可能改变了压强或使用了催化剂 |
B.图2:对于反应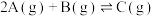  ,从图中可知温度 ,从图中可知温度 ,压强 ,压强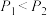 |
C.图3:将一定量冰醋酸加水稀释过程, 的电离程度: 的电离程度: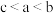 |
| D.图4:足量锌粉与pH、体积均相同的醋酸和盐酸溶液反应,②为与醋酸反应曲线 |
您最近一年使用:0次
5 . 定量分析是根据特定的化学反应及其计量关系对物质进行分析的一种重要方法。
回答下列问题:
(1)酸、碱在水溶液中的离子反应与平衡的分析
室温下,用0.1mol/LNaOH溶液分别滴定体积和浓度均为20.0mL0.1mol/L的盐酸和醋酸溶液,得到pH随加入NaOH溶液体积变化的滴定曲线如图所示。

①表示滴定盐酸过程的曲线是__________ (填“Ⅰ”或“Ⅱ”)。
②a点溶液中,离子浓度大小关系为__________ (用离子符号表示)。
③b点溶液中,由水电离出的
__________ mol/L。
④当加入20mLNaOH溶液时,
__________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
⑤比较溶液中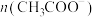 ,c点
,c点__________ b点(填“>”、“<”或“=”)。
(2)测定某些物质的含量
某实验小组设计了如下实验方案测定某血清样本中 的含量:
的含量:

滴定反应中氧化产物为 ,还原产物为
,还原产物为 ,滴定终点时
,滴定终点时 溶液的用量为12.00mL。
溶液的用量为12.00mL。
①滴定实验中,将 标准溶液装入滴定管的正确操作顺序为
标准溶液装入滴定管的正确操作顺序为__________ (填标号)。
a.装入 标准溶液至0刻度以上;b.检查滴定管是否漏液;c.排尽尖嘴部分气泡;d.用
标准溶液至0刻度以上;b.检查滴定管是否漏液;c.排尽尖嘴部分气泡;d.用 标准溶液润洗滴定管2~3次;e.用蒸馏水清洗2~3次;f.将液面调节至0刻度或以下。
标准溶液润洗滴定管2~3次;e.用蒸馏水清洗2~3次;f.将液面调节至0刻度或以下。
②判定滴定终点的现象为__________ 。
③血清样本中 的浓度为
的浓度为__________ mol/L。
回答下列问题:
(1)酸、碱在水溶液中的离子反应与平衡的分析
室温下,用0.1mol/LNaOH溶液分别滴定体积和浓度均为20.0mL0.1mol/L的盐酸和醋酸溶液,得到pH随加入NaOH溶液体积变化的滴定曲线如图所示。

①表示滴定盐酸过程的曲线是
②a点溶液中,离子浓度大小关系为
③b点溶液中,由水电离出的

④当加入20mLNaOH溶液时,

 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。⑤比较溶液中
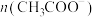 ,c点
,c点(2)测定某些物质的含量
某实验小组设计了如下实验方案测定某血清样本中
 的含量:
的含量:
滴定反应中氧化产物为
 ,还原产物为
,还原产物为 ,滴定终点时
,滴定终点时 溶液的用量为12.00mL。
溶液的用量为12.00mL。①滴定实验中,将
 标准溶液装入滴定管的正确操作顺序为
标准溶液装入滴定管的正确操作顺序为a.装入
 标准溶液至0刻度以上;b.检查滴定管是否漏液;c.排尽尖嘴部分气泡;d.用
标准溶液至0刻度以上;b.检查滴定管是否漏液;c.排尽尖嘴部分气泡;d.用 标准溶液润洗滴定管2~3次;e.用蒸馏水清洗2~3次;f.将液面调节至0刻度或以下。
标准溶液润洗滴定管2~3次;e.用蒸馏水清洗2~3次;f.将液面调节至0刻度或以下。②判定滴定终点的现象为
③血清样本中
 的浓度为
的浓度为
您最近一年使用:0次
解题方法
6 . 常温下,取两份10mL0.05mol/L的NaHA溶液,一份滴加0.05mol/L的盐酸,另一份滴1加0.05mol/LNaOH溶液,溶液的pH随加入酸(或碱)体积的变化如图(忽略溶液混合后的体积变化)。下列说法错误的是
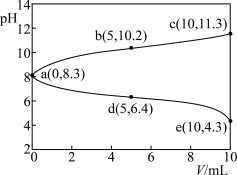

A.由a点可知:NaHA溶液中 的水解程度大于电离程度 的水解程度大于电离程度 |
B.c点溶液中,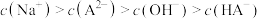 |
C. 过程中: 过程中: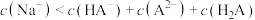 |
D.e点溶液中,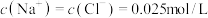 |
您最近一年使用:0次
7 . 下列关于原子或分子的结构与性质的说法错误的是
①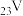 的电子排布式
的电子排布式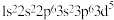 违反了洪特规则
违反了洪特规则
②基态氮原子有3种空间运动状态5种能量不同的电子
③ 、
、 、
、 、
、 熔、沸点随相对分子质量的增大而升高
熔、沸点随相对分子质量的增大而升高
④非极性分子可以含有极性键,但分子的正负电荷中心必须重合
⑤中心原子是 杂化的,其分子的空间结构一定为平面三角形
杂化的,其分子的空间结构一定为平面三角形
⑥邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
①
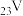 的电子排布式
的电子排布式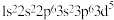 违反了洪特规则
违反了洪特规则②基态氮原子有3种空间运动状态5种能量不同的电子
③
 、
、 、
、 、
、 熔、沸点随相对分子质量的增大而升高
熔、沸点随相对分子质量的增大而升高④非极性分子可以含有极性键,但分子的正负电荷中心必须重合
⑤中心原子是
 杂化的,其分子的空间结构一定为平面三角形
杂化的,其分子的空间结构一定为平面三角形⑥邻羟基苯甲醛的沸点低于对羟基苯甲醛的沸点
| A.①②⑤ | B.①④⑤ | C.②③⑥ | D.③④⑥ |
您最近一年使用:0次
8 . 根据下列实验操作和实验现象,能够得出相应结论的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向 溶液中加入少量铁粉 溶液中加入少量铁粉 | 溶液红色变浅 | 减小 ,使反应 ,使反应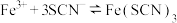 平衡逆向移动 平衡逆向移动 |
B | 将金属M片和Cu片与稀硫酸构成原电池 | Cu片上产生气泡,M片不断变小 | 金属活动性: |
C | 常温下,用pH计分别测定等物质的量浓度的 与 与 溶液的pH 溶液的pH |
| 证明非金属性: |
D | 向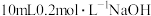 溶液中滴加2滴 溶液中滴加2滴 的 的 溶液,再滴加2滴 溶液,再滴加2滴 的 的 溶液 溶液 | 先生成白色沉淀,后生成红褐色沉淀 | 相同温度 : : |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
9 . 一种染料敏化太阳能电池如图,其成本便宜且对环境无污染。敏化染料(S)吸附在 纳米空心球表面。光照时:
纳米空心球表面。光照时: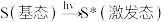 ,
,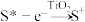 。下列说法正确的是
。下列说法正确的是

 纳米空心球表面。光照时:
纳米空心球表面。光照时: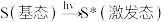 ,
,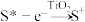 。下列说法正确的是
。下列说法正确的是
A.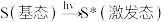 需要释放能量 需要释放能量 |
B.N极的电极反应式为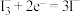 |
C.敏化染料还原过程为 |
| D.该电池工作一段时间后需要补充电解质 |
您最近一年使用:0次
10 . 短周期元素X、Y、Z、W的原子序数依次增大,基态Y原子有3个未成对电子,基态Z原子的价电子数等于其能层数,四种元素可形成化合物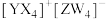 。下列说法错误的是
。下列说法错误的是
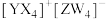 。下列说法错误的是
。下列说法错误的是| A.X和Y可形成含有非极性共价键的化合物 |
| B.电负性:Y>Z |
| C.同周期第一电离能处在Z和W之间的元素有4种 |
| D.阴阳离子中Y和Z的杂化类型不同 |
您最近一年使用:0次