1 . 锂离子电池具有质量小、体积小、储存和输出能量大等特点,是各种便携式电子设备的常用电池。一种可充电钴酸锂电池的工作原理如图所示。下列叙述不正确 的是


A.该电池放电过程中 经过隔膜向 经过隔膜向 电极移动 电极移动 |
B.放电过程中 电极反应: 电极反应: |
| C.该电池负极为石墨,正极为钴酸锂,组装后即可放电使用 |
| D.拆解废电池前先进行放电处理可保证安全且利于回收锂 |
您最近一年使用:0次
2 . 某小组做如下实验:
实验①:向含 的溶液中滴加
的溶液中滴加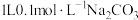 溶液并充分搅拌。
溶液并充分搅拌。
实验②:向 固体中加入
固体中加入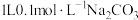 溶液充分搅拌浸泡。
溶液充分搅拌浸泡。
[已知:常温下,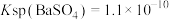 ,
, ,
, 的电离平衡常数:
的电离平衡常数: ,
, ,溶液混合后体积变化忽略不计],下列说法
,溶液混合后体积变化忽略不计],下列说法不正确 的是
实验①:向含
 的溶液中滴加
的溶液中滴加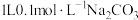 溶液并充分搅拌。
溶液并充分搅拌。实验②:向
 固体中加入
固体中加入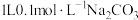 溶液充分搅拌浸泡。
溶液充分搅拌浸泡。[已知:常温下,
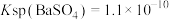 ,
, ,
, 的电离平衡常数:
的电离平衡常数: ,
, ,溶液混合后体积变化忽略不计],下列说法
,溶液混合后体积变化忽略不计],下列说法A.实验①混合后的溶液中, |
B.实验①混合后的溶液中 |
C.实验②涉及反应  |
D.实验②中再加入 溶液,可将 溶液,可将 完全转化为 完全转化为 |
您最近一年使用:0次
解题方法
3 . 下列有关实验操作的叙述正确的是
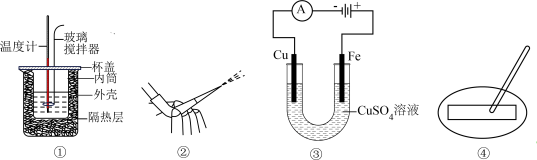

A.图①中和热测定,宜将 稀溶液一次快速加入稀盐酸中 稀溶液一次快速加入稀盐酸中 |
B.图②操作可排出盛有 溶液滴定管尖嘴内的气泡 溶液滴定管尖嘴内的气泡 |
C.图③装置可将 制品表面镀一层铜 制品表面镀一层铜 |
D.图④检测某氯水 ,稳定时读数值为3 ,稳定时读数值为3 |
您最近一年使用:0次
解题方法
4 .  过度排放会引起气候、环境等问题。一定条件下可利用化学反应将其转化为燃料
过度排放会引起气候、环境等问题。一定条件下可利用化学反应将其转化为燃料 。以
。以 和
和 为原料合成
为原料合成 的主要反应如下:
的主要反应如下:
Ⅰ.
 ;
;
Ⅱ.
 ;
;
Ⅲ.

回答下列问题:
(1)
______  。
。
(2)在恒温条件下向恒容的密闭容器中通入 和
和 发生上述反应,若只考虑反应
发生上述反应,若只考虑反应 ,下列
,下列不能 说明反应达到平衡状态的是______ 。
A.
B.容器内的压强不再变化
C.容器内混合气体的密度不再变化
D.混合气体的平均摩尔质量不再变化
E.相同时间内 断裂与
断裂与 断裂比值为1:1
断裂比值为1:1
(3)将 和
和 按1:3通入体积为
按1:3通入体积为 的密闭容器中,假设只发生反应Ⅰ和反应Ⅱ,改变反应温度,分别测得
的密闭容器中,假设只发生反应Ⅰ和反应Ⅱ,改变反应温度,分别测得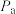 、
、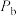 、
、 (单位
(单位 下
下 的平衡转化率(
的平衡转化率( )以及
)以及 时生成
时生成 、
、 选择性(
选择性( )的变化如图甲(选择性为目标产物在总产物中的比率,即
)的变化如图甲(选择性为目标产物在总产物中的比率,即 ;
; )。
)。


①图甲中 、
、 和
和 分别代表代表
分别代表代表 、
、 、
、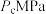 下
下 随温度变化趋势的是曲线,则
随温度变化趋势的是曲线,则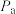 、
、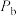 、
、 的从大到小的关系为
的从大到小的关系为______ 。
②随着温度升高, 、
、 和
和 条曲线接近重合的原因是
条曲线接近重合的原因是______ 。
③ 点对应的反应Ⅱ的平衡常数
点对应的反应Ⅱ的平衡常数
______ 。
④分子筛膜反应器可提高反应Ⅱ的平衡转化率,原理如图乙所示。同温同压下,将等物质的量的 和
和 通入无分子筛反应器,测得
通入无分子筛反应器,测得 的平衡转化率为
的平衡转化率为 ;若换成分子筛膜反应器,
;若换成分子筛膜反应器, 的平衡转化率为
的平衡转化率为 ,则相同时间内,上出口和下出口中
,则相同时间内,上出口和下出口中 的物质的量之比为
的物质的量之比为______ 。
(4)为同时提高 的平衡转化率和
的平衡转化率和 的平衡产率,应选择的反应条件为______。
的平衡产率,应选择的反应条件为______。
 过度排放会引起气候、环境等问题。一定条件下可利用化学反应将其转化为燃料
过度排放会引起气候、环境等问题。一定条件下可利用化学反应将其转化为燃料 。以
。以 和
和 为原料合成
为原料合成 的主要反应如下:
的主要反应如下:Ⅰ.

 ;
;Ⅱ.

 ;
;Ⅲ.


回答下列问题:
(1)

 。
。(2)在恒温条件下向恒容的密闭容器中通入
 和
和 发生上述反应,若只考虑反应
发生上述反应,若只考虑反应 ,下列
,下列A.

B.容器内的压强不再变化
C.容器内混合气体的密度不再变化
D.混合气体的平均摩尔质量不再变化
E.相同时间内
 断裂与
断裂与 断裂比值为1:1
断裂比值为1:1(3)将
 和
和 按1:3通入体积为
按1:3通入体积为 的密闭容器中,假设只发生反应Ⅰ和反应Ⅱ,改变反应温度,分别测得
的密闭容器中,假设只发生反应Ⅰ和反应Ⅱ,改变反应温度,分别测得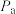 、
、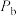 、
、 (单位
(单位 下
下 的平衡转化率(
的平衡转化率( )以及
)以及 时生成
时生成 、
、 选择性(
选择性( )的变化如图甲(选择性为目标产物在总产物中的比率,即
)的变化如图甲(选择性为目标产物在总产物中的比率,即 ;
; )。
)。

①图甲中
 、
、 和
和 分别代表代表
分别代表代表 、
、 、
、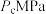 下
下 随温度变化趋势的是曲线,则
随温度变化趋势的是曲线,则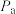 、
、 、
、 的从大到小的关系为
的从大到小的关系为②随着温度升高,
 、
、 和
和 条曲线接近重合的原因是
条曲线接近重合的原因是③
 点对应的反应Ⅱ的平衡常数
点对应的反应Ⅱ的平衡常数
④分子筛膜反应器可提高反应Ⅱ的平衡转化率,原理如图乙所示。同温同压下,将等物质的量的
 和
和 通入无分子筛反应器,测得
通入无分子筛反应器,测得 的平衡转化率为
的平衡转化率为 ;若换成分子筛膜反应器,
;若换成分子筛膜反应器, 的平衡转化率为
的平衡转化率为 ,则相同时间内,上出口和下出口中
,则相同时间内,上出口和下出口中 的物质的量之比为
的物质的量之比为(4)为同时提高
 的平衡转化率和
的平衡转化率和 的平衡产率,应选择的反应条件为______。
的平衡产率,应选择的反应条件为______。| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
您最近一年使用:0次
5 . 电解原理具有广泛应用。氯碱工业是以电解饱和食盐水为基础的工业生产和应用。图1为实验室模拟电解饱和食盐水的装置。图2为离子交换膜法电解饱和食盐水原理示意图。图3为人工肾脏利用间接电化学方法除去代谢产物中的尿素的原理示意图。结合所学知识回答:
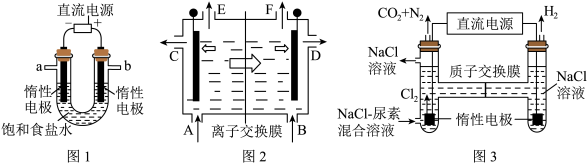
(1)写出用惰性电极电解饱和食盐水的化学方程式:______ 。
(2)写出检验 极产生气体的方法
极产生气体的方法______ 。
(3)图2中采用的离子交换膜为______ (填“阳离子交换膜”“阳离子交换膜”或“质子交换膜”), 应添加的原料为
应添加的原料为______ (填物质名称 )。
(4)图3左侧为电源______ (填“正极”或“负极”),写出该电极区域发生的总反应 方程式______ (尿素的化学式 ),每转化
),每转化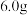 尿素,电解池右侧电极上生成气体的体积为
尿素,电解池右侧电极上生成气体的体积为______ (标准状况)。

(1)写出用惰性电极电解饱和食盐水的化学方程式:
(2)写出检验
 极产生气体的方法
极产生气体的方法(3)图2中采用的离子交换膜为
 应添加的原料为
应添加的原料为(4)图3左侧为电源
 ),每转化
),每转化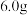 尿素,电解池右侧电极上生成气体的体积为
尿素,电解池右侧电极上生成气体的体积为
您最近一年使用:0次
解题方法
6 . 碘元素是人体必需的微量元素之一,健康成人体内的碘的总量约为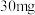 ,摄入过多或摄入不足均会对我们的健康造成危害,加碘盐和海带是我们日常摄入碘的主要来源。某学习小组按如下实验流程将海带进行处理并定量测定其中的碘元素。
,摄入过多或摄入不足均会对我们的健康造成危害,加碘盐和海带是我们日常摄入碘的主要来源。某学习小组按如下实验流程将海带进行处理并定量测定其中的碘元素。
(一)海带处理

(二)碘含量测定
方法一、氧化还原滴定法测定碘含量流程如下:

实验原理: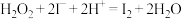
 ;
;
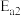 。
。
分析有效实验数据,平均每组实验消耗 溶液体积为
溶液体积为 。
。
方法二、电势滴定法测定碘含量取 的
的 标准溶液装入滴定管,取
标准溶液装入滴定管,取 海带浸取原液至滴定池。测得的电动势(
海带浸取原液至滴定池。测得的电动势( )反映溶液中
)反映溶液中 的变化,部分数据如下表:
的变化,部分数据如下表:
请回答:
(1)海带处理实验中的仪器名称:仪器
______ ,仪器
______ 。
(2)① 溶液应用
溶液应用______ (填“酸式”或“碱式”)滴定管盛装。
②氧化还原滴定过程中,以淀粉为指示剂,判断滴定终点的标准:当最后半滴 溶液滴入时,溶液的蓝色恰好褪去,且半分钟不恢复到蓝色。请写出半滴操作的实验操作方法:
溶液滴入时,溶液的蓝色恰好褪去,且半分钟不恢复到蓝色。请写出半滴操作的实验操作方法:______ 。
③关于滴定操作的下列说法正确的是______ ,
A.滴定的,锥形瓶和滴定管均须用标准液润洗
B.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
C.滴定时,通常用左手控制旋塞(或玻璃珠)滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
D.滴定前滴定管尖嘴无气泡,滴定后尖嘴内有气泡,则测得的浓度比实际小
④滴定过程中多次发现溶液褪色后会恢复蓝色的异常现象。为探究原因,小组多次实验,排除了空气中氧气及过量 溶液的影响。并发现将含
溶液的影响。并发现将含 原液氧化静置12小时后再进行滴定,异常现象消失,结合该实验原理解释导致异常现象的原因
原液氧化静置12小时后再进行滴定,异常现象消失,结合该实验原理解释导致异常现象的原因______ 。
(3)①根据电势滴定法表中数据绘制滴定曲线:______

②该次滴定终点时用去 溶液的体积为
溶液的体积为______  ,计算得海带中碘的百分含量为
,计算得海带中碘的百分含量为______  (保留三位有效数字)。
(保留三位有效数字)。
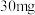 ,摄入过多或摄入不足均会对我们的健康造成危害,加碘盐和海带是我们日常摄入碘的主要来源。某学习小组按如下实验流程将海带进行处理并定量测定其中的碘元素。
,摄入过多或摄入不足均会对我们的健康造成危害,加碘盐和海带是我们日常摄入碘的主要来源。某学习小组按如下实验流程将海带进行处理并定量测定其中的碘元素。(一)海带处理

(二)碘含量测定
方法一、氧化还原滴定法测定碘含量流程如下:

实验原理:
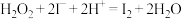
 ;
;
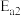 。
。分析有效实验数据,平均每组实验消耗
 溶液体积为
溶液体积为 。
。方法二、电势滴定法测定碘含量取
 的
的 标准溶液装入滴定管,取
标准溶液装入滴定管,取 海带浸取原液至滴定池。测得的电动势(
海带浸取原液至滴定池。测得的电动势( )反映溶液中
)反映溶液中 的变化,部分数据如下表:
的变化,部分数据如下表:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| 175 | 275 | 300 | 325 |
(1)海带处理实验中的仪器名称:仪器


(2)①
 溶液应用
溶液应用②氧化还原滴定过程中,以淀粉为指示剂,判断滴定终点的标准:当最后半滴
 溶液滴入时,溶液的蓝色恰好褪去,且半分钟不恢复到蓝色。请写出半滴操作的实验操作方法:
溶液滴入时,溶液的蓝色恰好褪去,且半分钟不恢复到蓝色。请写出半滴操作的实验操作方法:③关于滴定操作的下列说法正确的是
A.滴定的,锥形瓶和滴定管均须用标准液润洗
B.将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
C.滴定时,通常用左手控制旋塞(或玻璃珠)滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
D.滴定前滴定管尖嘴无气泡,滴定后尖嘴内有气泡,则测得的浓度比实际小
④滴定过程中多次发现溶液褪色后会恢复蓝色的异常现象。为探究原因,小组多次实验,排除了空气中氧气及过量
 溶液的影响。并发现将含
溶液的影响。并发现将含 原液氧化静置12小时后再进行滴定,异常现象消失,结合该实验原理解释导致异常现象的原因
原液氧化静置12小时后再进行滴定,异常现象消失,结合该实验原理解释导致异常现象的原因(3)①根据电势滴定法表中数据绘制滴定曲线:

②该次滴定终点时用去
 溶液的体积为
溶液的体积为 ,计算得海带中碘的百分含量为
,计算得海带中碘的百分含量为 (保留三位有效数字)。
(保留三位有效数字)。
您最近一年使用:0次
7 .  时,下列溶液中微粒浓度关系的说法正确的是
时,下列溶液中微粒浓度关系的说法正确的是
 时,下列溶液中微粒浓度关系的说法正确的是
时,下列溶液中微粒浓度关系的说法正确的是A.向 溶液中滴加 溶液中滴加 溶液至中性,溶液中离子浓度大小关系为: 溶液至中性,溶液中离子浓度大小关系为: |
B.某溶液中只含 、 、 、 、 、 、 四种离子,则可能存在下列关系: 四种离子,则可能存在下列关系: |
C.新制氯水中: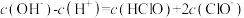 |
D.同浓度条件下,①氨水、② 溶液、③ 溶液、③ 溶液、④ 溶液、④ 溶液, 溶液, 大小关系:②>④>③>① 大小关系:②>④>③>① |
您最近一年使用:0次
8 . 下列操作或应用的主要原理与盐类水解无关 的是
A.利用 溶液制备 溶液制备 |
B.蒸干 溶液得不到纯净的 溶液得不到纯净的 |
C.铵态氮肥与草木灰(含 )不宜混合施用 )不宜混合施用 |
D.在实验室配置 溶液时,常滴加几滴 溶液时,常滴加几滴 溶液 溶液 |
您最近一年使用:0次
9 . 下列实验操作、现象、结论或解释不正确 的是
选项 | 实验损作: | 现象 | 结论或解释 |
A | 向试管中加入 | 加热后溶液变黄绿色,冷却后重新变回蓝色 | 反应 |
B | 向盛有 | 先生成白色沉淀,之后沉淀变为黄色 |
|
C | 向漂白粉溶液中通CO2气体 | 产生白色沉淀 | 因 |
D | 等体积、等 | HX放出的氢气多且反应速率快 | 酸的强弱: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 已知 、
、 、
、 、
、 、
、 是原子序数依次增大的前四周期元素。其中
是原子序数依次增大的前四周期元素。其中 对应的一种核素没有中子,
对应的一种核素没有中子, 的基态原子价层电子中有3个未成对电子,
的基态原子价层电子中有3个未成对电子, 最外层电子数是其内层的3倍,
最外层电子数是其内层的3倍, 的原子序数是
的原子序数是 的两倍,
的两倍, 的基态原子失去三个电子后,价层电子为半充满结构。下列说法正确的是
的基态原子失去三个电子后,价层电子为半充满结构。下列说法正确的是
 、
、 、
、 、
、 、
、 是原子序数依次增大的前四周期元素。其中
是原子序数依次增大的前四周期元素。其中 对应的一种核素没有中子,
对应的一种核素没有中子, 的基态原子价层电子中有3个未成对电子,
的基态原子价层电子中有3个未成对电子, 最外层电子数是其内层的3倍,
最外层电子数是其内层的3倍, 的原子序数是
的原子序数是 的两倍,
的两倍, 的基态原子失去三个电子后,价层电子为半充满结构。下列说法正确的是
的基态原子失去三个电子后,价层电子为半充满结构。下列说法正确的是A. 、 、 气态氢化物的稳定性: 气态氢化物的稳定性: |
B.元素电负性: |
C. 、 、 、 、 三种元素形成的化合物的水溶液一定显酸性 三种元素形成的化合物的水溶液一定显酸性 |
D. 与 与 的单质混合加热生成 的单质混合加热生成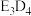 |
您最近一年使用:0次





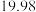


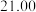

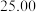
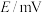
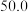
 ,
,
 溶液,先加热,然后置于冷水中
溶液,先加热,然后置于冷水中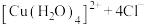

 ,升高温度平衡正移,降低温度平衡逆移
,升高温度平衡正移,降低温度平衡逆移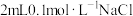 溶液的试管中滴加2滴
溶液的试管中滴加2滴
 溶液
溶液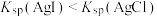
 酸性都强于HClO,发生反应
酸性都强于HClO,发生反应




