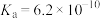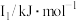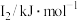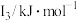1 . 我国科技工作者运用DFT计算研究HCOOH在不同催化剂(Pd和Rh)表面分解产生 的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是
的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是
 的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是
的部分反应历程如图所示,其中吸附在催化剂表面的物种用*表示。下列说法不正确的是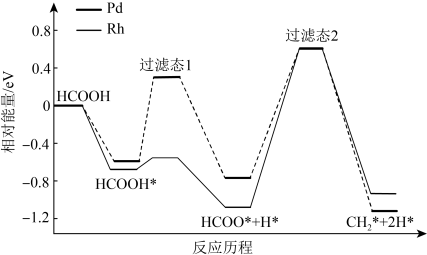
| A.参与反应的反应物总键能小于生成物总键能 |
B.Pd和Rh分别作催化剂时HCOOH分解产生 的 的 不同 不同 |
| C.HCOOH吸附在催化剂表面是一个放热过程 |
D. 是该历程的决速步骤 是该历程的决速步骤 |
您最近一年使用:0次
2024-05-17更新
|
248次组卷
|
2卷引用:浙江省绍兴市上虞区2023-2024学年高二上学期期末教学质量调测化学试题
解题方法
2 . 一种由含铜废催化剂(主要成分为Cu和少量Fe、 、CuO,
、CuO, 等)为原料制备CuCl的工艺流程如下:
等)为原料制备CuCl的工艺流程如下: 浓度较大的体系
浓度较大的体系 ,不溶于乙醇,在潮湿空气中易被氧化。
,不溶于乙醇,在潮湿空气中易被氧化。
(1)下列说法正确的是________。
(2)步骤I中 的实际用量远远超过理论用量,可能原因是
的实际用量远远超过理论用量,可能原因是________ 。
(3)为测定CuCl产品纯度进行如下实验:
A.称量所得CuCl产品10.00g溶于硝酸,配制成250mL溶液;取出25.00mL,加入足量的 溶液,充分反应;
溶液,充分反应;
B.向其中加入少量硝基苯,使沉淀表面被有机物覆盖;
C.加入指示剂,用 标准溶液滴定过量的
标准溶液滴定过量的 溶液;
溶液;
D.重复实验操作三次,消耗 溶液的体积平均为10.00mL。
溶液的体积平均为10.00mL。
已知: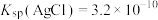 ,
,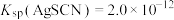 。
。
①加入硝基苯的作用是________ 。
②滴定选用的指示剂是________ ,滴定终点的现象为________ 。
A. B.
B. C.
C. D.
D.
③CuCl的纯度为________ 。
 、CuO,
、CuO, 等)为原料制备CuCl的工艺流程如下:
等)为原料制备CuCl的工艺流程如下:
 浓度较大的体系
浓度较大的体系 ,不溶于乙醇,在潮湿空气中易被氧化。
,不溶于乙醇,在潮湿空气中易被氧化。(1)下列说法正确的是________。
A.步骤Ⅰ,可以用 溶液代替双氧水 溶液代替双氧水 |
B.步骤Ⅱ,试剂X可以是CuO、 、 、 等物质 等物质 |
C.步骤Ⅲ, 适当过量的作用可能是及时除去反应过程中产生的 适当过量的作用可能是及时除去反应过程中产生的 ,避免产生 ,避免产生 |
D.步骤Ⅳ,为了防止CuCl被氧化,可用 水溶液洗涤 水溶液洗涤 |
(2)步骤I中
 的实际用量远远超过理论用量,可能原因是
的实际用量远远超过理论用量,可能原因是(3)为测定CuCl产品纯度进行如下实验:
A.称量所得CuCl产品10.00g溶于硝酸,配制成250mL溶液;取出25.00mL,加入足量的
 溶液,充分反应;
溶液,充分反应;B.向其中加入少量硝基苯,使沉淀表面被有机物覆盖;
C.加入指示剂,用
 标准溶液滴定过量的
标准溶液滴定过量的 溶液;
溶液;D.重复实验操作三次,消耗
 溶液的体积平均为10.00mL。
溶液的体积平均为10.00mL。已知:
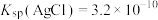 ,
,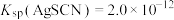 。
。①加入硝基苯的作用是
②滴定选用的指示剂是
A.
 B.
B. C.
C. D.
D.
③CuCl的纯度为
您最近一年使用:0次
解题方法
3 . “氢经济”是“双碳”转型中非常关键的一环。大量安全制空是关键技术之一。
方法一:甲烷-水蒸气催化重整法。其涉及的主要反应如下:
反应I:

反应Ⅱ:
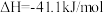
(1)反应 能自发进行的条件是
能自发进行的条件是________ (填“高温”“低温”或“任何温度下”)
(2)为了提高 的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。
的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。
(3)恒定压强为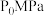 时,将
时,将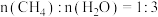 的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。 的物质的量分数与温度的变化曲线是
的物质的量分数与温度的变化曲线是________ (填字母)。
②系统中 的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:________ 。
③600℃时,计算反应Ⅱ的平衡常数
________ ( 是以分压表示的平衡常数,分压=总压
是以分压表示的平衡常数,分压=总压 物质的量分数,结果可用分数表示)。
物质的量分数,结果可用分数表示)。
方法二:甲醇催化脱空法。催化反应的部分机理如下:
历程i: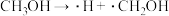 历程ii:
历程ii: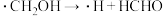
历程iii: 历程iv:
历程iv: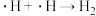
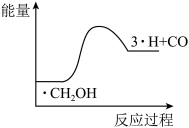
(4)在一个2L恒容密闭容器中投入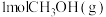 ,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图
,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图________ 。
方法一:甲烷-水蒸气催化重整法。其涉及的主要反应如下:
反应I:


反应Ⅱ:

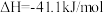
(1)反应
 能自发进行的条件是
能自发进行的条件是(2)为了提高
 的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。
的平衡转化率,同时提高CO的浓度,可以采取的措施是________(填字母)。| A.使用高效催化剂 | B.升高温度 |
| C.增大压强 | D.增大 和 和 物质的量之比 物质的量之比 |
(3)恒定压强为
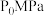 时,将
时,将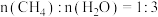 的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中发生反应I和Ⅱ,平衡时,各组分的物质的量分数与温度的关系如图所示。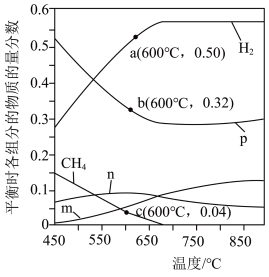
 的物质的量分数与温度的变化曲线是
的物质的量分数与温度的变化曲线是②系统中
 的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:③600℃时,计算反应Ⅱ的平衡常数

 是以分压表示的平衡常数,分压=总压
是以分压表示的平衡常数,分压=总压 物质的量分数,结果可用分数表示)。
物质的量分数,结果可用分数表示)。方法二:甲醇催化脱空法。催化反应的部分机理如下:
历程i:
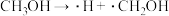 历程ii:
历程ii: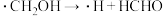
历程iii:
 历程iv:
历程iv: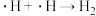
(4)在一个2L恒容密闭容器中投入
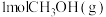 ,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图
,20min后,测得甲醇的转化率(X)与甲醛的选择性(S)分别与温度的关系如左图所示。700℃时,历程iii能量~反应过程如右图所示,在图上画出历程ii的“能量~反应过程”示意图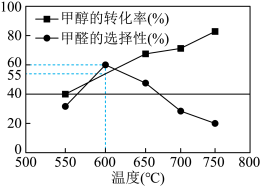
您最近一年使用:0次
4 . 已知25℃时,部分物质的电离常数如下表所示。
(1)根据表中数据,将 的下列三种酸溶液分别稀释100倍,pH变化最小的是
的下列三种酸溶液分别稀释100倍,pH变化最小的是________ 。
a. b.HCN C.
b.HCN C.
(2)常温下,0.1mol/L的 溶液和0.1mol/LHCOONa溶液相比.
溶液和0.1mol/LHCOONa溶液相比.

________ 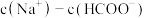 (填“<”“<”=或“>”)。
(填“<”“<”=或“>”)。
(3)下列说法正确的是________。
(4)已知常温下0.1mol/L的 和
和 的pH分别为8.9和8.3,而水解常数
的pH分别为8.9和8.3,而水解常数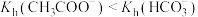 ,则
,则 溶液pH更小的原因是
溶液pH更小的原因是________ 。
HCOOH |
| HCN |
|
|
|
|
|
|
|
 的下列三种酸溶液分别稀释100倍,pH变化最小的是
的下列三种酸溶液分别稀释100倍,pH变化最小的是a.
 b.HCN C.
b.HCN C.
(2)常温下,0.1mol/L的
 溶液和0.1mol/LHCOONa溶液相比.
溶液和0.1mol/LHCOONa溶液相比.
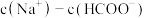 (填“<”“<”=或“>”)。
(填“<”“<”=或“>”)。(3)下列说法正确的是________。
A. 溶液中加入少量水,则溶液中 溶液中加入少量水,则溶液中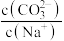 将减小 将减小 |
B.等物质的量浓度的 与 与 混合液中, 混合液中, |
C.向KCN溶液中通入少量 气体发生反应的离子方程式为: 气体发生反应的离子方程式为: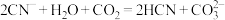 |
D.常温下,将 通入NaOH溶液中,当 通入NaOH溶液中,当 降至 降至 时,溶液中的 时,溶液中的 |
 和
和 的pH分别为8.9和8.3,而水解常数
的pH分别为8.9和8.3,而水解常数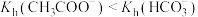 ,则
,则 溶液pH更小的原因是
溶液pH更小的原因是
您最近一年使用:0次
解题方法
5 . 周期表中25号锰元素及其化合物在生产、生活中有广泛应用。
(1)基态Mn原子核外共有________ 种能量不同的电子。
(2)利用 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是:________ 。
①阴极产生气体,其电极反应式为________ 。
② 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是________ 。
③电解过程中,当有 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大________ mol(不考虑溶液中水的体积变化)。
(1)基态Mn原子核外共有
(2)利用
 与
与 反应既可消除污染又可以制备
反应既可消除污染又可以制备 ,将含有
,将含有 尾气和一定比例的空气通入
尾气和一定比例的空气通入 悬浊液中,保持温度不变的情况下,测得溶液中
悬浊液中,保持温度不变的情况下,测得溶液中 和
和 随反应时间的变化如图1所示。导致溶液中
随反应时间的变化如图1所示。导致溶液中 和
和 的变化产生明显差异的原因是:
的变化产生明显差异的原因是: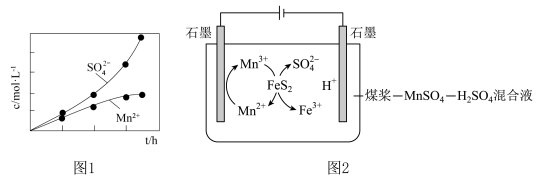
①阴极产生气体,其电极反应式为
②
 与煤中的含硫物质(主要是
与煤中的含硫物质(主要是 )反应的离子方程式是
)反应的离子方程式是③电解过程中,当有
 被氧化时,混合溶液中
被氧化时,混合溶液中 的物质的量将增大
的物质的量将增大
您最近一年使用:0次
6 . 按要求回答下列问题:
(1)酸溶于水可形成 ,
, 的电子式为
的电子式为________ 。判断 和
和 的键角大小:
的键角大小:
________  (填“>”或“<”)。
(填“>”或“<”)。
(2)氨硼烷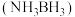 是一种特殊的化合物,分子中与N原子相连的H呈正电性
是一种特殊的化合物,分子中与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。则氨硼烷分子中元素电负性由小到大的顺序为
。则氨硼烷分子中元素电负性由小到大的顺序为________ (填元素符号)
(3)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是________ 。
(4)丁二酮肟(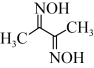 )可与
)可与 反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定
反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定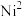 的存在。
的存在。
①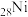 的价电子轨道表示式为
的价电子轨道表示式为________ 。
②丁二酮肟分子中 键和
键和 键数目的比例为
键数目的比例为________ 。
(5)在空气中FeO稳定性小于 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是________ 。
(1)酸溶于水可形成
 ,
, 的电子式为
的电子式为 和
和 的键角大小:
的键角大小:
 (填“>”或“<”)。
(填“>”或“<”)。(2)氨硼烷
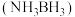 是一种特殊的化合物,分子中与N原子相连的H呈正电性
是一种特殊的化合物,分子中与N原子相连的H呈正电性 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性 。则氨硼烷分子中元素电负性由小到大的顺序为
。则氨硼烷分子中元素电负性由小到大的顺序为(3)N、O、Mg元素的前3级电离能如下表所示:X、Y、Z中为N元素的是
元素 |
|
|
|
X | 737.7 | 1450.7 | 7732.7 |
Y | 1313.9 | 3388.3 | 5300.5 |
Z | 1402.3 | 2856.0 | 4578.1 |
(4)丁二酮肟(
 )可与
)可与 反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定
反应,生成鲜红色的沉淀丁二酮肟镍,这个反应可用来鉴定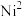 的存在。
的存在。①
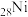 的价电子轨道表示式为
的价电子轨道表示式为②丁二酮肟分子中
 键和
键和 键数目的比例为
键数目的比例为(5)在空气中FeO稳定性小于
 ,从电子排布的角度分析,其主要原因是
,从电子排布的角度分析,其主要原因是
您最近一年使用:0次
解题方法
7 . 下列实验方案设计、现象和结论都正确的是
实验方案 | 现象 | 结论 | |
A | 常温下,用pH计测得 饱和溶液的 饱和溶液的 , , 饱和溶液的 饱和溶液的 |  | 金属性 |
B | 向含有ZnS和 的悬浊液中滴加 的悬浊液中滴加 溶液 溶液 | 生成黑色沉淀 |  |
C | 向稀硫酸中加入铜粉,再加入少量硝酸钾固体 | 开始无明显现象,加入硝酸钾后溶液变蓝 | 硝酸钾起催化作用 |
D | 取 溶液于试管中,加入 溶液于试管中,加入 溶液,充分反应后滴入5滴 溶液,充分反应后滴入5滴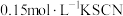 溶液 溶液 | 溶液变血红色 | 说明KI与 的反应有一定限度 的反应有一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 常温下,用 溶液分别滴定浓度均为0.01mol/L的KCl、
溶液分别滴定浓度均为0.01mol/L的KCl、 溶液,所得的沉淀溶解平衡图象如图所示(不考虑
溶液,所得的沉淀溶解平衡图象如图所示(不考虑 的水解)。下列叙述不正确的是
的水解)。下列叙述不正确的是
 溶液分别滴定浓度均为0.01mol/L的KCl、
溶液分别滴定浓度均为0.01mol/L的KCl、 溶液,所得的沉淀溶解平衡图象如图所示(不考虑
溶液,所得的沉淀溶解平衡图象如图所示(不考虑 的水解)。下列叙述不正确的是
的水解)。下列叙述不正确的是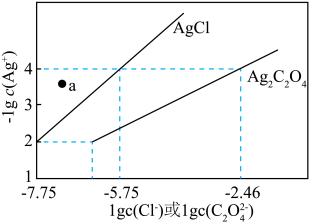
A.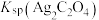 的数量级等于 的数量级等于 |
B.a点时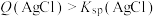 |
C.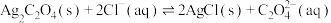 的平衡常数为 的平衡常数为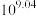 |
D.向浓度相同的KCl、 混合溶液中滴入 混合溶液中滴入 溶液时,先生成AgCl沉淀 溶液时,先生成AgCl沉淀 |
您最近一年使用:0次
9 . 常温下,用0.1000mol/L的NaOH溶液滴定20mL0.1000mol/L的二元弱酸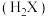 溶液,所得溶液中各种含X的微粒的物质的量分数
溶液,所得溶液中各种含X的微粒的物质的量分数 与pH的变化曲线如图所示。下列叙述不正确的是
与pH的变化曲线如图所示。下列叙述不正确的是
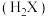 溶液,所得溶液中各种含X的微粒的物质的量分数
溶液,所得溶液中各种含X的微粒的物质的量分数 与pH的变化曲线如图所示。下列叙述不正确的是
与pH的变化曲线如图所示。下列叙述不正确的是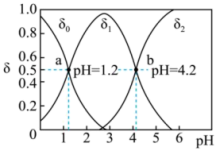
A.加入20mLNaOH溶液时,溶液中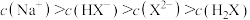 |
B.由图可知 的水解常数 的水解常数 为 为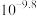 |
C.b点对应的溶液中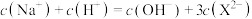 |
D.将等物质的量的NaHX、 溶于水中,所得溶液pH恰好为4.2 溶于水中,所得溶液pH恰好为4.2 |
您最近一年使用:0次
解题方法
10 . 氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图(电极均为石墨电极)。已知:空气中氧气的体积分数为20%。下列说法不正确的是

| A.燃料电池中阳离子的移动方向是从左侧移向右侧 |
B.丁电极上的反应为 |
C.若两池中所用离子膜类型相同,则 |
| D.标准状况下,若电解产生22.4LY,则消耗空气56L |
您最近一年使用:0次