解题方法
1 . 回收利用 是目前解决空间站供氧问题的有效途径,其物质转化如图:
是目前解决空间站供氧问题的有效途径,其物质转化如图:

反应A为 ,是回收利用
,是回收利用 的关键步骤。
的关键步骤。
发生反应A的过程中,有副反应发生,主要涉及的副反应如下:
Ⅰ.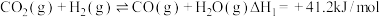
Ⅱ.
(1)反应 的
的
_______  。
。
(2)向某容积为 的恒容密闭容器中充入
的恒容密闭容器中充入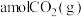 和
和 ,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得
,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得 的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
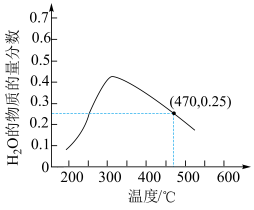
①请用虚线 在上图中画出在250℃-550℃间内,反应 达到平衡时,
达到平衡时, 的物质的量分数随温度变化的曲线
的物质的量分数随温度变化的曲线_______ 。
②在470℃时,反应 的平衡常数
的平衡常数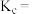
_______  (用含a的最简分数表示)。
(用含a的最简分数表示)。
③实际生产中,温度过高或温度过低均不利于该反应的进行,原因是_______ 。
(3)下列关于空间站内物质转化和能量变化的说法中,不正确 的是_______ (填字母)。
a.反应B的能量变化是电能(或光能) 化学能
化学能
b.目前科学家致力于开发新型催化剂,此催化剂可将 的分解转为放热反应,降低生产
的分解转为放热反应,降低生产 的成本
的成本
c.反应Ⅰ的 ,反应II的
,反应II的
d.镍粒子催化剂的颗粒大小不影响反应速率
(4)用 代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是_______ 。
 是目前解决空间站供氧问题的有效途径,其物质转化如图:
是目前解决空间站供氧问题的有效途径,其物质转化如图:
反应A为
 ,是回收利用
,是回收利用 的关键步骤。
的关键步骤。发生反应A的过程中,有副反应发生,主要涉及的副反应如下:
Ⅰ.
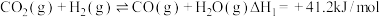
Ⅱ.

(1)反应
 的
的
 。
。(2)向某容积为
 的恒容密闭容器中充入
的恒容密闭容器中充入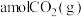 和
和 ,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得
,在纳米镍粒子催化剂作用下,假设只发生反应A(不考虑副反应),在相同时间内测得 的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
的物质的量分数与温度的变化曲线如图所示(不考虑催化剂失效问题)。
①请用
 达到平衡时,
达到平衡时, 的物质的量分数随温度变化的曲线
的物质的量分数随温度变化的曲线②在470℃时,反应
 的平衡常数
的平衡常数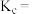
 (用含a的最简分数表示)。
(用含a的最简分数表示)。③实际生产中,温度过高或温度过低均不利于该反应的进行,原因是
(3)下列关于空间站内物质转化和能量变化的说法中,
a.反应B的能量变化是电能(或光能)
 化学能
化学能b.目前科学家致力于开发新型催化剂,此催化剂可将
 的分解转为放热反应,降低生产
的分解转为放热反应,降低生产 的成本
的成本c.反应Ⅰ的
 ,反应II的
,反应II的
d.镍粒子催化剂的颗粒大小不影响反应速率
(4)用
 代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
代替反应A,可实现氢、氧元素完全循环利用,缺点是使用一段时间后催化剂的催化效果会明显下降,其原因是
您最近一年使用:0次
2 . 按要求解答下列各题。
(1)黄铜是人类最早使用的合金之一,主要由 和
和 组成。基态
组成。基态 原子的核外价层电子排布图为
原子的核外价层电子排布图为_______ ;第二电离能
_______ (填“<”“>”或“=”)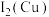 。
。
(2) 和
和 中
中 之间以双键结合,
之间以双键结合, 之间以单键结合。请你预测
之间以单键结合。请你预测 和
和 分子的空间结构为
分子的空间结构为_______ 。 分子中
分子中
_______  分子中
分子中 (选填“<”“>”或“=”)。
(选填“<”“>”或“=”)。
(3)甲醇的沸点(64.7℃)介于水和甲硫醇 ,其原因是
,其原因是_______ 。
(1)黄铜是人类最早使用的合金之一,主要由
 和
和 组成。基态
组成。基态 原子的核外价层电子排布图为
原子的核外价层电子排布图为
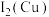 。
。(2)
 和
和 中
中 之间以双键结合,
之间以双键结合, 之间以单键结合。请你预测
之间以单键结合。请你预测 和
和 分子的空间结构为
分子的空间结构为 分子中
分子中
 分子中
分子中 (选填“<”“>”或“=”)。
(选填“<”“>”或“=”)。(3)甲醇的沸点(64.7℃)介于水和甲硫醇
 ,其原因是
,其原因是
您最近一年使用:0次
3 . 下列方程式不正确 的是
A. 与 与 溶液反应的化学方程式: 溶液反应的化学方程式: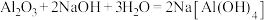 |
B.向氯水中通入 的离子方程式: 的离子方程式: |
C.用覆铜板制作印刷电路板的离子方程式: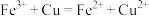 |
D.将 通入到 通入到 溶液变浑浊的化学方程式: 溶液变浑浊的化学方程式: |
您最近一年使用:0次
解题方法
4 . 某同学设计如图装置制备少量的 (易水解).下列说法
(易水解).下列说法不正确 的是

 (易水解).下列说法
(易水解).下列说法
A.B装置中所装试剂为饱和 溶液,其作用是除去 溶液,其作用是除去 中的 中的 |
| B.实验过程中应先点燃A处的酒精灯,再点燃D处的酒精灯 |
C.用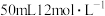 的盐酸与足量的 的盐酸与足量的 反应,所得氯气可以制取 反应,所得氯气可以制取 |
| D.装置C和F中的试剂均为浓硫酸,其作用是防止水蒸气进入E中 |
您最近一年使用:0次
5 . 下列说法不正确 的是
| A.硬铝常用于制造飞机的外壳 |
| B.储氢合金是一类能大量吸收氢气,并与氢气结合成金属氢化物的材料 |
C.葡萄酒中通常添加少量 ,利用它还原性实现杀菌的目的 ,利用它还原性实现杀菌的目的 |
D.84消毒液是以 为主要有效成分的消毒液,与白醋混合可以提升消毒效果 为主要有效成分的消毒液,与白醋混合可以提升消毒效果 |
您最近一年使用:0次
6 . 下列有关化学用语表示正确的是
A.中子数为14的铝原子: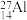 | B.烧碱的化学式: |
C.镁离子的结构示意图: | D. 的电子式为: 的电子式为: |
您最近一年使用:0次
7 . 下列仪器与名称对应且书写正确的是
A.三脚架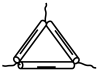 | B.坩埚 | C.平底烧瓶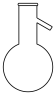 | D.容量瓶 |
您最近一年使用:0次
解题方法
8 . 钠的化合物在日常生活中的应用非常广泛.回答下列问题:
Ⅰ.为了测定 和
和 的混合物中
的混合物中 的质量分数,某同学用如下实验装置完成实验.
的质量分数,某同学用如下实验装置完成实验.

(1)某同学称取 混合物于锥形瓶中,打开止水夹,通入
混合物于锥形瓶中,打开止水夹,通入 ,一段时间后,关闭止水夹,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间
,一段时间后,关闭止水夹,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间 .停止通
.停止通 ,装置C的质量增加
,装置C的质量增加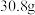 .
.
①仪器a的名称_________ .
②第二次通入 的目的是
的目的是_________ .
③混合物中 的物质的量为
的物质的量为__________  .
.
Ⅱ.侯德榜“联合制碱法”将制碱技术发展到一个新的水平.实验室模拟该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质己略去).

沉淀反应为:
(2)操作1的名称为__________ ;煅烧的化学方程式为__________ .
(3)工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与 反应可制得一种在生产、生活中常用于漂白、消毒的钠盐,同时有
反应可制得一种在生产、生活中常用于漂白、消毒的钠盐,同时有 生成,该反应的化学方程式是
生成,该反应的化学方程式是__________ .
(4)某同学提出制得的纯碱中可能含有氯化钠,请设计实验检验:__________ (写出步骤、现象和结论).
Ⅰ.为了测定
 和
和 的混合物中
的混合物中 的质量分数,某同学用如下实验装置完成实验.
的质量分数,某同学用如下实验装置完成实验.
(1)某同学称取
 混合物于锥形瓶中,打开止水夹,通入
混合物于锥形瓶中,打开止水夹,通入 ,一段时间后,关闭止水夹,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间
,一段时间后,关闭止水夹,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间 .停止通
.停止通 ,装置C的质量增加
,装置C的质量增加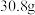 .
.①仪器a的名称
②第二次通入
 的目的是
的目的是③混合物中
 的物质的量为
的物质的量为 .
.Ⅱ.侯德榜“联合制碱法”将制碱技术发展到一个新的水平.实验室模拟该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质己略去).

沉淀反应为:

(2)操作1的名称为
(3)工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与
 反应可制得一种在生产、生活中常用于漂白、消毒的钠盐,同时有
反应可制得一种在生产、生活中常用于漂白、消毒的钠盐,同时有 生成,该反应的化学方程式是
生成,该反应的化学方程式是(4)某同学提出制得的纯碱中可能含有氯化钠,请设计实验检验:
您最近一年使用:0次
9 . 取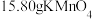 ,加热分解后剩余固体
,加热分解后剩余固体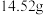 ,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以
,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以 存在,请计算:
存在,请计算:
(1)写出 受热分解的化学方程式
受热分解的化学方程式__________ 。
(2) 的分解率
的分解率__________ 。
(3)气体A的物质的量_________ 。
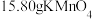 ,加热分解后剩余固体
,加热分解后剩余固体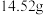 ,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以
,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以 存在,请计算:
存在,请计算:(1)写出
 受热分解的化学方程式
受热分解的化学方程式(2)
 的分解率
的分解率(3)气体A的物质的量
您最近一年使用:0次
10 . 为探究某不溶性固体X(仅含四种元素)的成分,设计并完成了如下实验:
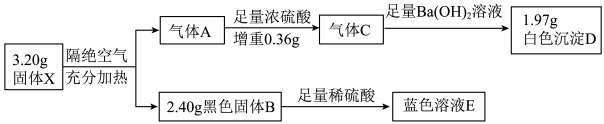
已知气体A是混合物,气体C是纯净物且无色无味.请回答:
(1)盐X中的4种元素是H、O和__________ (填元素符号),黑色固体B的化学式为__________ .
(2)气体C的结构式为__________ .
(3)该流程中X隔绝空气加热分解的化学方程式为__________ .
(4)向蓝色溶液E中加入 溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是
溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是 ,写出该反应的离子方程式
,写出该反应的离子方程式__________ .

已知气体A是混合物,气体C是纯净物且无色无味.请回答:
(1)盐X中的4种元素是H、O和
(2)气体C的结构式为
(3)该流程中X隔绝空气加热分解的化学方程式为
(4)向蓝色溶液E中加入
 溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是
溶液,有白色沉淀生成,溶液的颜色则由蓝色变为深黄色,经分析白色沉淀是 ,写出该反应的离子方程式
,写出该反应的离子方程式
您最近一年使用:0次



