1 . 化学工业上用二氧化锰生产硫酸锰、高锰酸钾、碳酸锰、氯化锰、硝酸锰、一氧化锰等。利用含锰工业废料[含 ,MnOOH,
,MnOOH, 及少量Fe]制备Zn和
及少量Fe]制备Zn和 的一种工艺流程如图所示:
的一种工艺流程如图所示: 在酸性条件下比较稳定,pH高于5.5时易被氧气氧化;
在酸性条件下比较稳定,pH高于5.5时易被氧气氧化;
②室温下,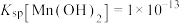 ,
,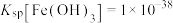 ,
,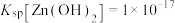 ,
,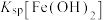
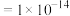 ;
;
③当离子浓度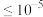 mol/L时,离子沉淀完全。
mol/L时,离子沉淀完全。
请回答下列问题:
(1)“还原焙烧”时,需要把“废料”粉碎的目的是_______ 。
(2)“还原焙烧”时,加入过量炭黑的主要作用是将 、MnOOH转化成MnO,其中炭黑与MnOOH反应时还原剂和还原产物物质的量之比为
、MnOOH转化成MnO,其中炭黑与MnOOH反应时还原剂和还原产物物质的量之比为_______ 。
(3)“酸浸”过程中发生的非氧化还原反应的离子方程式为_______ 。
(4)“酸浸”分离滤渣1和滤液在实验室中使用到的玻璃仪器有_______ ,滤渣1的主要成分是_______ 。
(5)“净化”包括_______ 和调节pH两步,向溶液中加入_______ (填化学式)来调节溶液pH,假设滤液中 ,
, 的浓度是0.1 mol/L,应将溶液pH调节的合理范围是
的浓度是0.1 mol/L,应将溶液pH调节的合理范围是_______ 。
(6)“电解”时,阳极的电极反应式为_______ ,电解后的溶液可以循环利用于该流程中的_______ 步骤。
 ,MnOOH,
,MnOOH, 及少量Fe]制备Zn和
及少量Fe]制备Zn和 的一种工艺流程如图所示:
的一种工艺流程如图所示: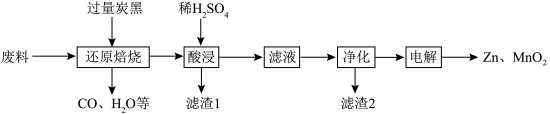
 在酸性条件下比较稳定,pH高于5.5时易被氧气氧化;
在酸性条件下比较稳定,pH高于5.5时易被氧气氧化;②室温下,
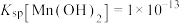 ,
,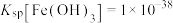 ,
,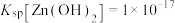 ,
,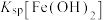
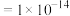 ;
;③当离子浓度
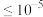 mol/L时,离子沉淀完全。
mol/L时,离子沉淀完全。请回答下列问题:
(1)“还原焙烧”时,需要把“废料”粉碎的目的是
(2)“还原焙烧”时,加入过量炭黑的主要作用是将
 、MnOOH转化成MnO,其中炭黑与MnOOH反应时还原剂和还原产物物质的量之比为
、MnOOH转化成MnO,其中炭黑与MnOOH反应时还原剂和还原产物物质的量之比为(3)“酸浸”过程中发生的非氧化还原反应的离子方程式为
(4)“酸浸”分离滤渣1和滤液在实验室中使用到的玻璃仪器有
(5)“净化”包括
 ,
, 的浓度是0.1 mol/L,应将溶液pH调节的合理范围是
的浓度是0.1 mol/L,应将溶液pH调节的合理范围是(6)“电解”时,阳极的电极反应式为
您最近一年使用:0次
今日更新
|
39次组卷
|
2卷引用:专题8 水溶液中的离子反应与平衡-工业流程题解题策略
解题方法
2 . 利用平衡移动原理,分析一定温度下 在不同pH的
在不同pH的 体系中的可能产物。已知:
体系中的可能产物。已知:
ⅰ.图甲中曲线表示 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。
ⅱ.图乙中曲线I的离子浓度关系符合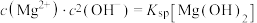 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合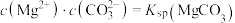 ;[注:起始
;[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图甲得到]。
由图甲得到]。
 在不同pH的
在不同pH的 体系中的可能产物。已知:
体系中的可能产物。已知:ⅰ.图甲中曲线表示
 体系中各含碳粒子的物质的量分数与pH的关系。
体系中各含碳粒子的物质的量分数与pH的关系。ⅱ.图乙中曲线I的离子浓度关系符合
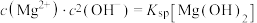 ;曲线Ⅱ的离子浓度关系符合
;曲线Ⅱ的离子浓度关系符合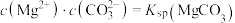 ;[注:起始
;[注:起始 mol⋅L
mol⋅L ,不同pH下
,不同pH下 由图甲得到]。
由图甲得到]。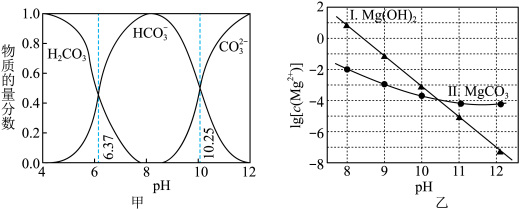
A. 时,碳酸钠溶液体系中存在: 时,碳酸钠溶液体系中存在: |
B.由图甲可知,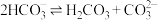 的平衡常数为 的平衡常数为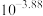 |
C.由图乙可知,初始状态 、 、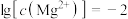 ,平衡后溶液中存在: ,平衡后溶液中存在: 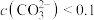 mol⋅L-1 mol⋅L-1 |
D.增大pH,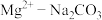 溶液体系中均可发生反应,发生反应: 溶液体系中均可发生反应,发生反应: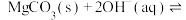 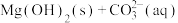 |
您最近一年使用:0次
7日内更新
|
50次组卷
|
2卷引用:专题8 水溶液中的离子反应与平衡-沉淀溶解平衡
3 . 下列实验操作、实验现象和实验结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 向一定浓度 溶液中通入 溶液中通入 气体 气体 | 出现黑色沉淀 |  酸性比 酸性比 强 强 |
| B | 2 mL 1 mol·L NaOH:溶液中滴加2滴0.1 mol·L NaOH:溶液中滴加2滴0.1 mol·L  ,再滴加2滴0.1 mol·L ,再滴加2滴0.1 mol·L  溶液 溶液 | 先生成白色沉淀,后生成红褐色沉淀 | 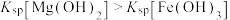 |
| C | 测定等浓度的NaClO溶液和 溶液的pH 溶液的pH | 前者的pH比后者的大 | 非金属性:S>Cl |
| D | 用导线连接铁片和锌片,并插入稀硫酸溶液中,一段时间后,取少量溶液于试管中,向试管中滴加 溶液 溶液 | 溶液颜色无明显变化 | 利用牺牲阳极的阴极法,铁被保护 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7日内更新
|
46次组卷
|
2卷引用:专题8 水溶液中的离子反应与平衡-沉淀溶解平衡
4 . 为达到相应实验目的,下列实验设计可行的是
| 编号 | 实验目的 | 实验过程 |
| A | 证明NO2气体中存在平衡2NO2(g) N2O4(g) N2O4(g) | 压缩盛有NO2气体的注射器至原来体积的一半,红棕色变浅 |
| B | 比较室温下Cu(OH)2、Mg(OH)2溶度积的大小 | 向5mL0.2mol/LMgCl2溶液中滴加少量NaOH溶液,充分振荡后,再滴加几滴0.2mo/LCuCl2溶液,白色沉淀逐渐转化为蓝色 |
| C | 比较FeCl3和H2O2的氧化性强弱 | 常温下,向H2O2溶液中加入FeCl3溶液,将带火星的木条放在试管口,木条复燃 |
| D | 探究浓度对反应速率的影响 | 向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液,观察实验现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-09-16更新
|
32次组卷
|
2卷引用:专题8 水溶液中的离子反应与平衡-沉淀溶解平衡
5 . 三氯化六氨合钴 是一种重要的化工产品,实验室可用反应
是一种重要的化工产品,实验室可用反应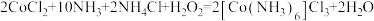 制备。下列说法正确的是
制备。下列说法正确的是
 是一种重要的化工产品,实验室可用反应
是一种重要的化工产品,实验室可用反应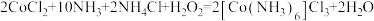 制备。下列说法正确的是
制备。下列说法正确的是A. 的VSEPR模型为 的VSEPR模型为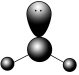 |
B. 的电子式为 的电子式为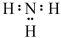 |
C.基态Cl原子的价电子轨道表示式为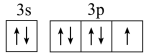 |
D. 中含有18mol共价键 中含有18mol共价键 |
您最近一年使用:0次
2024-09-07更新
|
51次组卷
|
2卷引用:专题5 物质结构与性质 元素周期律-原子结构与性质
6 . 异山梨醇是一种由生物质制备的高附加值化学品,150℃时其制备过程及相关物质浓度随时间变化如图所示,15h后异山梨醇浓度不再变化。下列说法错误的是
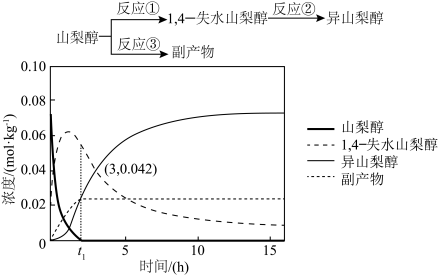
A.选择相对较短的反应时间,及时分离可获得高产率的1, 失水山梨醇 失水山梨醇 |
| B.反应的活化能:①<② |
C. 时刻,反应①和③趋于彻底 时刻,反应①和③趋于彻底 |
D.3h时,瞬时速率(异山梨醇)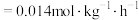 |
您最近一年使用:0次
2024-09-06更新
|
177次组卷
|
2卷引用:专题7 化学反应速率与化学平衡-化学反应速率及影响因素
解题方法
7 . 碳化钛在航空航天、机械加工等领域应用广泛,其晶胞结构(如图所示)与氯化钠相似,晶胞的边长为anm。下列说法正确的是
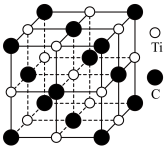
A.该物质的化学式为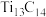 |
B.基态Ti原子的价电子排布式为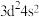 |
C.C原子之间的最短距离为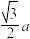 |
D.设 为阿伏加德罗常数的值,则晶体的密度为 为阿伏加德罗常数的值,则晶体的密度为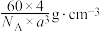 |
您最近一年使用:0次
2024-09-04更新
|
63次组卷
|
2卷引用:专题5 物质结构与性质 元素周期律-晶体结构与性质
8 . 下列化学用语表述正确的是
A. 的电子式: 的电子式: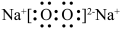 | B. 电离: 电离: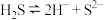 |
| C.Ge位于元素周期表的d区 | D.有机物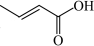 不存在顺反异构 不存在顺反异构 |
您最近一年使用:0次
2024-09-04更新
|
43次组卷
|
2卷引用:专题5 物质结构与性质 元素周期律-原子结构与性质
9 . 下列化学用语表示正确的是
A.NH3分子的VSEPR模型: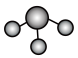 |
B.中子数为18的氯原子: |
C.HCl的形成过程: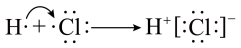 |
D.碳的基态原子轨道表示式: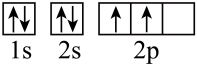 |
您最近一年使用:0次
2024-08-28更新
|
68次组卷
|
2卷引用:专题5 物质结构与性质 元素周期律-原子结构与性质
解题方法
10 . 化学用语是学习化学的重要工具,下列化学用语表述正确的是
A. 的电离方程式: 的电离方程式: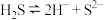 |
B.2-己烯的键线式: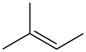 |
C. 的VSEPR模型: 的VSEPR模型: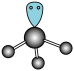 |
D.基态 的价层电子排布图: 的价层电子排布图: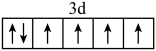 |
您最近一年使用:0次
2024-08-28更新
|
52次组卷
|
2卷引用:专题5 物质结构与性质 元素周期律-原子结构与性质



