1 . 黑火药爆炸时的反应为: ,该反应的还原剂是
,该反应的还原剂是
 ,该反应的还原剂是
,该反应的还原剂是| A.C | B. | C. | D.S |
您最近一年使用:0次
2023-04-21更新
|
1342次组卷
|
22卷引用:浙江省丽水市高中发展共同体2021-2022学年高一下学期(2月)返校考试化学试题
浙江省丽水市高中发展共同体2021-2022学年高一下学期(2月)返校考试化学试题重庆市2020-2021学年高一上学期期末联合检测化学试题河北省石家庄市第二中学西校区2020-2021学年高一上学期假期考试化学试题浙江省嘉兴市2020-2021学年高一下学期期末考试化学试题第2课时 氧化剂和还原剂(课后)——课前、课中、课后同步专题精编(人教版2019必修第一册)浙江省温州市2021-2022学年高一上学期期末教学质量统一检测化学试题(B卷)浙江省温州市2021-2022学年高一上学期期末教学质量统一检测化学(A卷)试题浙江省杭州市富阳区第二中学等两校2021-2022学年高一下学期3月检测化学试题浙江省杭州学军中学2021-2022学年高一下学期期中考试化学试题黑龙江省七台河市勃利县高级中学2022-2023学年高一上学期9月月考化学试题浙江省杭州市八县区2022-2023学年高一上学期期末检测化学试题浙江省杭州市临平区2022-2023学年高一上学期期末学业水平测试化学试题(已下线)【2023】【高一上】【杭七】【期末考】【高中化学】【廖汨平收集】浙江省杭州市S9联盟2022-2023学年高一下学期期中考试化学试题(已下线)第04讲 氧化剂和还原剂 氧化还原反应的配平及规律-【暑假自学课】2023年新高一化学暑假精品课(人教版2019必修第一册)浙江省宁波市2022—2023学年高一下学期学业水平考试模拟化学试题浙江省杭嘉湖金四县区2022-2023学年高一6月学考模拟考试化学试题(已下线)专题七 氧化还原反应(已下线)合格考真题汇编5氧化还原反应山西省大同市阳高县第四中学2023-2024学年高一上学期期中考试化学试卷浙江省余姚中学2023-2024学年高一下学期3月质量检测化学(学考)试题浙江省“七彩阳光”新高考研究联盟2023-2024学年高一下学期4月期中联考化学试题
11-12高一上·江苏南通·阶段练习
名校
解题方法
2 . 下列各组中的离子,能在溶液中大量共存的是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
您最近一年使用:0次
2022-06-24更新
|
950次组卷
|
62卷引用:浙江省丽水市高中发展共同体2021-2022学年高一下学期(2月)返校考试化学试题
浙江省丽水市高中发展共同体2021-2022学年高一下学期(2月)返校考试化学试题青海省西宁市大通回族土族自治县第二完全中学2022-2023学年高一下学期开学检测化学试卷 (已下线)2011-2012学年江苏省如皋中学高一上学期质量检测化学试卷(已下线)2011-2012学年安徽省桐城十中高一上学期期末考试化学试卷2015-2016学年湖北省黄石市有色一中高一上11月期中月考化学试卷云南省峨山彝族自治县第一中学2016-2017学年高二下学期期末考试化学试题西藏林芝二中2017-2018学年高一上学期期末考试化学试卷2017-2018学年度深圳市富源学校第一学期高一化学期中考试试题北京市大兴区2017-2018学年高一上学期期末检测化学试题广西桂梧高中2017-2018学年高一上学期期末考试化学试卷【全国百强校】吉林省长春外国语学校2018-2019学年高一(文)上学期期末考试化学试题云南省峨山彝族自治县第一中学2018-2019学年高一下学期期中考试化学试题西藏自治区拉萨市那曲第二高级中学2018-2019学年高一上学期期末考试化学试题山西省运城市永济涑北中学2019-2020学年高一12月月考化学试题山东省淄博市淄川区般阳中学2019-2020学年高一上学期期中考试化学试题陕西省咸阳百灵中学2019-2020学年高一上学期第二次月考化学试题湖北省荆州市沙市区沙市中学高一上学期化学第二章《化学物质及其变化》过关训练7四川省宜宾市第四中学校2019-2020学年高一下学期第二次月考化学试题(已下线)3.2.3 离子反应练习(1)——《高中新教材同步备课》(苏教版 必修第一册)重庆市部分区2019-2020学年高一上学期期末考试化学试题北京市昌平区新学道临川学校2020-2021学年高一(京津班)上学期第一次月考化学试题(已下线)第二章 元素与物质世界(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)云南省腾冲市益群中学2020-2021学年高一上学期期中考试化学试题山东省沂水县第四中学2020~2021学年高一上学期阶段检测化学试题(已下线)【浙江新东方】26北京市北京教育学院附属中学2020-2021学年高一上学期期中考试化学试题北京市第十四中学2020-2021学年高一上学期期中考试化学试题北京市第三十五中学2020-2021学年高一上学期期中考试化学试题广东省汕头市澄海中学2020-2021学年高一上学期期中考试化学试题辽宁省大连市普兰店区第一中学2020-2021学年高一上学期第一阶段考试化学试题重庆市复旦中学2020-2021学度高一上学期第一次段考化学试题北京市石景山区2020-2021学年高一上学期期末调研化学试卷题广东省台山市华侨中学2020-2021学年高一上学期第一次月考化学试题云南省文山州砚山县第三高级中学2020-2021学年高一上学期期中考试化学试题吉林省长春市第二十中学2020-2021学年高一上学期第二次考试化学试题吉林省长春市第二十中学2020-2021学年高一上学期第三次考试化学试题甘肃省庆阳市第六中学2021-2022学年高一上学期第一次月考化学试题人教2019版必修第一册课后习题 第一章 物质及其变化复习与提高天津市第三中学2021-2022学年高一上学期期中考试化学试题河南省开封市2021-2022学年高一上学期期末调研考试化学试题天津市河东区普通高中2022年高二学业水平合格考试模拟化学试题云南省红河州2021-2022学年高二下学期期末考试化学试题天津市红桥区2019-2020学年高一上学期期中考试化学试题天津市红桥区2020-2021学年高一上学期期末考试化学试题重庆市沙坪坝实验中学校2021-2022学年高一上学期期末考试化学试题河南省平顶山市蓝天高级中学2021-2022学年高一上学期期末考试化学试题北京市顺义区杨镇一中2022-2023学年高一上学期期中考试化学试题云南昆明师范专科学校附属中学2022-2023学年高一上学期期中考试化学试题甘肃省临夏州临夏县中学2021-2022学年高一上学期期中考试化学试题陕西省西安市鄠邑区第二中学2021-2022学年高一上学期第二次月考化学试题江西省萍乡市2022-2023学年高一上学期期末考试化学试题吉林省舒兰市第十八中学校2022-2023学年高一上学期期中考试化学试题甘肃省天水市秦安县第一中学2022-2023学年高一上学期期末考试化学试题(已下线)合格考汇编2离子反应辽宁省朝阳市名校联考2023-2024学年高一上学期期中考试化学试题 云南省宣威市第三中学2023-2024学年高一上学期第一次月考化学试题北京市回民学校2023-2024学年高一上学期期中考试化学试题甘肃省武威第七中学2023-2024学年高一上学期期末考试化学试题陕西省铜川市第一中学2023-2024学年高一上学期期中考试化学试题广东省湛江市某校2023-2024学年高一上学期期中考试化学试题广东省揭阳市惠来慈云实验中学2024-2025学年高一上学期月考化学试卷宁夏回族自治区中宁县第一中学2022-2023学年高一上学期10月月考化学试题
3 . 亚磷酸(H3PO3)为二元弱酸,是重要的化工原料,可作尼龙增白剂、农药中间体等。25℃时,H3PO3电离常数Ka1=8.4×10-3、Ka2=2.9×10-7。
(1)Na2HPO3为____ (填“正盐”或“酸式盐”),其溶液显____ (填“酸性”、“中性”、“碱性”或“无法判断”)。
(2)写出NaH2PO3水解的离子方程式____ ;25℃时,NaH2PO3水解常数K=____ (结果保留两位有效数字)。
(3)25℃时,CH3COOH电离常数Ka=1.8×10-5,写出CH3COOH溶液中与少量Na2HPO3溶液反应的离子方程式____ 。
(1)Na2HPO3为
(2)写出NaH2PO3水解的离子方程式
(3)25℃时,CH3COOH电离常数Ka=1.8×10-5,写出CH3COOH溶液中与少量Na2HPO3溶液反应的离子方程式
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题:
(1)常用作油漆、涂料的红色颜料(填写化学式)_______ ;
(2)写出NaOH的电子式_______ ;
(3)比较沸点:H2O_______ H2S(填“>”“<”“=”),并解释原因_______ 。
(1)常用作油漆、涂料的红色颜料(填写化学式)
(2)写出NaOH的电子式
(3)比较沸点:H2O
您最近一年使用:0次
2022-02-22更新
|
188次组卷
|
2卷引用:浙江省丽水市高中发展共同体2021-2022学年高一下学期(2月)返校考试化学试题
5 . 碘在生活和科研中有重要的应用。
(1)加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。
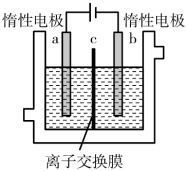
先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。阳极的电极反应式为____ 。电解过程中b电极附近溶液的pH____ (填“增大”或“减小”)
(2)已知:①I2(aq) I2(CCl4) K1=85
I2(CCl4) K1=85
②I2(aq)+I-(aq) I
I (aq) K2≈1000
(aq) K2≈1000
③I2(g)+H2(g) 2HI(g) ΔH=-9.48kJ·mol-1
2HI(g) ΔH=-9.48kJ·mol-1
④W(s)+I2(g) WI2(g) ΔH<0
WI2(g) ΔH<0
常温下,把溶解在H2O的I2提取到CCl4中的方法叫萃取,①正向移动,碘单质在水和CCl4混合液中存在①的溶解平衡,萃取时通常采用“少量多次”的目的是____ 。
(3)常温下,10mL0.1mol·L-1KI水溶液加入一定量的碘单质,加入10mLCCl4进行萃取,静置分层(实验过程中不考虑体积变化)。已知:I-和I 不溶于CCl4,实验测得CCl4层液体中c(I2)=0.085mol·L-1,则水层中c(I-)=
不溶于CCl4,实验测得CCl4层液体中c(I2)=0.085mol·L-1,则水层中c(I-)=____ mol·L-1。
(4)反应③在一定条件下速率方程:v正=Kc(I2)c(H2),K为速率常数,下列说法正确的是____ 。
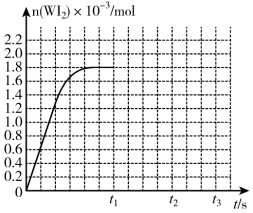
(5)在碘钨灯灯泡内封存少量的碘可以延长钨丝寿命,发生反应④,为模拟上述反应,取0.004mol碘和0.004mol钨放置在50.0mL密闭容器中反应,在450℃,n(WI2)随时间变化图象如图所示,t1时,将温度升高到530℃,t2时达到平衡(530℃平衡常数K=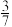 )。请在图中画出n(WI2)从t1~t3随时间变化图象
)。请在图中画出n(WI2)从t1~t3随时间变化图象____ 。
(1)加碘食盐中含有碘酸钾(KIO3),现以电解法制备碘酸钾,实验装置如图所示。

先将一定量的碘溶于过量氢氧化钾溶液,发生反应:3I2+6KOH=5KI+KIO3+3H2O,将该溶液加入阳极区,另将氢氧化钾溶液加入阴极区,开始电解。阳极的电极反应式为
(2)已知:①I2(aq)
 I2(CCl4) K1=85
I2(CCl4) K1=85②I2(aq)+I-(aq)
 I
I (aq) K2≈1000
(aq) K2≈1000③I2(g)+H2(g)
 2HI(g) ΔH=-9.48kJ·mol-1
2HI(g) ΔH=-9.48kJ·mol-1④W(s)+I2(g)
 WI2(g) ΔH<0
WI2(g) ΔH<0常温下,把溶解在H2O的I2提取到CCl4中的方法叫萃取,①正向移动,碘单质在水和CCl4混合液中存在①的溶解平衡,萃取时通常采用“少量多次”的目的是
(3)常温下,10mL0.1mol·L-1KI水溶液加入一定量的碘单质,加入10mLCCl4进行萃取,静置分层(实验过程中不考虑体积变化)。已知:I-和I
 不溶于CCl4,实验测得CCl4层液体中c(I2)=0.085mol·L-1,则水层中c(I-)=
不溶于CCl4,实验测得CCl4层液体中c(I2)=0.085mol·L-1,则水层中c(I-)=(4)反应③在一定条件下速率方程:v正=Kc(I2)c(H2),K为速率常数,下列说法正确的是
| A.反应③的ΔS=0 |
| B.反应③I2平衡转化率随温度升高变大 |
| C.升高温度速率常数k变大 |
| D.混合气体颜色不变时,反应已达到平衡状态 |
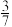 )。请在图中画出n(WI2)从t1~t3随时间变化图象
)。请在图中画出n(WI2)从t1~t3随时间变化图象
您最近一年使用:0次
6 . 某实验小组用100mL0.50mol·L-1NaOH溶液与60mL0.50mo·L-1硫酸溶液进行中和热的测定,装置如图所示。回答下列问题:

(1)若实验共需要400mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体____ g。
(2)图中玻璃搅拌棒“环形”的目的是____ 。
(3)测量终止温度的方法是____ 。
(4)请填写表中的平均温度差:
(5)近似认为0.50mol·L-1NaOH溶液与0.50mol·L-1硫酸溶液的密度都是lg·cm-3,中和后生成溶液的比热容c=4.2J·g-1·℃-1,则上述实验测得的中和热ΔH=____ (结果保留至小数点后一位)。
(6)上述实验测得中和热的数值小于57.3kJ·mol-1,产生偏差的原因可能是____ 。

(1)若实验共需要400mLNaOH溶液,实验室在配制该溶液时,则需要称量NaOH固体
(2)图中玻璃搅拌棒“环形”的目的是
(3)测量终止温度的方法是
(4)请填写表中的平均温度差:
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 平均温度差(t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.2 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
(6)上述实验测得中和热的数值小于57.3kJ·mol-1,产生偏差的原因可能是
| A.量取NaOH溶液时俯视读数 | B.配制NaOH溶液定容时俯视 |
| C.实验装置保温隔热效果差 | D.向酸溶液中一次性加入碱溶液 |
您最近一年使用:0次
7 . 随着能源技术的发展,科学家们将目光聚焦于锂的开发与研究。
(1)基态Li原子中电子占据最高能级的符号是____ ,占据该能级电子的电子云轮廓图的形状为____ 形。
(2)在周期表中,与Li元素的化学性质最相似的邻族元素是____ (填元素符号)。
(3)部分元素的第一电离能(I1)如表所示。
①碱金属的第一电离能与碱金属的金属性的联系是____ 。
②Be的第一电离能比Li的大,从原子结构角度分析其原因是____ 。
(1)基态Li原子中电子占据最高能级的符号是
(2)在周期表中,与Li元素的化学性质最相似的邻族元素是
(3)部分元素的第一电离能(I1)如表所示。
| 元素 | Li | Be | Na | K |
| I1(kJ·mol-1) | 520 | 900 | 496 | 419 |
①碱金属的第一电离能与碱金属的金属性的联系是
②Be的第一电离能比Li的大,从原子结构角度分析其原因是
您最近一年使用:0次
解题方法
8 . 氧化石墨烯的结构片段如图所示。一种新的制备方法是用Pt电极,在稀硫酸中对石墨进行电解氧化。电解水产生的大量高活性氧自由基(如:·OH)与石墨反应生成了氧化石墨烯。下列说法正确的是


| A.石墨烯应该与电源的负极相连 |
| B.电解过程中阴极反应式:2H2O+2e-=H2↑+2OH- |
| C.可用稀盐酸代替稀硫酸进行电解 |
| D.生成“·OH”的电极反应式:H2O-e-=OH-+H+ |
您最近一年使用:0次
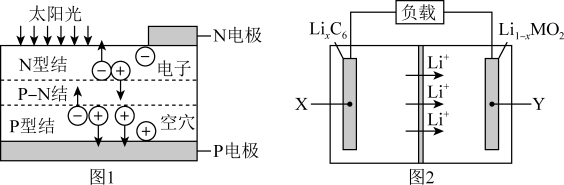
9 . 近年来国家大力扶持新能源项目建设。图1是太阳能电池工作示意图,可与图2石墨烯锂电池联合使用。已知石墨烯锂电池的反应式:LixC6+Li1-xMO2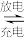 C6+LiMO2(M=Mn、Co、Ni),下列说法正确的是
C6+LiMO2(M=Mn、Co、Ni),下列说法正确的是
 C6+LiMO2(M=Mn、Co、Ni),下列说法正确的是
C6+LiMO2(M=Mn、Co、Ni),下列说法正确的是
| A.给石墨烯锂电池充电时,Y接太阳能电池的N电极 |
| B.石墨烯锂电池放电时,正极反应为:Li1-xMnO2+xLi+=LiMnO2 |
| C.石墨烯锂电池放电时,负极反应为:LixC6-xe-=xLi++C6 |
| D.石墨烯锂电池充电时,每转移lmol电子,图2中X极质量减少7g |
您最近一年使用:0次
2022-02-21更新
|
427次组卷
|
2卷引用:浙江省丽水市高中发展共同体2021-2022学年高二下学期(2月)返校考试化学试题
10 . 已知NaHCO3溶液与盐酸反应生成CO2吸热,Na2CO3溶液与盐酸反应生成CO2放热。关于下列△H的判断不正确的是
CO (aq)+H+(aq)
(aq)+H+(aq) HCO
HCO (aq) △H1
(aq) △H1
HCO (aq)+H+(aq)
(aq)+H+(aq) H2CO3(aq) △H2
H2CO3(aq) △H2
H2CO3(aq) H2O(l)+CO2(g) △H3
H2O(l)+CO2(g) △H3
OH-(aq)+H+(aq) H2O(l) △H4
H2O(l) △H4
CO
 (aq)+H+(aq)
(aq)+H+(aq) HCO
HCO (aq) △H1
(aq) △H1HCO
 (aq)+H+(aq)
(aq)+H+(aq) H2CO3(aq) △H2
H2CO3(aq) △H2H2CO3(aq)
 H2O(l)+CO2(g) △H3
H2O(l)+CO2(g) △H3OH-(aq)+H+(aq)
 H2O(l) △H4
H2O(l) △H4| A.△H1<0 | B.△H2+△H3>0 |
| C.△H1+△H2+△H3<0 | D.△H2<△H4 |
您最近一年使用:0次



