名校
解题方法
1 . 如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:
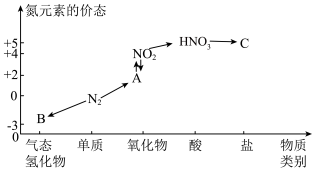
(1)写出 N2 的一种用途:________________ 。
(2)B 物质的电子式为:________________ 。
(3)HNO3与图中的物质 C 常用于检验 Cl-的存在,则 C 的化学式为______________ 。
(4)实验室制取物质 B 的化学方程式为______________ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为___________ 。
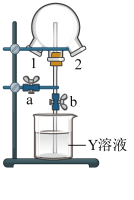
(6)如图装置可用于探究氯气与氨气的反应。实验时先通过三颈瓶瓶口 1 通入氨气,然后关闭 b 活塞,再通过瓶口 2 通入氯气。
①实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为________ ,请设计一个实验方案鉴定该固体中的阳离子____________
② 实验完毕后,观察到三颈瓶内还有黄绿色气体, 简述如何处理才能不污染环境___________________ 。
(7)将 3.2g 铜与 60.0mL 一定浓度的硝酸发生反应,铜完全溶解,产生 NO2和 NO 混合气体的体积为 8.96L(标况)。待产生的气体全部释放后,向溶液加入 100mL 2.0mol/L 的 NaOH 溶液,恰好使溶液中的 Cu2+全部转化成沉淀,则原硝酸溶液的浓度为_______________ mol/L。

(1)写出 N2 的一种用途:
(2)B 物质的电子式为:
(3)HNO3与图中的物质 C 常用于检验 Cl-的存在,则 C 的化学式为
(4)实验室制取物质 B 的化学方程式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为

(6)如图装置可用于探究氯气与氨气的反应。实验时先通过三颈瓶瓶口 1 通入氨气,然后关闭 b 活塞,再通过瓶口 2 通入氯气。
①实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为
② 实验完毕后,观察到三颈瓶内还有黄绿色气体, 简述如何处理才能不污染环境
(7)将 3.2g 铜与 60.0mL 一定浓度的硝酸发生反应,铜完全溶解,产生 NO2和 NO 混合气体的体积为 8.96L(标况)。待产生的气体全部释放后,向溶液加入 100mL 2.0mol/L 的 NaOH 溶液,恰好使溶液中的 Cu2+全部转化成沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次
2020-03-28更新
|
399次组卷
|
2卷引用:天津市滨海新区塘沽第一中学2019 —2020 学年高一下学期第一 次月考化学试题
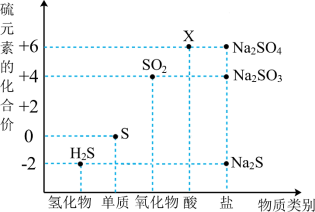
2 . 如图是硫元素的常见化合价与部分物质类别的对应关系。请回答下列问题。
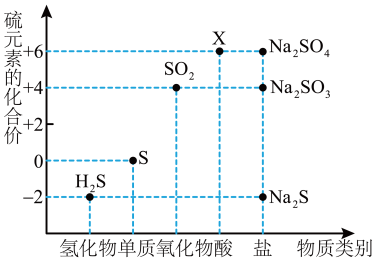
(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的___________ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有___________ (填化学式)。
(3)将 与
与 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为___________ 。
(4)配平下列反应_________________ 。
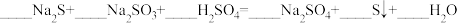
(5)一定条件下,在 密闭容器中发生反应:
密闭容器中发生反应: ,开始时加入
,开始时加入 、
、 、
、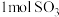 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 ,用
,用 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为___________ ,在 末
末 的浓度为
的浓度为___________ 。若改变下列一个条件,推测该反应的速率发生的变化(填“增大”“减小”或“不变”)
①升高温度,化学反应速率___________ ;
②再充入 ,化学反应速率
,化学反应速率___________ ;
③将容器体积变为 ,化学反应速率
,化学反应速率___________ 。

(1)X的浓溶液与碳在一定条件下可以发生反应,体现了X的
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质有
(3)将
 与
与 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为(4)配平下列反应
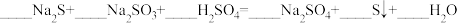
(5)一定条件下,在
 密闭容器中发生反应:
密闭容器中发生反应: ,开始时加入
,开始时加入 、
、 、
、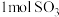 ,在
,在 末测得
末测得 的物质的量是
的物质的量是 ,用
,用 的浓度变化表示反应的平均速率为
的浓度变化表示反应的平均速率为 末
末 的浓度为
的浓度为①升高温度,化学反应速率
②再充入
 ,化学反应速率
,化学反应速率③将容器体积变为
 ,化学反应速率
,化学反应速率
您最近一年使用:0次
3 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:___________ (填化学式)。
(2)X的浓溶液与铜在一定条件下可以发生反应,该反应的化学反应方程式为___________ ,体现了X的_________ 性质。
(3)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了___________ 。
(4)配平下列反应:_______
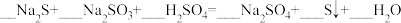 。
。
(5)如图是验证二氧化硫性质的实验装置。___________ (填序号,下同);B中___________ ;C中___________ 。D装置的作用是___________ 。
(2)X的浓溶液与铜在一定条件下可以发生反应,该反应的化学反应方程式为
(3)收集了一些含有S元素的酸雨,放置一段时间后,pH变小,小攀认为可能是因为酸雨中的亚硫酸被氧化为了
(4)配平下列反应:
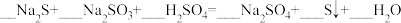 。
。(5)如图是验证二氧化硫性质的实验装置。

您最近一年使用:0次
名校
解题方法
4 . 如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:_____ ,体现了c的_____ 性。
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质是_____ (填化学式)。
(3)将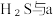 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为_____ 。
(4)配平下列反应:_____ 。
_____
(5)为防止多余的a气体污染环境,应将尾气通入_____ 溶液中;
(6)将足量的 溶液中,下列说法正确的是
溶液中,下列说法正确的是_____ (填字母)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀

(7)将 片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,
片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时, 被腐蚀的速率逐渐降低的可能原因为
被腐蚀的速率逐渐降低的可能原因为_____ 。 的污染并变废为宝,我国正在探索在一定条件下,用
的污染并变废为宝,我国正在探索在一定条件下,用 还原,
还原, 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:_____ 。
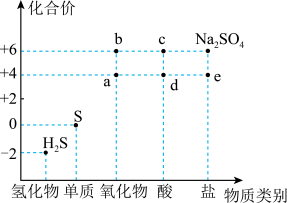
(2)仅从硫元素化合价变化的角度分析,图中只有还原性的物质是
(3)将
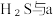 混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为
混合可生成淡黄色沉淀,该反应中氧化产物与还原产物的物质的量之比为(4)配平下列反应:
_____

(5)为防止多余的a气体污染环境,应将尾气通入
(6)将足量的
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(7)将
 片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,
片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时, 被腐蚀的速率逐渐降低的可能原因为
被腐蚀的速率逐渐降低的可能原因为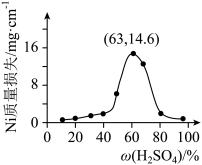
 的污染并变废为宝,我国正在探索在一定条件下,用
的污染并变废为宝,我国正在探索在一定条件下,用 还原,
还原, 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:
您最近一年使用:0次
5 . 如图是氨元素的几种价态与物质类别的对应关系:

回答下列问题:
(1)写出氮元素在元素周期表的位置_______ 。
(2)从氢元素化合价分析, 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式:_______ ,这个反应 体现了
体现了_______ 性。
(3) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为_______ 。写出用C检验 的存在的离子方程式
的存在的离子方程式_______ 。
(4)物质B为氮元素的气态氢化物,B的化学式为_______ ;实验室制取B的化学方程式为_______ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为_______ 。

回答下列问题:
(1)写出氮元素在元素周期表的位置
(2)从氢元素化合价分析,
 具有氧化性和还原性。写出
具有氧化性和还原性。写出 生成A的化学反应方程式:
生成A的化学反应方程式: 体现了
体现了(3)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为 的存在的离子方程式
的存在的离子方程式(4)物质B为氮元素的气态氢化物,B的化学式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
您最近一年使用:0次
6 . 回答下列问题
(Ⅰ)自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:

(1)图2中的N对应图1中物质的化学式为_______ 。
(2)X与Z反应中氧化剂与还原剂的物质的量之比为_______ 。
(3) 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为_______ 。
(4)铜和M的浓溶液反应生成Z的化学方程式为_______ ;若要证明该反应产物有 ,需要采取的操作是
,需要采取的操作是_______ 。
(Ⅱ)氮氧化物( )是大气污染物之一,处理
)是大气污染物之一,处理 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。
方案l:
(5)汽车排气管上装有催化转化器,可减少尾气对环境的污染,有害气体CO和NO反应可转化为无害气体排放,写出反应的化学方程式_______ 。
方案2:
在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
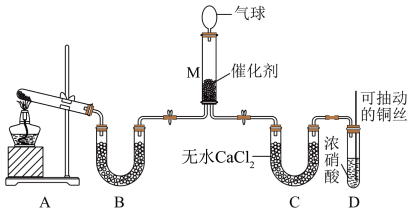
(6)用装置A制备 ,反应的化学方程式为
,反应的化学方程式为_______ ;装置B内的试剂是_______ 。
(7)装置D中发生反应的离子方程式是_______ ;可抽动铜丝的优点是_______ 。
(8)在装置M中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中 和
和 的物质的量之比为
的物质的量之比为_______ 。
方案3:
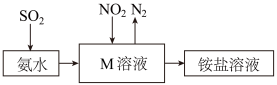
(9)工业生产中利用氨水吸收少量 和
和 ,原理如图所示。
,原理如图所示。 被吸收过程的离子方程式是
被吸收过程的离子方程式是_______ 。
(Ⅰ)自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:

(1)图2中的N对应图1中物质的化学式为
(2)X与Z反应中氧化剂与还原剂的物质的量之比为
(3)
 溶液易被氧化,检验
溶液易被氧化,检验 溶液变质的试剂为
溶液变质的试剂为(4)铜和M的浓溶液反应生成Z的化学方程式为
 ,需要采取的操作是
,需要采取的操作是(Ⅱ)氮氧化物(
 )是大气污染物之一,处理
)是大气污染物之一,处理 对于环境保护具有重要的意义。
对于环境保护具有重要的意义。方案l:
(5)汽车排气管上装有催化转化器,可减少尾气对环境的污染,有害气体CO和NO反应可转化为无害气体排放,写出反应的化学方程式
方案2:
在一定条件下
 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
(6)用装置A制备
 ,反应的化学方程式为
,反应的化学方程式为(7)装置D中发生反应的离子方程式是
(8)在装置M中
 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中 和
和 的物质的量之比为
的物质的量之比为方案3:
(9)工业生产中利用氨水吸收少量
 和
和 ,原理如图所示。
,原理如图所示。 被吸收过程的离子方程式是
被吸收过程的离子方程式是
您最近一年使用:0次
7 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:

(1)写出化学式:Y______ ,Z______ 。
(2)X与Y能否共存______ (填“能”或“不能”),若不能请写出化学方程式若能请说明理由______ 。
(3)Na2SO3与足量Z反应的离子方程式______ 。
(4)Na2S2O3是重要的化工原料。Na2S2O3中硫元素的化合价为______ ,从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______ (填序号)。
a.Na2S+S b.Na2SO3+S c.Na2SO4+SO2 d.Na2SO3+SO3
(5)Y与稀硝酸反应,硝酸的还原产物为NO,写出反应的化学方程式:______ 。

(1)写出化学式:Y
(2)X与Y能否共存
(3)Na2SO3与足量Z反应的离子方程式
(4)Na2S2O3是重要的化工原料。Na2S2O3中硫元素的化合价为
a.Na2S+S b.Na2SO3+S c.Na2SO4+SO2 d.Na2SO3+SO3
(5)Y与稀硝酸反应,硝酸的还原产物为NO,写出反应的化学方程式:
您最近一年使用:0次
名校
解题方法
8 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
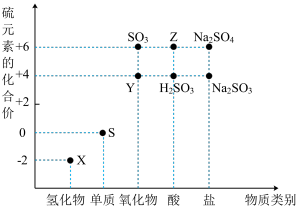
(1)写出化学式:Y___________ ,Z___________ 。
(2)X与Y能否共存___________ (填“能”或“不能”),若不能请写出化学方程式若能请说明理由___________ 。
(3) 与足量Z反应的离子方程式
与足量Z反应的离子方程式___________ 。
(4) 是重要的化工原料。
是重要的化工原料。 中硫元素的化合价为
中硫元素的化合价为___________ ,从氧化还原反应的角度分析,下列制备 的方案理论上可行的是
的方案理论上可行的是___________ (填序号)。
a. b.
b. c.
c.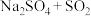 d.
d.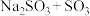
(5)写出Z的浓溶液与木炭发生反应的化学方程式___________ 。
(6)Y与稀硝酸反应,硝酸的还原产物为 ,写出反应的化学方程式:
,写出反应的化学方程式:___________ 。

(1)写出化学式:Y
(2)X与Y能否共存
(3)
 与足量Z反应的离子方程式
与足量Z反应的离子方程式(4)
 是重要的化工原料。
是重要的化工原料。 中硫元素的化合价为
中硫元素的化合价为 的方案理论上可行的是
的方案理论上可行的是a.
 b.
b. c.
c.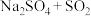 d.
d.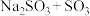
(5)写出Z的浓溶液与木炭发生反应的化学方程式
(6)Y与稀硝酸反应,硝酸的还原产物为
 ,写出反应的化学方程式:
,写出反应的化学方程式:
您最近一年使用:0次
2023-11-15更新
|
274次组卷
|
2卷引用:天津市北辰区2023-2024学年高三上学期11月期中考试化学试题
9 . 利用物质类别及核心元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系。回答下列问题:

(1)质量相同的a和b的物质的量之比为_______ 。
(2)c的浓溶液能与S反应产生一种含硫元素的气体,该气体的化学式为_______ 。
(3)将足量的a通入 溶液中,下列说法正确的是
溶液中,下列说法正确的是_______ (填字母)。
A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀
(4)将c的浓溶液滴到白纸上,白纸变黑体现了c的_______ 性。
(5)将Ni片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为_______ 。

(6)“银针验毒”的原理: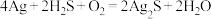 。
。 在该反应中_______(填字母)。
在该反应中_______(填字母)。
(7)为进一步减少 的污染并变废为宝,我国正在探索在一定条件下,用CO还原
的污染并变废为宝,我国正在探索在一定条件下,用CO还原 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:_______ 。

(1)质量相同的a和b的物质的量之比为
(2)c的浓溶液能与S反应产生一种含硫元素的气体,该气体的化学式为
(3)将足量的a通入
 溶液中,下列说法正确的是
溶液中,下列说法正确的是A.溶液中出现白色沉淀
B.溶液没有明显变化
C.若再通入
 或
或 ,则溶液中均会出现白色沉淀
,则溶液中均会出现白色沉淀(4)将c的浓溶液滴到白纸上,白纸变黑体现了c的
(5)将Ni片浸在不同质量分数的c溶液中,经4小时腐蚀后的质量损失情况如图所示,当c的浓度大于63%时,Ni被腐蚀的速率逐渐降低的可能原因为

(6)“银针验毒”的原理:
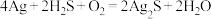 。
。 在该反应中_______(填字母)。
在该反应中_______(填字母)。| A.是氧化剂 | B.是还原剂 |
| C.既是氧化剂也是还原剂 | D.既不是氧化剂也不是还原剂 |
 的污染并变废为宝,我国正在探索在一定条件下,用CO还原
的污染并变废为宝,我国正在探索在一定条件下,用CO还原 得到单质硫的方法来除去
得到单质硫的方法来除去 。写出该反应的化学方程式:
。写出该反应的化学方程式:
您最近一年使用:0次
2023-03-27更新
|
192次组卷
|
2卷引用:天津市西青区杨柳青一中2022-2023学年高一下学期第一次适应性测试化学试题
名校
10 . 易混易错题组
Ⅰ.使用正确的化学用语填空
(1)写出下列物质的电子式
氮气_______ 过氧化钠 _________ 四氯化碳________
(2)写出下列物质的结构式
二氧化碳________ 过氧化氢 _________ 次氯酸________
(学法题)正确书写化合物的电子式需要注意的问题是_____________
Ⅱ.正确比较下列各组对应关系
(1)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序为:___________
②原子半径由大到小的顺序为:___________
③离子半径由大到小的顺序为:___________
(2)比较下列微粒半径大小,用“>”或“<”填空
①F-________ Cl- ②Fe2+________ Fe3+ ③O2-_________ Mg2+
(学法题)粒子半径大小比较方法(两点即可)___________
Ⅰ.使用正确的化学用语填空
(1)写出下列物质的电子式
氮气
(2)写出下列物质的结构式
二氧化碳
(学法题)正确书写化合物的电子式需要注意的问题是
Ⅱ.正确比较下列各组对应关系
(1)已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则这四种元素:
①原子序数由大到小的顺序为:
②原子半径由大到小的顺序为:
③离子半径由大到小的顺序为:
(2)比较下列微粒半径大小,用“>”或“<”填空
①F-
(学法题)粒子半径大小比较方法(两点即可)
您最近一年使用:0次



