1 . 化学是一门以实验为基础的学科。回答下列问题:
I.碘的溶解性
(1)在碘水溶液中加入1mL四氯化碳,振荡试管,观察碘被四氯化碳萃取,形成___________ 色的碘的四氯化碳溶液。再向试管里加入1mL浓碘化钾水溶液,振荡试管,溶液颜色变浅,用离子方程式解释溶液颜色变浅的原因:___________ ,碘在四氯化碳中比在纯水中的溶解性好,试从分子结构角度解释其原因:___________ 。
Ⅱ. 晶体制备
晶体制备
(2)向盛有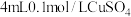 溶液的试管里滴加几滴1molL氨水,首先形成难溶物,继续添加氨水并振荡试管,可以观察到的实验现象为
溶液的试管里滴加几滴1molL氨水,首先形成难溶物,继续添加氨水并振荡试管,可以观察到的实验现象为___________ 。再向试管中加入极性较___________ 的试剂乙醇(填“大”或“小”),并用玻璃棒摩擦试管壁,可以观察到有___________ 色的Cu(NH3)4SO4·H2O晶体析出。
Ⅲ.乙酸乙酯的制备
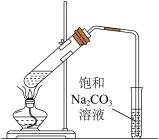
(3)利用下图装置制备乙酸乙酯,乙醇、乙酸、浓硫酸三种试剂的加入顺序为___________ ,反应的化学方程式为___________ 。
I.碘的溶解性
(1)在碘水溶液中加入1mL四氯化碳,振荡试管,观察碘被四氯化碳萃取,形成
Ⅱ.
 晶体制备
晶体制备(2)向盛有
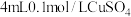 溶液的试管里滴加几滴1molL氨水,首先形成难溶物,继续添加氨水并振荡试管,可以观察到的实验现象为
溶液的试管里滴加几滴1molL氨水,首先形成难溶物,继续添加氨水并振荡试管,可以观察到的实验现象为Ⅲ.乙酸乙酯的制备
(3)利用下图装置制备乙酸乙酯,乙醇、乙酸、浓硫酸三种试剂的加入顺序为

您最近一年使用:0次
名校
解题方法
2 . 将少量饱和FeCl3溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
甲:饱和FeCl3溶液滴加到冷水中;
乙:饱和FeCl3溶液滴加到NaOH溶液中;
丙:饱和FeCl3溶液滴加到沸水中。
(1)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为___ 。
(2)判断丙中是否成功制备胶体的方法,在化学上称作___ 。
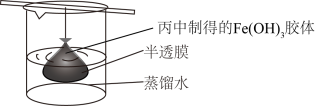
(3)可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若___ (填实验现象),则说明该Fe(OH)3胶体中的杂质离子已经完全除去。
甲:饱和FeCl3溶液滴加到冷水中;
乙:饱和FeCl3溶液滴加到NaOH溶液中;
丙:饱和FeCl3溶液滴加到沸水中。
(1)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为
(2)判断丙中是否成功制备胶体的方法,在化学上称作
(3)可用如图所示的装置除去Fe(OH)3胶体中的杂质离子来提纯Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若

您最近一年使用:0次
2021-11-01更新
|
164次组卷
|
3卷引用:天津市武清区杨村第一中学2021-2022学年高一上学期第一次阶段性检测化学试题
名校
3 . 回答下列问题:
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
(2)磷的一种化合物叫亚磷酸(H3PO3)。已知:
Ⅰ.0.1mol/LH3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。
①关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是___________ 。
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
②写出H3PO3与过量NaOH溶液反应的离子方程式___________ 。
(3)H3PO2(次磷酸)是一元中强酸,H3PO2及NaH2PO2均可将溶液中的 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。
①NaH2PO2属于___________ (填“正盐”“酸式盐”或“碱式盐”)。
②利用H3PO2化学镀银,反应中氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为___________ (写化学式)。
(1)下列为用氯化铁固体制备氢氧化铁胶体的相关实验,可以达到实验目的的是___________。
| A | B | C | D |
| 配制FeCl3溶液制备 | Fe(OH)3胶体 | 观察胶体的丁达尔效应 | 分离Fe(OH)3胶体与溶液 |
 |  |  | 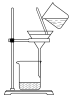 |
| A.A | B.B | C.C | D.D |
Ⅰ.0.1mol/LH3PO3溶液的pH=1.7;
Ⅱ.H3PO3与NaOH反应只生成Na2HPO3和NaH2PO3两种盐;
Ⅲ.H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。
①关于H3PO3的说法:①强酸;②弱酸;③二元酸;④三元酸;⑤氧化性酸;⑥还原性酸,其中正确的是
A.②④⑥ B.②③⑥ C.①④⑤ D.②③⑤
②写出H3PO3与过量NaOH溶液反应的离子方程式
(3)H3PO2(次磷酸)是一元中强酸,H3PO2及NaH2PO2均可将溶液中的
 还原为银,从而可用于化学镀银。
还原为银,从而可用于化学镀银。①NaH2PO2属于
②利用H3PO2化学镀银,反应中氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为
您最近一年使用:0次
4 . 烃类物质是整个有机化学的基础,烃及其衍生物共同构成了庞大的有机物世界。
(1)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。___________ 。___________ (填化学式)。
③甲烷与氯气反应生成的产物最多的是___________ (填化学式)。
④若将1molCH4与一定量的 反应,得到等物质的量的4种有机产物,则消耗
反应,得到等物质的量的4种有机产物,则消耗 的物质的量为
的物质的量为___________ mol。
(2)我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇。乙醇的官能团名称是___________ 。使用酸性 溶液可以检测酒驾,利用了乙醇的
溶液可以检测酒驾,利用了乙醇的___________ (填“氧化性”或“还原性”),其原理是:司机口中呼出的乙醇可以使检测仪中的橙色重铬酸钾(K2Cr2O)转变为绿色的硫酸铬[Cr2(SO4)3],上述反应涉及的乙醇性质有___________ 。
A.无色液体 B.密度比水的小 C.易挥发 D.具有还原性
(1)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。

A.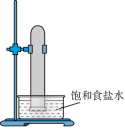 B.
B. C.
C.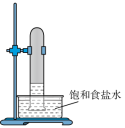 D.
D.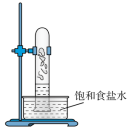
③甲烷与氯气反应生成的产物最多的是
④若将1molCH4与一定量的
 反应,得到等物质的量的4种有机产物,则消耗
反应,得到等物质的量的4种有机产物,则消耗 的物质的量为
的物质的量为(2)我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇。乙醇的官能团名称是
 溶液可以检测酒驾,利用了乙醇的
溶液可以检测酒驾,利用了乙醇的A.无色液体 B.密度比水的小 C.易挥发 D.具有还原性
您最近一年使用:0次
名校
解题方法
5 . 现有甲、乙、丙三名同学分别进行 Fe(OH)3胶体的制备实验。
甲同学:向 FeCl3溶液中加少量NaOH溶液。
乙同学:向40mL煮沸的蒸馏水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
丙同学:直接加热饱和 FeCl3溶液。
(1)其中操作正确的同学是___________ ,反应的离子方程式为___________ 。
(2)证明有Fe(OH)3胶体生成的方法是___________ 。
(3)向Fe(OH)3胶体中逐滴加入稀硫酸至过量,过程中的现象是___________ 。
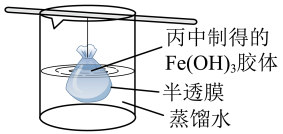
(4)可用如图所示的装置除去 Fe(OH)3胶体中的杂质离子来提纯 Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若___________ (填实验现象),则说明该Fe(OH)3胶体中的杂质离子已经完全除去。
甲同学:向 FeCl3溶液中加少量NaOH溶液。
乙同学:向40mL煮沸的蒸馏水中逐滴加入5~6滴 FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。
丙同学:直接加热饱和 FeCl3溶液。
(1)其中操作正确的同学是
(2)证明有Fe(OH)3胶体生成的方法是
(3)向Fe(OH)3胶体中逐滴加入稀硫酸至过量,过程中的现象是
(4)可用如图所示的装置除去 Fe(OH)3胶体中的杂质离子来提纯 Fe(OH)3胶体,实验过程中需不断更换烧杯中的蒸馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入AgNO3溶液,若

您最近一年使用:0次
解题方法
6 . 利用铁元素价类二维图可以多角度研究含铁物质的性质及转化关系,请完成下列问题。__________ 。
A.Fe B. C.
C.
(2)下列说法正确的是___________ 。 粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为
粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为__________ ,
(4)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:___________ 。
(5)人体血红蛋白分子中含有 ,正是这些
,正是这些 使血红蛋白分子具有载氧功能。亚硝酸钠(
使血红蛋白分子具有载氧功能。亚硝酸钠( )可将人体血红蛋白中的
)可将人体血红蛋白中的 转化为
转化为 ,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中
,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中 发生
发生__________ 反应,说明亚硝酸钠具有__________ 性;误食亚硝酸钠中毒,可服维生素C缓解,说明维生素C具有__________ 性。
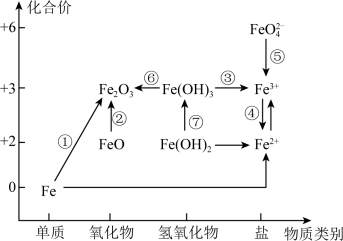
A.Fe B.
 C.
C.
(2)下列说法正确的是
A. 是碱性氧化物
是碱性氧化物
B.铁与高温水蒸气的反应可实现上述转化①
C.FeO是一种黑色粉末,不稳定,在空气中受热,迅速发生转化②
(3)取少量 粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为
粉末于烧杯中,加入适量盐酸至完全溶解,发生反应的离子方程式为(4)制备氢氧化亚铁时,现象由白色絮状沉淀最终转化为红褐色沉淀,请用化学方程式解释现象:
(5)人体血红蛋白分子中含有
 ,正是这些
,正是这些 使血红蛋白分子具有载氧功能。亚硝酸钠(
使血红蛋白分子具有载氧功能。亚硝酸钠( )可将人体血红蛋白中的
)可将人体血红蛋白中的 转化为
转化为 ,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中
,生成高铁血红蛋白而丧失与氧气的结合能力,反应过程中 发生
发生
您最近一年使用:0次
7 . Ⅰ.如图所示,在一个小烧杯里加入研细的 晶体。将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入
晶体。将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入 晶体,并用玻璃棒快速搅拌。
晶体,并用玻璃棒快速搅拌。
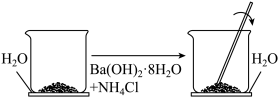
(1)该实验中观察到的现象除产生刺激性气味的气体及反应混合物呈糊状以外,还有___________ 。该反应___________ (填“是”或“不是”)氧化还原反应。
(2)该反应为___________ (填“吸”或“放”)热反应,说明反应物的总能量___________ (填“大于”或“小于”)生成物的总能量。
(3)实验中要用玻璃棒搅拌的原因是________ 。
Ⅱ.
(4)现有如下两个反应:A. ,B.
,B. 。判断上述两个反应中能设计成原电池的是
。判断上述两个反应中能设计成原电池的是___________ (填“A”或“B”)。
(5)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:
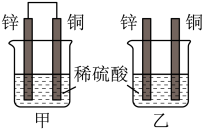
①下列说法正确的是___________ 。
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲___________ 乙(填“>”“<”或“=”)。
③请写出图中构成原电池的负极电极反应式:___________ 。
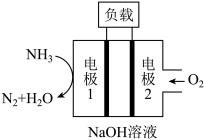
(6)瑞典ASES公司设计的曾用于驱动潜艇的液氨一液氧燃料电池的示意图如下,则该燃料电池工作时的总反应方程式为___________ 。
(7)燃料电池的工作原理是将燃料和氧化剂(如 )反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极,
)反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极, 为燃料,采用氢氧化钠溶液为电解液,电池工作时消耗
为燃料,采用氢氧化钠溶液为电解液,电池工作时消耗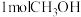 ,则电路中通过
,则电路中通过___________ mol电子。
(8)请设计一个简单原电池,证明氧化性 ,则负极材料为
,则负极材料为___________ ,正极电极反应式为___________ 。
 晶体。将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入
晶体。将此小烧杯放在事先滴有3~4滴水的玻璃片上,然后向小烧杯中加入 晶体,并用玻璃棒快速搅拌。
晶体,并用玻璃棒快速搅拌。
(1)该实验中观察到的现象除产生刺激性气味的气体及反应混合物呈糊状以外,还有
(2)该反应为
(3)实验中要用玻璃棒搅拌的原因是
Ⅱ.
(4)现有如下两个反应:A.
 ,B.
,B. 。判断上述两个反应中能设计成原电池的是
。判断上述两个反应中能设计成原电池的是(5)将纯锌片和纯铜片按图中方式插入100mL相同浓度的稀硫酸中一段时间,回答下列问题:

①下列说法正确的是
A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化
C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大
②在相同时间内,两烧杯中产生气泡的速度:甲
③请写出图中构成原电池的负极电极反应式:
(6)瑞典ASES公司设计的曾用于驱动潜艇的液氨一液氧燃料电池的示意图如下,则该燃料电池工作时的总反应方程式为

(7)燃料电池的工作原理是将燃料和氧化剂(如
 )反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极,
)反应所放出的化学能直接转化为电能。现设计一燃料电池,以C为电极, 为燃料,采用氢氧化钠溶液为电解液,电池工作时消耗
为燃料,采用氢氧化钠溶液为电解液,电池工作时消耗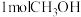 ,则电路中通过
,则电路中通过(8)请设计一个简单原电池,证明氧化性
 ,则负极材料为
,则负极材料为
您最近一年使用:0次
名校
8 . 通过如图完成氢氧化铁胶体制备及性质实验。

【实验步骤】
①向沸水中加入几滴饱和 FeCl3溶液,继续煮沸至液体呈红褐色停止加热。
②把盛有 CuSO4溶液和 Fe(OH)3胶体的烧杯置于暗处,用红色激光笔照射两杯中的液体,观察现象。
【回答问题】
(1)图中盛有饱和FeCl3溶液的仪器名称为:___________ 。
(2)Fe(OH)3胶体___________ (“能”或“不能”)透过半透膜,请写出制备Fe(OH)3胶体的离子方程式:___________ 。
(3)步骤2中能观察到的现象为___________ ,胶体产生的该现象称为___________ 。胶体与其他分散系不同的根本原因是___________ 。
(4)若将实验改为向饱和FeCl3溶液中加入NaOH溶液,则观察到的现象为___________ ,该反应的离子方程式为___________ 。

【实验步骤】
①向沸水中加入几滴饱和 FeCl3溶液,继续煮沸至液体呈红褐色停止加热。
②把盛有 CuSO4溶液和 Fe(OH)3胶体的烧杯置于暗处,用红色激光笔照射两杯中的液体,观察现象。
【回答问题】
(1)图中盛有饱和FeCl3溶液的仪器名称为:
(2)Fe(OH)3胶体
(3)步骤2中能观察到的现象为
(4)若将实验改为向饱和FeCl3溶液中加入NaOH溶液,则观察到的现象为
您最近一年使用:0次
9 . 按要求回答下列问题:
(1)将少量铁红(成分为 )加到适量盐酸中,得到黄色溶液。离子方程式为:
)加到适量盐酸中,得到黄色溶液。离子方程式为:_____ ;
(2)小烧杯中加入 蒸馏水,加热至沸腾,向沸水中滴入几滴上述黄色溶液,继续煮沸直至液体呈
蒸馏水,加热至沸腾,向沸水中滴入几滴上述黄色溶液,继续煮沸直至液体呈_____ 色,可制得 胶体。
胶体。 粒子直径大小的范围是
粒子直径大小的范围是_____ 。写出生成 胶体的化学方程式:
胶体的化学方程式:_____ 。
(3)制备 胶体时,加热煮沸时间过长,结果出现红褐色沉淀,滴加稀硫酸沉淀又溶解。沉淀溶解的离子方程式
胶体时,加热煮沸时间过长,结果出现红褐色沉淀,滴加稀硫酸沉淀又溶解。沉淀溶解的离子方程式_____ 。
(4)下列现象或过程不属于化学过程的是_____ 。
a.丁达尔效应 b.悬浊液静置后澄清 c.稀豆浆变质 d. 在空气中放置变质
在空气中放置变质
(5)当光束通过下列分散系时,能观察到丁达尔效应的是_____ 。
a.蒸馏水 b. 溶液 c.鸡蛋清加
溶液 c.鸡蛋清加 混合液 d.稀硫酸
混合液 d.稀硫酸
(1)将少量铁红(成分为
 )加到适量盐酸中,得到黄色溶液。离子方程式为:
)加到适量盐酸中,得到黄色溶液。离子方程式为:(2)小烧杯中加入
 蒸馏水,加热至沸腾,向沸水中滴入几滴上述黄色溶液,继续煮沸直至液体呈
蒸馏水,加热至沸腾,向沸水中滴入几滴上述黄色溶液,继续煮沸直至液体呈 胶体。
胶体。 粒子直径大小的范围是
粒子直径大小的范围是 胶体的化学方程式:
胶体的化学方程式:(3)制备
 胶体时,加热煮沸时间过长,结果出现红褐色沉淀,滴加稀硫酸沉淀又溶解。沉淀溶解的离子方程式
胶体时,加热煮沸时间过长,结果出现红褐色沉淀,滴加稀硫酸沉淀又溶解。沉淀溶解的离子方程式(4)下列现象或过程不属于化学过程的是
a.丁达尔效应 b.悬浊液静置后澄清 c.稀豆浆变质 d.
 在空气中放置变质
在空气中放置变质(5)当光束通过下列分散系时,能观察到丁达尔效应的是
a.蒸馏水 b.
 溶液 c.鸡蛋清加
溶液 c.鸡蛋清加 混合液 d.稀硫酸
混合液 d.稀硫酸
您最近一年使用:0次
10 . 化学是一门以实验为基础的学科。回答下列问题:
Ⅰ.压强对化学平衡的影响。
(1)如图所示,用50 mL注射器吸入20 mLNO2和N2O4的混合气体(使注射器的活塞位于Ⅰ处),将细管端用胶塞封闭。然后把活塞拉到Ⅱ处,观察到管内混合气体的颜色变化为_____ 。

Ⅱ.沉淀的转化
(2)向盛有2 mL0.1 mol/LKI溶液的试管中滴加2滴0.1 mol/LAgNO3溶液,观察到的现象为_____ ,振荡试管,然后再向其中滴加8滴0.1 mol Na2S溶液,发生反应的离子方程式为_____ ,观察到的现象为_____ 。
Ⅲ.金属的腐蚀。
(3)将经过酸洗除锈的铁钉用饱和食盐水浸泡一下,放入如图所示的装置中,仪器a的名称为_____ ,几分钟后,观察导管中水柱的变化为______ ,引起这种变化的原因为_____ 。

Ⅰ.压强对化学平衡的影响。
(1)如图所示,用50 mL注射器吸入20 mLNO2和N2O4的混合气体(使注射器的活塞位于Ⅰ处),将细管端用胶塞封闭。然后把活塞拉到Ⅱ处,观察到管内混合气体的颜色变化为

Ⅱ.沉淀的转化
(2)向盛有2 mL0.1 mol/LKI溶液的试管中滴加2滴0.1 mol/LAgNO3溶液,观察到的现象为
Ⅲ.金属的腐蚀。
(3)将经过酸洗除锈的铁钉用饱和食盐水浸泡一下,放入如图所示的装置中,仪器a的名称为

您最近一年使用:0次



