1 . I.化学兴趣小组对以下实验进行探究:
(1)牙膏摩擦剂由碳酸钙、氢氧化铝组成;写出氢氧化铝与NaOH溶液反应的离子方程式______ 。
II.现欲探究铁及其化合物的氧化性或还原性,请完成以下实验报告:
(2)称取用磨砂纸打磨后的铁钉2.8g放入50.0mL稀硫酸中,充分反应后若2.8g纯净的Fe全部参加反应。反应中转移______ mol电子。
(3)下列有关Fe2+的说法不正确的是_______ (选填序号)。
III.卤族元素是典型的非金属元素,已知稀溴水与稀铁盐(含Fe3+)溶液的颜色相近;Cl2能将Fe2+氧化为Fe3+;Fe3+能将I-氧化为I2。请完成以下实验报告:
(4)关于F、Cl、Br、I的比较,不正确的是_______ (选填序号)。
(5)稀溴水的颜色为_______ 。
(6)将Fe2+逐滴滴加到稀溴水溶液中,再加入几滴淀粉碘化钾溶液。溶液变为蓝色,不能证明证明Br2能将Fe2+氧化为Fe3+,因为Br2与I-作用产生的碘可以使淀粉变蓝,写出Br2与I-作用的离子方程式_______ 。另将Fe2+逐滴滴加到另一份稀溴水溶液中,加入几滴______ 溶液,溶液变为红色,证明Br2能将Fe2+氧化为Fe3+。
(7)另取20mLFeSO4溶液,向其中通入Cl2。若Fe2+恰好完全转化为Fe3+,消耗的Cl2在标准状况下的体积为0.336L,则该FeSO4溶液的物质的量浓度为______ mol/L。
(1)牙膏摩擦剂由碳酸钙、氢氧化铝组成;写出氢氧化铝与NaOH溶液反应的离子方程式
II.现欲探究铁及其化合物的氧化性或还原性,请完成以下实验报告:
(2)称取用磨砂纸打磨后的铁钉2.8g放入50.0mL稀硫酸中,充分反应后若2.8g纯净的Fe全部参加反应。反应中转移
(3)下列有关Fe2+的说法不正确的是
| A.可以先加KSCN溶液再加氯水来检验Fe2+ |
| B.可以先加铁粉再加KSCN溶液来检验Fe2+ |
| C.能使酸性KMnO4溶液紫色褪去 |
| D.能观察到溶液颜色为浅绿色 |
III.卤族元素是典型的非金属元素,已知稀溴水与稀铁盐(含Fe3+)溶液的颜色相近;Cl2能将Fe2+氧化为Fe3+;Fe3+能将I-氧化为I2。请完成以下实验报告:
(4)关于F、Cl、Br、I的比较,不正确的是
| A.它们的原子核外电子层数随核电荷数的增加而增多 |
| B.单质(F2、Cl2、Br2、I2)的氧化性随核电荷数的增加而减弱 |
| C.被其他卤素单质从卤化物中置换出来的可能性随原子序数的增加而增大 |
| D.它们的氢化物的稳定性随原子序数的增加而增强 |
(6)将Fe2+逐滴滴加到稀溴水溶液中,再加入几滴淀粉碘化钾溶液。溶液变为蓝色,不能证明证明Br2能将Fe2+氧化为Fe3+,因为Br2与I-作用产生的碘可以使淀粉变蓝,写出Br2与I-作用的离子方程式
(7)另取20mLFeSO4溶液,向其中通入Cl2。若Fe2+恰好完全转化为Fe3+,消耗的Cl2在标准状况下的体积为0.336L,则该FeSO4溶液的物质的量浓度为
您最近一年使用:0次
2 . 氨水中存在的主要溶质微粒是NH3·H2O。
已知:常温下,醋酸和NH3·H2O的电离平衡常数均为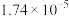
(1)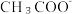 结合H+的能力
结合H+的能力___________  结合OH-的能力(填“>”“=”或“<”),则
结合OH-的能力(填“>”“=”或“<”),则 溶液呈
溶液呈___________ 性。
(2)为证明一水合氨是弱电解质,甲乙丙三位同学利用下面的试剂进行实验:
试剂: 氨水、NH₄Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸馏水。
氨水、NH₄Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸馏水。
①甲用pH试纸测出 氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论是否正确?
氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论是否正确?___________ (“正确”或“错误”)。
②乙取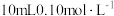 氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测出其pH为b,他认为只要a、b满足:a-b
氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测出其pH为b,他认为只要a、b满足:a-b___________ 2(填“>”“=”或“<”)即可确认一水合氨是弱电解质。
③丙取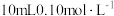 氨水,滴入2滴酚酞试液,显粉红色,再加入
氨水,滴入2滴酚酞试液,显粉红色,再加入 晶体少量,颜色变浅。你认为这一方法能否证明一水合氨是弱电解质
晶体少量,颜色变浅。你认为这一方法能否证明一水合氨是弱电解质___________ (填“能”或“否”)。
(3)常温下,取不同浓度、不同温度的氨水测定,得到下表实验数据。
①温度升高, 的电离平衡向
的电离平衡向___________ 方向移动,能支持该结论的表中数据是___________ 。
a.电离常数 b.电离程度 c.c(OH⁻) d.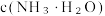
②表中c(OH-))基本不变的原因是___________ 。
③常温下,在氨水中加入少量的氯化铵晶体,下列说法错误的是___________ 。
a.溶液的pH增大 b. 减小 c.
减小 c.  减小
减小
已知:常温下,醋酸和NH3·H2O的电离平衡常数均为
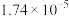
(1)
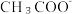 结合H+的能力
结合H+的能力 结合OH-的能力(填“>”“=”或“<”),则
结合OH-的能力(填“>”“=”或“<”),则 溶液呈
溶液呈(2)为证明一水合氨是弱电解质,甲乙丙三位同学利用下面的试剂进行实验:
试剂:
 氨水、NH₄Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸馏水。
氨水、NH₄Cl晶体、醋酸铵晶体、酚酞试剂、pH试纸、蒸馏水。①甲用pH试纸测出
 氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论是否正确?
氨水的pH为10,据此他认定一水合氨是弱电解质,你认为这一结论是否正确?②乙取
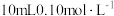 氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测出其pH为b,他认为只要a、b满足:a-b
氨水,用pH试纸测出其pH为a,然后用蒸馏水稀释至1000mL,再用pH试纸测出其pH为b,他认为只要a、b满足:a-b③丙取
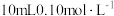 氨水,滴入2滴酚酞试液,显粉红色,再加入
氨水,滴入2滴酚酞试液,显粉红色,再加入 晶体少量,颜色变浅。你认为这一方法能否证明一水合氨是弱电解质
晶体少量,颜色变浅。你认为这一方法能否证明一水合氨是弱电解质(3)常温下,取不同浓度、不同温度的氨水测定,得到下表实验数据。
| 温度 | c(NH₃·H₂O)/mol·L⁻¹ | 电离常数 | 电离程度 | c(OH~)/mol·L⁻¹ |
| 0℃ | 16.56 | 1.37×10˜5 | 9.098% | 1.507×10⁻² |
| 10℃ | 15.16 | 1.57×10˜5 | 10.18% | 1.543×10⁻² |
| 20℃ | 13.63 | 1.71×10~5 | 11.2% | 1.527×10⁻² |
 的电离平衡向
的电离平衡向a.电离常数 b.电离程度 c.c(OH⁻) d.
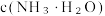
②表中c(OH-))基本不变的原因是
③常温下,在氨水中加入少量的氯化铵晶体,下列说法错误的是
a.溶液的pH增大 b.
 减小 c.
减小 c.  减小
减小
您最近一年使用:0次
名校
3 . 回答下列问题:
(1)关于甲、乙、丙、丁四套装置的说法正确的是_______ 。

(2)以下物质(或粒子)与其用途之间关联正确的是_______ 。
(3)实验室制取Cl2的化学方程式:_______ 。浓盐酸表现的性质是_______ 。
(4)已知:在稀硫酸中,MnO 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。_______
(1)关于甲、乙、丙、丁四套装置的说法正确的是

| A.用装置甲制取氯气 | B.用丙装置可以较长时间看到白色Fe(OH)2白色沉淀 |
| C.用丁装置证明碳酸氢钠受热易分解 | D.用装置乙除去氢气中的少量氯化氢 |
| A.硬铝——制导线 | B.14C——测定文物年代 |
| C.锗——作半导体材料 | D.Ti-Fe合金——作不锈钢材料 |
(4)已知:在稀硫酸中,MnO
 与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
与H2O2也能发生以下反应:2KMnO4+3H2O2+3H2SO4=K2SO4+2MnSO4+5O2↑+8H2O。由上述反应得出物质氧化性强弱的结论是_______>_______(填化学式)。
您最近一年使用:0次
2023-09-24更新
|
325次组卷
|
4卷引用:天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题
天津市宁河区芦台第一中学2022-2023学年高一上学期期末考试化学试题(已下线)专题07 铁及其化合物 金属材料-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)(已下线)专项02 氧化还原反应的概念、规律及综合应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(天津专用)山西运城盐湖五中2023-2024学年高一上学期化学期末练兵卷(三)
名校
解题方法
4 . 我国化学家侯德榜发明了联合制碱法,为世界制碱工业做出了巨大贡献。联合制碱法的主要过程如图所示(部分物质已略去)。
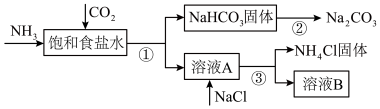
(1)饱和食盐水中通二氧化碳和氨气的化学方程式是_______
(2)下列说法中合理的是_______(填标号)。
(3)一场突如其来的新冠肺炎疫情,给人们的生活带来了巨大的冲击,在疫情期间外出需戴好口罩,返家后立即杀菌消毒。双氧水和84消毒液是日常生活常用的消毒剂,二氧化氯 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。
①某同学设计如下实验研究 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是_______ (填序号)
②某届奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种原因可能是 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
_______  (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为_______ mol。
③ 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式_______ ,将 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式_______ 。

(1)饱和食盐水中通二氧化碳和氨气的化学方程式是
(2)下列说法中合理的是_______(填标号)。
A.副产物 可用作氮肥 可用作氮肥 |
B.溶液B中的主要离子是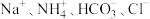 |
C.制碱流程中可回收并循环利用的物质只有碳酸氢钠分解产生的 |
| D.饱和食盐水中应该先通二氧化碳至饱和,再通入氨气至饱和 |
 气体是一种常用高效的自来水消毒剂。
气体是一种常用高效的自来水消毒剂。①某同学设计如下实验研究
 的性质,能证明
的性质,能证明 有还原性的实验是
有还原性的实验是| 序号 | 实验 | 实验现象 |
| 1 | 向 溶液中滴加酸性 溶液中滴加酸性 溶液 溶液 | a.溶液紫色裉去;b.有大量气泡产生 |
| 2 | 向 溶液中滴加淀粉碘化钾溶液 溶液中滴加淀粉碘化钾溶液 | c.溶液变蓝 |
 与
与 反应产生
反应产生 促进藻类快速生长。该反应说明氧化性:
促进藻类快速生长。该反应说明氧化性:
 (填“>”或“<”);当有
(填“>”或“<”);当有 生成时,转移电子的物质的量为
生成时,转移电子的物质的量为③
 和浓盐酸在一定温度下反应会生成
和浓盐酸在一定温度下反应会生成 和
和 ,该反应的离子方程式
,该反应的离子方程式 通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
通入到硫化氢溶液中,然后加入少量的稀盐酸酸化的氯化钡溶液,发现有白色沉淀生成,写出二氧化氯与硫化氢溶液反应的化学方程式
您最近一年使用:0次
2023-01-07更新
|
492次组卷
|
3卷引用:天津市第四十七中学2023-2024学年高三上学期第一次阶段性检测化学试题
名校
解题方法
5 . I.化学反应中伴随着能量变化,根据相关知识回答下列问题:
(1)下列过程吸热的是___________ (填序号)。
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为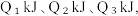 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是___________ (填序号)。
①.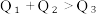 ②.
②. 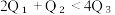 ③.
③. 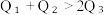 ④.
④. 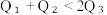
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。___________ 。
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)___________ 。
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为___________ ,___________ (填“电子”或“电流”)是由锌片经导线流向铜片。标准状况下,若反应过程中溶解了6.5g锌,则生成的氢气的体积为___________ L。
(6)某同学想利用反应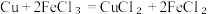 设计一个原电池请在下图
设计一个原电池请在下图___________ (共2处)标出使用的用品。
(1)下列过程吸热的是
a.生石灰溶于水 b.浓硫酸稀释 c.硝酸铵溶于水 d.铜溶于浓硝酸
e.氯化铵固体与氢氧化钡晶体混合搅拌
(2)已知H2和O2反应放热, 且断开1molH-H键、1molO=O键、1molO-H键需吸收的能量分别为
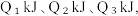 由此可以推知下列关系正确的是
由此可以推知下列关系正确的是①.
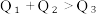 ②.
②. 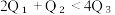 ③.
③. 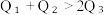 ④.
④. 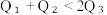
Ⅱ.某同学用导线将电流表与Zn片、Cu片相连接,插入盛有稀硫酸的烧杯中进行实验,如图所示。
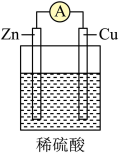
(4)从构成原电池的基本要素来看,稀硫酸的作用是(选填以下序号)
a.反应物 b.电极材料 c.离子导体 d.电子导体
(5)该原电池的负极反应式为
(6)某同学想利用反应
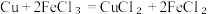 设计一个原电池请在下图
设计一个原电池请在下图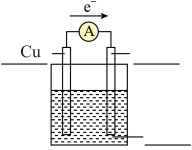
您最近一年使用:0次
6 . 硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)下列物质属于硅酸盐材料的是 。
(2) 是玻璃的主要成分之一,
是玻璃的主要成分之一, 与氢氧化钠溶液反应的化学方程为
与氢氧化钠溶液反应的化学方程为_____________ 。工艺师常用___________ (填物质名称)来雕刻玻璃。
(3)用 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作___________ 。 可由
可由 与纯碱混合高温熔融反应制得,方程式为
与纯碱混合高温熔融反应制得,方程式为____________ ,高温熔融纯碱时下列坩埚可选___________ 。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(4)工业制备硅单质方程式____________________ ,该反应中氧化剂是______________ 。
(5)根据如图所示装置回答以下问题。 ,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀
,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀 ②稀盐酸 ③碳酸钙 ④
②稀盐酸 ③碳酸钙 ④ 溶液 ⑤
溶液 ⑤ 。试剂A与C分别为
。试剂A与C分别为_____ (填序号);试管中发生反应的离子方程式为__________________ 。有同学认为此实验不能说明酸性强弱,你认为原因是_______________________ 。
(1)下列物质属于硅酸盐材料的是 。
| A.陶瓷 | B.玻璃 | C.水泥 | D.生石灰 |
(2)
 是玻璃的主要成分之一,
是玻璃的主要成分之一, 与氢氧化钠溶液反应的化学方程为
与氢氧化钠溶液反应的化学方程为(3)用
 水溶液浸泡过的棉花不易燃烧,说明
水溶液浸泡过的棉花不易燃烧,说明 可用作
可用作 可由
可由 与纯碱混合高温熔融反应制得,方程式为
与纯碱混合高温熔融反应制得,方程式为A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D.铁坩埚
(4)工业制备硅单质方程式
(5)根据如图所示装置回答以下问题。

 ,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀
,从以下所给物质中选出甲同学设计的实验所用到的物质:①稀 ②稀盐酸 ③碳酸钙 ④
②稀盐酸 ③碳酸钙 ④ 溶液 ⑤
溶液 ⑤ 。试剂A与C分别为
。试剂A与C分别为
您最近一年使用:0次
7 . 根据要求填空:
(1)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的化学方程式如下:
,反应的化学方程式如下:
 .
.
①请用“单线桥法”表示上述反应中电子转移的方向和数目.(请在答题纸的方程式上作答)______________________________________________________ 。
②该反应中,______ 是氧化剂,______ 是氧化产物.
③转移3mol电子,则所产生的氮气在标准状况下的体积为______ .
(2)铁是人类较早使用的金属之一.
①鉴别 胶体和
胶体和 溶液的常用方法是
溶液的常用方法是______ .
②某研究性学习小组为测定 溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有
溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有 ,下列叙述正确的是
,下列叙述正确的是______ (填序号).
A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若紫红色退去,证明溶液中含有
C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明溶液中含有
(1)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为
还原为 ,反应的化学方程式如下:
,反应的化学方程式如下: .
.①请用“单线桥法”表示上述反应中电子转移的方向和数目.(请在答题纸的方程式上作答)
②该反应中,
③转移3mol电子,则所产生的氮气在标准状况下的体积为
(2)铁是人类较早使用的金属之一.
①鉴别
 胶体和
胶体和 溶液的常用方法是
溶液的常用方法是②某研究性学习小组为测定
 溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有
溶液腐蚀铜后所得溶液的组成,进行了如下实验:取少量待测溶液,要验证上述溶液中含有 ,下列叙述正确的是
,下列叙述正确的是A.观察溶液是否呈浅绿色
B.取适量溶液,滴入酸性高锰酸钾溶液,若紫红色退去,证明溶液中含有

C.取适量溶液,滴入氯水,再滴入KSCN溶液,若显红色,证明溶液中含有

您最近一年使用:0次
8 . 硫及其化合物在工业上有广泛的用途。回答下列问题:
(1)硫是一种黄色晶体,化学性质比较活泼,能与许多金属单质反应,硫与铜在加热条件下反应的产物为_______ 。
(2)不同价态含硫物质在一定条件下能够相互转化,标准状况下11.2 LH2S与足量SO2反应,转移的电子数为_______ ,H2S分子中化学键的类型为_______ (填 “离子键”、“极性共价键”或“非极性共价键”)。
(3)黄铁矿(FeS2)是工业上制硫酸的重要原料,在氧气中煅烧生成Fe2O3和SO2,其煅烧的化学方程式为_______ 。
(4)在实验室中,几位同学围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌。
①可以观察到的现象为_______ 。
②上述实验现象表明浓硫酸具有_______ (填字母)。
a.酸性 b.吸水性 c.脱水性 d.强氧化性
(5)二氧化硫及其在大气中发生反应后的生成物溶于水会形成酸雨。简述证明酸雨中含有硫酸根的实验操作步骤:_______ 。
(6)某工厂每天燃烧含硫质量分数为0.64%的煤100 t,如果煤中的硫全部转化为SO2,且产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量为_______ 。
(1)硫是一种黄色晶体,化学性质比较活泼,能与许多金属单质反应,硫与铜在加热条件下反应的产物为
(2)不同价态含硫物质在一定条件下能够相互转化,标准状况下11.2 LH2S与足量SO2反应,转移的电子数为
(3)黄铁矿(FeS2)是工业上制硫酸的重要原料,在氧气中煅烧生成Fe2O3和SO2,其煅烧的化学方程式为
(4)在实验室中,几位同学围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀;然后再加入适量浓硫酸,迅速搅拌。
①可以观察到的现象为
②上述实验现象表明浓硫酸具有
a.酸性 b.吸水性 c.脱水性 d.强氧化性
(5)二氧化硫及其在大气中发生反应后的生成物溶于水会形成酸雨。简述证明酸雨中含有硫酸根的实验操作步骤:
(6)某工厂每天燃烧含硫质量分数为0.64%的煤100 t,如果煤中的硫全部转化为SO2,且产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量为
您最近一年使用:0次
名校
解题方法
9 . 铁及其重要化合物的“价类二维图”如图所示。
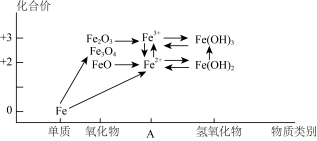
(1)该“价类二维图”中缺失的类别A应为_______ 。
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为________。
(3)要实现Fe转化为Fe3O4,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)_______ 。
(4)要实现Fe转化为Fe2+,可选用足量的_______ (填字母)
(5)为证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时最佳顺序:_______ 。
①加入适量的氯水 ②加入足量酸性KMnO4溶液 ③加入KSCN溶液
(6)氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是_______ 。

(1)该“价类二维图”中缺失的类别A应为
(2)生活中的钢铁制品如废旧铁锅,使用时间长久后若要丢弃,应归为________。
| A.干垃圾 | B.湿垃圾 | C.有毒有害垃圾 | D.可回收垃圾 |
(3)要实现Fe转化为Fe3O4,除了将Fe与氧气点燃外,另外的方法是(写出化学方程式)
(4)要实现Fe转化为Fe2+,可选用足量的
| A.稀盐酸 | B.Fe2(SO4)3溶液 | C.稀硝酸 | D.浓硫酸 |
(5)为证明某溶液中不含Fe3+而可能含有Fe2+,进行如下实验操作时最佳顺序:
①加入适量的氯水 ②加入足量酸性KMnO4溶液 ③加入KSCN溶液
| A.①③ | B.③② | C.③① | D.①②③ |
(6)氯化铁溶液中同时加入铁粉和铜粉,反应结束后烧杯底部不可能出现的是
| A.有铁无铜 | B.有铜无铁 | C.有铁有铜 | D.无铁无铜 |
您最近一年使用:0次
10 . 为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了如下实验:
(1)观察氯水颜色,发现氯水呈黄绿色,证明氯水中含有的粒子是______ 。
(2)向氯水中滴入碳酸氢钠溶液,有气体生成,说明氯水中含有的粒子是______ 。
(3)盛有氯水的试管中的有色布条褪色,说明氯水中含有的粒子是______ 。
(4)向氯水中滴加硝酸银溶液有白色沉淀生成,证明氯水中含有的粒子是______ 。
(5)氯水经光照后,颜色逐渐消失,放出的气体是______ ,溶液的酸性______ (填“增强”“不变”或“减弱”)。
(6)将氯气通入水中,所得溶液中具有氧化性的含氯微粒是______ 。
(1)观察氯水颜色,发现氯水呈黄绿色,证明氯水中含有的粒子是
(2)向氯水中滴入碳酸氢钠溶液,有气体生成,说明氯水中含有的粒子是
(3)盛有氯水的试管中的有色布条褪色,说明氯水中含有的粒子是
(4)向氯水中滴加硝酸银溶液有白色沉淀生成,证明氯水中含有的粒子是
(5)氯水经光照后,颜色逐渐消失,放出的气体是
(6)将氯气通入水中,所得溶液中具有氧化性的含氯微粒是
您最近一年使用:0次



