名校
1 . 如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:
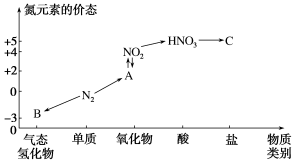
(1)写出N2的一种用途:_______ 。
(2)硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:_______ 。
(3)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为_______ 。
(4)实验室物质B的催化氧化是工业制硝酸的基础,其化学方程式为_______ 。
(5)从N元素化合价角度分析,图中涉及的六种物质只有还原性的是_______ (填化学式,下同),既有氧化性又有还原性的是_______ 。

(1)写出N2的一种用途:
(2)硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:
(3)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为
(4)实验室物质B的催化氧化是工业制硝酸的基础,其化学方程式为
(5)从N元素化合价角度分析,图中涉及的六种物质只有还原性的是
您最近一年使用:0次
2022-08-21更新
|
79次组卷
|
2卷引用:广西贺州第五高级中学2012-2022学年高一下学期第一次月考化学试题
2 . 如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:

(1)写出N2的一种用途:___ 。
(2)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为___ 。
(3)实验室制取物质B的化学方程式为____ 。
(4)NO2与水反应生成物质A的化学方程式为____ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为___ 。

(1)写出N2的一种用途:
(2)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为
(3)实验室制取物质B的化学方程式为
(4)NO2与水反应生成物质A的化学方程式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
您最近一年使用:0次
2019-12-05更新
|
594次组卷
|
6卷引用:广西壮族自治区崇左市扶绥县第二中学2019-2020学年高一上学期期末考试化学试题
广西壮族自治区崇左市扶绥县第二中学2019-2020学年高一上学期期末考试化学试题广西壮族自治区来宾市金秀县民族中学2019-2020学年高一上学期期末考试化学试题鲁科版必修一2019—2020学年第三章检测试题贵州省三穗县三中2019-2020学年高一上学期期末考试化学试题(已下线)考点16 常见非金属元素单质及其重要化合物4——氮-2020年【衔接教材·暑假作业】新高三一轮复习化学(已下线)第三单元 物质的性质与转化(基础过关)-2020-2021学年高一化学必修第一册单元测试定心卷 (鲁科版2019)
3 . 甲醇是一种可再生能源,在日常生活中有着广泛的应用.工业上用CO生产燃料甲醇,如:CO(g)+2H2(g)⇌CH3OH(g).图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化.
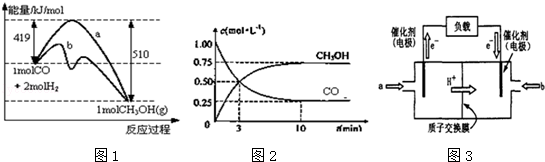
请回答下列问题:
(1)图1表示使用和未使用催化剂时反应过程和能量的对应关系.下列有关催化剂的说法不正确的是_____
(2)从反应开始到建立平衡,该过程中释放_________ kJ热量.
(3)在T2℃下,将2molCO和6molH2充入2L的密闭容器中,达到平衡状态时,测得C(CO)=0.2mol•L﹣1,则CO的转化率为_______ .
(4)如图3为常用笔记本电脑所用甲醇质子交换膜燃料电池的结构示意图如.电池总反应为2CH3OH+3O2⇌2CO2+4H2O.在电脑的使用过程中,电池的温度往往因为各种原因会升高.温度升高_____________ (填:“有利于”或“不利于”)电池将化学能转化为电能.该装置中_____ (填:“a”或“B”)为电池的负极,该电极反应式为 _________________________ .

请回答下列问题:
(1)图1表示使用和未使用催化剂时反应过程和能量的对应关系.下列有关催化剂的说法不正确的是
| A.降低分子的能量 |
| B.增加了活化分子数 |
| C.提高了活化分子百分数 |
| D.增加了单位体积内的活化分子数 |
(2)从反应开始到建立平衡,该过程中释放
(3)在T2℃下,将2molCO和6molH2充入2L的密闭容器中,达到平衡状态时,测得C(CO)=0.2mol•L﹣1,则CO的转化率为
(4)如图3为常用笔记本电脑所用甲醇质子交换膜燃料电池的结构示意图如.电池总反应为2CH3OH+3O2⇌2CO2+4H2O.在电脑的使用过程中,电池的温度往往因为各种原因会升高.温度升高
您最近一年使用:0次
2016-12-09更新
|
76次组卷
|
2卷引用:2015-2016学年广西钦州市钦南区高二上学期期中测试化学试卷
名校
4 . 回答下列问题:
(1)化学与生活、生产息息相关。
① 可用于制备纯碱; ②
可用于制备纯碱; ② 可用于葡萄酒保存;
可用于葡萄酒保存;
③ 可用于制供氧剂; ④
可用于制供氧剂; ④ 可用于制耐火材料;
可用于制耐火材料;
⑤CO可用于冶炼金属; ⑥ 可用于制硫酸;
可用于制硫酸;
⑦ 可用于制硝酸
可用于制硝酸
上述物质中,属于酸性氧化物的是______________________ (填序号)。
(2)硝酸是用途广泛的重要化工原料。氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比为___________ 。
(3)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。明胶是水溶性蛋白质混合物,溶于水形成胶体。明胶的水溶液与NaCl溶液的共同点是___________ (填序号)。
A.都可以产生丁达尔效应 B.都属于混合物 C.都能透过滤纸
(4)氮、磷都是生命元素,它们的氢化物结构相似。 的沸点
的沸点___________  的沸点(填“>”或“<”)。
的沸点(填“>”或“<”)。
(5)经研究,发现可能存在第119号元素,有人称“类纺”,其位于元素周期表第八周期ⅠA族。有关“类钫”的预测正确的是 。
(6)实验室中 溶液久置后出现浑浊,请写出发生的化学反应方程式
溶液久置后出现浑浊,请写出发生的化学反应方程式_________________________ 。
(7)氰气[ ]称为拟卤素,与
]称为拟卤素,与 结构相似、性质相近。在
结构相似、性质相近。在 中元素
中元素___________ (写元素符号)显负价。
(1)化学与生活、生产息息相关。
①
 可用于制备纯碱; ②
可用于制备纯碱; ② 可用于葡萄酒保存;
可用于葡萄酒保存;③
 可用于制供氧剂; ④
可用于制供氧剂; ④ 可用于制耐火材料;
可用于制耐火材料;⑤CO可用于冶炼金属; ⑥
 可用于制硫酸;
可用于制硫酸;⑦
 可用于制硝酸
可用于制硝酸上述物质中,属于酸性氧化物的是
(2)硝酸是用途广泛的重要化工原料。氨的催化氧化是工业合成硝酸的重要步骤,其中氧化剂与还原剂物质的量之比为
(3)央视《每周质量报告》曝光了河北省一些明胶企业将皮革废料熬制成工业明胶,出售给浙江绍兴某些制药企业,最终变成药用胶囊。明胶是水溶性蛋白质混合物,溶于水形成胶体。明胶的水溶液与NaCl溶液的共同点是
A.都可以产生丁达尔效应 B.都属于混合物 C.都能透过滤纸
(4)氮、磷都是生命元素,它们的氢化物结构相似。
 的沸点
的沸点 的沸点(填“>”或“<”)。
的沸点(填“>”或“<”)。(5)经研究,发现可能存在第119号元素,有人称“类纺”,其位于元素周期表第八周期ⅠA族。有关“类钫”的预测正确的是 。
| A.“类钫”单质具有强氧化性 | B.“类钫”单质能与冷水剧烈反应 |
| C.“类钫”最高价氧化物对应的水化物为弱碱 | D.“类钫”在化合物中显+1价 |
(6)实验室中
 溶液久置后出现浑浊,请写出发生的化学反应方程式
溶液久置后出现浑浊,请写出发生的化学反应方程式(7)氰气[
 ]称为拟卤素,与
]称为拟卤素,与 结构相似、性质相近。在
结构相似、性质相近。在 中元素
中元素
您最近一年使用:0次
名校
5 . 氧化还原反应是一类重要的反应,在工农业生产、实验室、日常生活中都有广泛的用途。
(1)广西南宁隆安县是全国知名的火龙果种植基地,火龙果富含的花肝素能够消耗活性氧,说明花青素可以作为___________ 剂(填“氧化”或“还原”)。
(2)治理汽车尾气的一种方法是在汽车的排气管上装一个催化转化装置。在催化转化器中,汽车尾气中的CO和NO在催化剂、高温条件下发生反应,生成两种无毒气体。请写出该反应的化学方程式___________ 。
(3) 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 和
和 反应的化学方程式
反应的化学方程式___________ ,其中 在该反应中
在该反应中___________ (填标号)。
A.作氧化剂B.作还原剂
C.既是氧化剂又是还原剂D.既不是氧化剂也不是还原剂
(4)《天工开物》记载“凡火药以硝石、硫磺为主,草木灰为辅……魂散惊而魄齑粉”,其中涉及的主要反应为: ,该反应过程中转移6mol电子时,产生的
,该反应过程中转移6mol电子时,产生的 在标况下体积为
在标况下体积为___________ L。
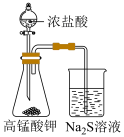
(5)实验室可以用高锰酸钾和浓盐酸反应制备氯气,请写出该反应的离子方程式:__________ 。现采用如图所示的装置探究物质氧化性强弱,若观察到右侧烧杯出现淡黄色沉淀,则说明 、
、 和S的氧化性由强到弱的顺序为:
和S的氧化性由强到弱的顺序为:___________ 。
(1)广西南宁隆安县是全国知名的火龙果种植基地,火龙果富含的花肝素能够消耗活性氧,说明花青素可以作为
(2)治理汽车尾气的一种方法是在汽车的排气管上装一个催化转化装置。在催化转化器中,汽车尾气中的CO和NO在催化剂、高温条件下发生反应,生成两种无毒气体。请写出该反应的化学方程式
(3)
 可在呼吸面具和潜水艇中作为氧气的来源,请写出
可在呼吸面具和潜水艇中作为氧气的来源,请写出 和
和 反应的化学方程式
反应的化学方程式 在该反应中
在该反应中A.作氧化剂B.作还原剂
C.既是氧化剂又是还原剂D.既不是氧化剂也不是还原剂
(4)《天工开物》记载“凡火药以硝石、硫磺为主,草木灰为辅……魂散惊而魄齑粉”,其中涉及的主要反应为:
 ,该反应过程中转移6mol电子时,产生的
,该反应过程中转移6mol电子时,产生的 在标况下体积为
在标况下体积为(5)实验室可以用高锰酸钾和浓盐酸反应制备氯气,请写出该反应的离子方程式:
 、
、 和S的氧化性由强到弱的顺序为:
和S的氧化性由强到弱的顺序为:
您最近一年使用:0次
解题方法
6 . Ⅰ.物质的分类是学习化学的一种重要方法,有下列几种物质:①盐酸;② ;③
;③ ;④
;④ 溶液;⑤
溶液;⑤ ;⑥纯碱;⑦
;⑥纯碱;⑦ 。回答下列问题:
。回答下列问题:
(1)属于碱性氧化物的是_______ (填序号),属于盐类的是_______ (填序号)。
(2)写出⑦在熔融状态下的电离方程式:_______ 。
(3)写出少量③和④反应的离子方程式:_______ 。
Ⅱ.有以下四个反应:①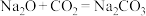 ;②
;② ;③
;③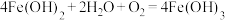 ;④
;④ 。
。
(4)属于复分解反应的是_______ (填序号,下同),既是化合反应又是氧化还原反应的是_______ 。
Ⅲ.单质到盐的转化关系可表示为:A(单质) B(氧化物)
B(氧化物) C
C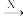 D(盐)。
D(盐)。
(5)若A是碳单质,则C的水溶液呈_______ (填“酸”“碱”或“中”)性。
(6)若B是一种淡黄色固体,X是 ,则B的用途是
,则B的用途是_______ (举一例),D的化学式可能是_______ 。
 ;③
;③ ;④
;④ 溶液;⑤
溶液;⑤ ;⑥纯碱;⑦
;⑥纯碱;⑦ 。回答下列问题:
。回答下列问题:(1)属于碱性氧化物的是
(2)写出⑦在熔融状态下的电离方程式:
(3)写出少量③和④反应的离子方程式:
Ⅱ.有以下四个反应:①
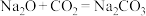 ;②
;② ;③
;③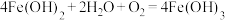 ;④
;④ 。
。(4)属于复分解反应的是
Ⅲ.单质到盐的转化关系可表示为:A(单质)
 B(氧化物)
B(氧化物) C
C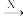 D(盐)。
D(盐)。(5)若A是碳单质,则C的水溶液呈
(6)若B是一种淡黄色固体,X是
 ,则B的用途是
,则B的用途是
您最近一年使用:0次
名校
解题方法
7 . 化学与人类生产、生活密切相关,按要求回答下列问题。
(1)铁及其化合物中,常用作红色油漆与涂料的是_______ (填化学式);具有磁性的黑色晶体是_______ (填化学式)。
(2)①“84消毒液”②高铁酸钠 ③碘酒④
③碘酒④ 酒精⑤
酒精⑤ 是人们日常生活中常用的杀菌消毒剂。上述杀菌消毒剂属于电解质的是
是人们日常生活中常用的杀菌消毒剂。上述杀菌消毒剂属于电解质的是_______ (填序号),写出②的电离方程式为_______ ,双氧水也是常用消毒剂,其电子式为_______ 。
(3)钠的化合物中,可用作潜水艇中供氧剂的是_______ (填名称),其与 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(4)印刷电路板用途广泛,电子工业中常用覆铜板为基材,利用 溶液将覆铜板上不需要的铜腐蚀,发生反应的离子方程式为
溶液将覆铜板上不需要的铜腐蚀,发生反应的离子方程式为_______ ;其氧化剂为_______ 。
(1)铁及其化合物中,常用作红色油漆与涂料的是
(2)①“84消毒液”②高铁酸钠
 ③碘酒④
③碘酒④ 酒精⑤
酒精⑤ 是人们日常生活中常用的杀菌消毒剂。上述杀菌消毒剂属于电解质的是
是人们日常生活中常用的杀菌消毒剂。上述杀菌消毒剂属于电解质的是(3)钠的化合物中,可用作潜水艇中供氧剂的是
 发生反应的化学方程式为
发生反应的化学方程式为(4)印刷电路板用途广泛,电子工业中常用覆铜板为基材,利用
 溶液将覆铜板上不需要的铜腐蚀,发生反应的离子方程式为
溶液将覆铜板上不需要的铜腐蚀,发生反应的离子方程式为
您最近一年使用:0次
2024-03-14更新
|
40次组卷
|
2卷引用:2024年广西南宁、柳州等地示范性高中高一下学期3月开学考调研测试 化学试题
名校
8 . I.生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用___________ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面___________(填字母)反应释放的热量加热食物。
II.研究含碳、氮的物质间转化的热效应,在日常生活与工业生产中均有很重要的意义。
(3)已知:H2O(l)= H2O(g) △H= +44.0kJ·mol-1,甲烷完全燃烧与不完全燃烧的热效应如下图所示。
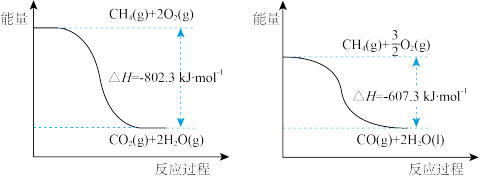
①写出表示甲烷燃烧热的热化学方程式:_____________________________ 。
②CO的燃烧热△H=_______ kJ·mol-1。
(4)以NH3、CO2为原料生产尿素[CONH2)2]的反应历程与能量变化示意图如下。
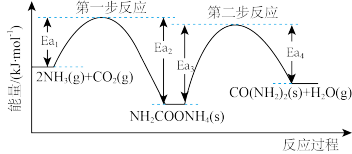
①第一步反应的热化学方程式为_______ 。
②第二步反应的△H_______ 0(填“>”、“<”或“=”)。
③从图象分析决定生产尿素的总反应的反应速率的步骤是第_______ 步反应。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面___________(填字母)反应释放的热量加热食物。
| A.生石灰和水 | B.浓硫酸和水 | C.纯碱和水 | D.食盐和白醋 |
II.研究含碳、氮的物质间转化的热效应,在日常生活与工业生产中均有很重要的意义。
(3)已知:H2O(l)= H2O(g) △H= +44.0kJ·mol-1,甲烷完全燃烧与不完全燃烧的热效应如下图所示。

①写出表示甲烷燃烧热的热化学方程式:
②CO的燃烧热△H=
(4)以NH3、CO2为原料生产尿素[CONH2)2]的反应历程与能量变化示意图如下。

①第一步反应的热化学方程式为
②第二步反应的△H
③从图象分析决定生产尿素的总反应的反应速率的步骤是第
您最近一年使用:0次
名校
9 . 一方面,磷矿藏在地球上分布不均匀且储量有限;另一方面,污水中含有较多的磷元素。因此在污水处理生物污泥中的蓝铁矿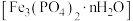 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
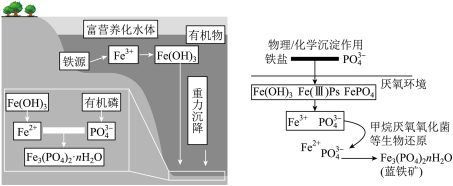
(1)水处理时,加入的高铁酸钾( )作为净水消毒剂,发生反应的化学方程式为
)作为净水消毒剂,发生反应的化学方程式为 。
。
① 中Fe的化合价为
中Fe的化合价为_______ 价,上述反应涉及的物质中属于盐的是_______ 。
②高铁酸钾可用于净水消毒的原因是_______
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:_______ 。
_______ _______
_______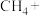 _______
_______ _______
_______ _______
_______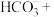 _______
_______
该反应中的氧化产物为_______ (填离子符号),被氧化的原子与被还原的原子的数目之比为_______ 。
(3)无氧条件下加热,蓝铁矿(无杂质)发生分解: ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=_______ 。
 因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。
(1)水处理时,加入的高铁酸钾(
 )作为净水消毒剂,发生反应的化学方程式为
)作为净水消毒剂,发生反应的化学方程式为 。
。①
 中Fe的化合价为
中Fe的化合价为②高铁酸钾可用于净水消毒的原因是
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:
_______
 _______
_______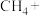 _______
_______ _______
_______ _______
_______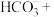 _______
_______
该反应中的氧化产物为
(3)无氧条件下加热,蓝铁矿(无杂质)发生分解:
 ,蓝铁矿的质量由5.02g减小为3.58g,则n=
,蓝铁矿的质量由5.02g减小为3.58g,则n=
您最近一年使用:0次
10 . Ⅰ.家庭厨卫用品中有许多常见的化学物质,括号内为其主要成分:
①料酒(乙醇);②食醋(乙酸);③碱面( );④小苏打(
);④小苏打( );⑤84消毒液(
);⑤84消毒液( ):⑥洁厕灵(
):⑥洁厕灵( );⑦铁锅(
);⑦铁锅( )
)
(1)乙醇的化学式为 ,属于
,属于______ (填“纯净物”或“混合物”)。
(2)用铁锅炒菜时,不宜加入过多的食醋,原因是:______ 。
(3)小苏打常用作面食的膨松剂,请用化学方程式说明原理______ 。
(4)家庭中不可将84消毒液与洁厕灵混用,否则会因产生一种有毒气体,请用离子方程式解释原因______ 。
Ⅱ.亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
(5)若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素 可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是______。
可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是______。
(6)已知 能发生如下反应:
能发生如下反应: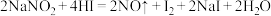 ,该反应的还原产物是
,该反应的还原产物是______ , 体现出的性质有
体现出的性质有______ 。请标出该反应的电子转移方向和数目______ 。
①料酒(乙醇);②食醋(乙酸);③碱面(
 );④小苏打(
);④小苏打( );⑤84消毒液(
);⑤84消毒液( ):⑥洁厕灵(
):⑥洁厕灵( );⑦铁锅(
);⑦铁锅( )
)(1)乙醇的化学式为
 ,属于
,属于(2)用铁锅炒菜时,不宜加入过多的食醋,原因是:
(3)小苏打常用作面食的膨松剂,请用化学方程式说明原理
(4)家庭中不可将84消毒液与洁厕灵混用,否则会因产生一种有毒气体,请用离子方程式解释原因
Ⅱ.亚硝酸钠(
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。(5)若误食亚硝酸钠会导致血红蛋白中亚铁离子转化为铁离子而中毒,服用维生素
 可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是______。
可解除亚硝酸钠的中毒,下列关于上述中毒。解毒过程的说法中,正确的是______。| A.亚硝酸钠是还原剂 | B.维生素 是氧化剂 是氧化剂 |
C.维生素 能把铁离子还原成为亚铁离子 能把铁离子还原成为亚铁离子 | D.亚硝酸钠被还原 |
 能发生如下反应:
能发生如下反应: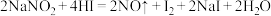 ,该反应的还原产物是
,该反应的还原产物是 体现出的性质有
体现出的性质有
您最近一年使用:0次



