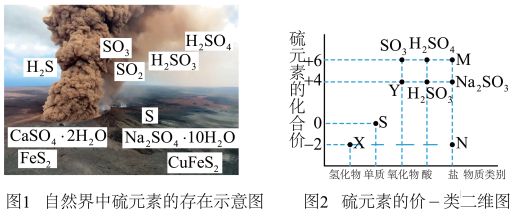
1 . 硫元素是动植物生长不可缺少的元素,图1是自然界中硫元素的存在示意图。图2是硫元素的常见化合价与部分物质类别的对应关系,回答下列问题。___________ 。
(2) 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是___________ 。
(3) 和氯水都有漂白性,有人为增强漂白效果,将
和氯水都有漂白性,有人为增强漂白效果,将 和
和 混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:
混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:___________ 。
(4)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即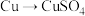
方案乙:由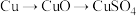
①方案甲中,铜和浓硫酸反应的化学方程式是___________ 。
②方案乙比方案甲更合理,理由是___________ 。
(5) 、NO和
、NO和 是大气初期污染物的主要成分,
是大气初期污染物的主要成分, 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图3所示。当
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图3所示。当 与NO的物质的量之比为
与NO的物质的量之比为 时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
时,与足量氨气在一定条件下发生反应,该反应的化学方程式为___________ 。
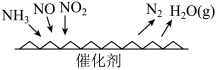
图3
(6)研究表明硝酸与金属反应时,最容易生成亚硝酸( ,弱酸),然后才转化成
,弱酸),然后才转化成 ,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸。图4为金属在不同浓度的
,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸。图4为金属在不同浓度的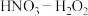 混合溶液中的溶解速率和生成
混合溶液中的溶解速率和生成 的体积V的变化示意图,请回答下列问题:
的体积V的变化示意图,请回答下列问题:
①最佳溶解金属的混合溶液中 的浓度分数为
的浓度分数为___________ 。
②过氧化氢与亚硝酸反应的化学方程式为___________ 。
(2)
 溶液易变质,实验室检验
溶液易变质,实验室检验 溶液是否变质的基本操作是
溶液是否变质的基本操作是(3)
 和氯水都有漂白性,有人为增强漂白效果,将
和氯水都有漂白性,有人为增强漂白效果,将 和
和 混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:
混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:(4)硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。甲、乙两位同学用铜和硫酸做原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
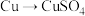
方案乙:由
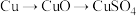
①方案甲中,铜和浓硫酸反应的化学方程式是
②方案乙比方案甲更合理,理由是
(5)
 、NO和
、NO和 是大气初期污染物的主要成分,
是大气初期污染物的主要成分, 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图3所示。当
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图3所示。当 与NO的物质的量之比为
与NO的物质的量之比为 时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
时,与足量氨气在一定条件下发生反应,该反应的化学方程式为
图3
(6)研究表明硝酸与金属反应时,最容易生成亚硝酸(
 ,弱酸),然后才转化成
,弱酸),然后才转化成 ,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸。图4为金属在不同浓度的
,如果溶液中存在更强的氧化剂,如过氧化氢,它完全有能力将新产生的亚硝酸再氧化成硝酸。图4为金属在不同浓度的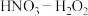 混合溶液中的溶解速率和生成
混合溶液中的溶解速率和生成 的体积V的变化示意图,请回答下列问题:
的体积V的变化示意图,请回答下列问题: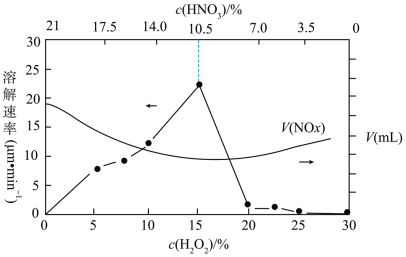
①最佳溶解金属的混合溶液中
 的浓度分数为
的浓度分数为②过氧化氢与亚硝酸反应的化学方程式为
您最近一年使用:0次
2 . 在人们高度重视环境和保护环境的今天,消除和利用氮氧化物、碳氧化物、硫氧化物对改善大气质量具有重要的意义。
(1)氮氧化物是造成光化学污染的罪魁祸首,用一氧化碳还原氮氧化物,可防止氮氧化物污染,如反应:
 。
。
已知:i.碳的燃烧热为
ii.
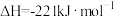
iii.

则

___________ 。
(2)已知:
 。将1mol CO和
。将1mol CO和 充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
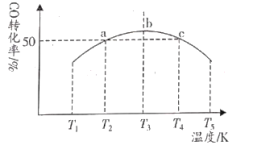
①
___________ 0(填“>”或“<”)。
②能否根据a点CO的转化率为50%求算反应 的平衡常数K:
的平衡常数K:___________ (填“能”或“不能”),理由是___________ 。
③已知c点时容器内的压强为p,在 温度下该反应的压强平衡常数
温度下该反应的压强平衡常数 为
为___________ (用含p的关系式表示)。( 为以分压表示的平衡常数,分压=总压×物质的量分数)
为以分压表示的平衡常数,分压=总压×物质的量分数)
(3)在绝热的某刚性容器中置入 和
和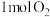 ,发生反应:
,发生反应:
 。下列说法中能够判断该反应一定处于平衡状态的有
。下列说法中能够判断该反应一定处于平衡状态的有___________ (填数字序号)。
①容器中 、
、 、
、 共存
共存
②单位时间内生成 的同时消耗
的同时消耗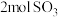
③ 与
与 浓度之比恒定不变
浓度之比恒定不变
④容器中温度恒定不变
⑤容器中 、
、 、
、 的物质的量之比为2∶1∶2
的物质的量之比为2∶1∶2
⑥反应容器中压强不随时间变化
(1)氮氧化物是造成光化学污染的罪魁祸首,用一氧化碳还原氮氧化物,可防止氮氧化物污染,如反应:

 。
。已知:i.碳的燃烧热为

ii.

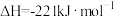
iii.


则


(2)已知:

 。将1mol CO和
。将1mol CO和 充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
充入1L恒容密闭容器中,在一定条件下发生反应,相同时间内测得CO的转化率与温度的对应关系如图所示:
①

②能否根据a点CO的转化率为50%求算反应
 的平衡常数K:
的平衡常数K:③已知c点时容器内的压强为p,在
 温度下该反应的压强平衡常数
温度下该反应的压强平衡常数 为
为 为以分压表示的平衡常数,分压=总压×物质的量分数)
为以分压表示的平衡常数,分压=总压×物质的量分数)(3)在绝热的某刚性容器中置入
 和
和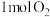 ,发生反应:
,发生反应:
 。下列说法中能够判断该反应一定处于平衡状态的有
。下列说法中能够判断该反应一定处于平衡状态的有①容器中
 、
、 、
、 共存
共存②单位时间内生成
 的同时消耗
的同时消耗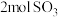
③
 与
与 浓度之比恒定不变
浓度之比恒定不变④容器中温度恒定不变
⑤容器中
 、
、 、
、 的物质的量之比为2∶1∶2
的物质的量之比为2∶1∶2⑥反应容器中压强不随时间变化
您最近一年使用:0次
2021-10-20更新
|
705次组卷
|
3卷引用:广西河池市高级中学2021-2022学年高三上学期第一次月考化学试题
3 . 某同学做同主族元素性质相似性、递变性实验时,自己设计了一套实验方案,并记录了有关实验现象(见下表,表中的“实验方案”与“实验现象”前后不一定是对应关系)。
请你帮助该同学整理并完成实验报告。
(1)实验目的:________________ 。
(2)实验用品:
①实验试剂:金属钠、金属钾、新制氯水、溴水、0.1mol·L-1溴化钠溶液、0.1 mol·L-1碘化钠溶液、四氯化碳。
②实验仪器:________ 、________ 、________ 、镊子、小刀、玻璃片等。
(3)实验内容(填写与实验方案对应的实验现象的标号和化学方程式):
(4)实验结论:____________________ 。
实验步骤 | 实验现象 |
| ①将氯水滴加到NaBr溶液中,振荡后再加入适量CCl4,振荡,静置 | A、浮在水面上,熔成小球,不定向移动,随之消失 |
| ②将一小块金属钠放入到冷水中 | B、分层,上层无色,下层紫红色 |
| ③将溴水滴加到NaI溶液中,振荡后再加入适量 CCl4,振荡,静置 | C、浮在水面上,熔成小球,不定向移动,并伴有轻微的爆炸声,很快消失 |
| ④将一小块金属钾放入冷水中 | D、分层,上层无色,下层棕红色 |
(1)实验目的:
(2)实验用品:
①实验试剂:金属钠、金属钾、新制氯水、溴水、0.1mol·L-1溴化钠溶液、0.1 mol·L-1碘化钠溶液、四氯化碳。
②实验仪器:
(3)实验内容(填写与实验方案对应的实验现象的标号和化学方程式):
| 实验方案 | 实验现象 | 化学方程式 |
| ① | ||
| ② | ||
| ③ | ||
| ④ |
您最近一年使用:0次
2019-04-24更新
|
84次组卷
|
2卷引用:广西靖西市第二中学2019-2020学年高二下学期开学考试化学试题
4 . 人们认识和应用物质常从两方面入手,一是从物质的类别认识该物质可能跟哪些物质发生反应;二是从物质所含元素的化合价分析该物质是否具有氧化性或还原性。
(1)下图1是硫元素的各个价态与物质类别的对应关系:
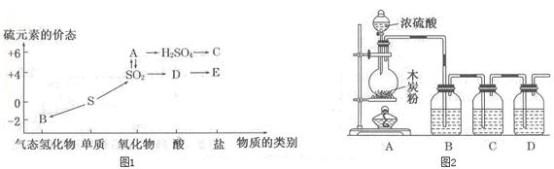
①写出指定物质的化学式:A___________ ,B___________ 。
②写出SO2转化为A的化学反应方程式:_______________________________________ 。
(2)为认识浓硫酸的强氧化性,老师在B、C、D试剂瓶中依次分装酸性KMnO4溶液、品红溶液、澄清石灰水,进行图2所示的实验。
①写出A中发生的化学反应方程式:_______________________________________________ 。
②C试剂瓶中品红溶液的作用:_____________________________ 。。
③老师提醒同学们,如果B、D顺序对调,即使澄清石灰水变浑浊也不能说明木炭已被氧化成CO2其原因是________________________________________________ (用化学方程式表示)
④下列实验中能证明某气体为SO2的是___
a.使澄清石灰水变浑浊
b.使湿润的蓝色石蕊试纸变红
c.使品红溶液褪色
d.通入足量NaOH溶液中,再滴加BaCl2溶液,有白色沉淀生成,该沉淀溶于稀盐酸
e.通入氯水中,能使氯水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生
(1)下图1是硫元素的各个价态与物质类别的对应关系:

①写出指定物质的化学式:A
②写出SO2转化为A的化学反应方程式:
(2)为认识浓硫酸的强氧化性,老师在B、C、D试剂瓶中依次分装酸性KMnO4溶液、品红溶液、澄清石灰水,进行图2所示的实验。
①写出A中发生的化学反应方程式:
②C试剂瓶中品红溶液的作用:
③老师提醒同学们,如果B、D顺序对调,即使澄清石灰水变浑浊也不能说明木炭已被氧化成CO2其原因是
④下列实验中能证明某气体为SO2的是
a.使澄清石灰水变浑浊
b.使湿润的蓝色石蕊试纸变红
c.使品红溶液褪色
d.通入足量NaOH溶液中,再滴加BaCl2溶液,有白色沉淀生成,该沉淀溶于稀盐酸
e.通入氯水中,能使氯水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生
您最近一年使用:0次
名校
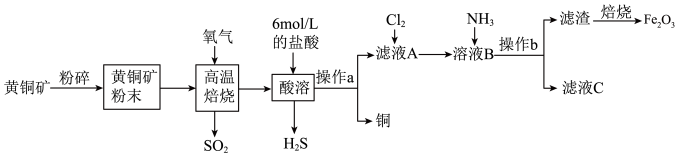
5 . Cu和Fe2O3在工农业生产中用途广泛,用黄铜矿(主要成分为CuFeS2,其中Cu为+2价,Fe为+2价)制取Cu和Fe2O3的工艺流程如图所示:__________ 。
(2)CuFeS2中S元素的化合价是______ ,高温焙烧时生成FeS及另外两种产物,则发生的化学反应方程式为____________ 。
(3)操作a为____________ 。
(4)向滤液A中通入Cl2的目的是__________ 。
(5)向溶液B中通入NH3发生反应的离子方程式为___________ 。
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O
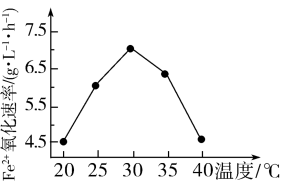
由下图可知,使用硫杆菌的最佳温度为______ ℃,若反应温度过高,反应速率下降,其原因是_______________ 。
(2)CuFeS2中S元素的化合价是
(3)操作a为
(4)向滤液A中通入Cl2的目的是
(5)向溶液B中通入NH3发生反应的离子方程式为
(6)工业上用生物法处理H2S的原理为(硫杆菌作催化剂):H2S+Fe2(SO4)3=S↓+2FeSO4+H2SO4
4FeSO4+O2+2H2SO4
 2Fe2(SO4)3+2H2O
2Fe2(SO4)3+2H2O由下图可知,使用硫杆菌的最佳温度为
您最近一年使用:0次
名校
解题方法
6 . 离子液体被认为是21世纪最有希望的绿色溶液和功能材料之一,在诸多领域的用途已被研究开发。有几种离子液体由原子序数依次增大的短周期主族元素X、Y、Z、W、R、Q组成。请回答:
(1)基态Z原子的价电子排布式为________ ,基态Y原子占据最高能级的电子云轮廓图为________ 形。
(2)下列说法正确的是____。
(3)试解释 分子中X-W-X键角比
分子中X-W-X键角比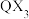 分子中X-Q-X键角大的原因
分子中X-Q-X键角大的原因________ 。
(4)化合物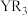 水解生成
水解生成 【也可写作
【也可写作 ,结构如图1】和
,结构如图1】和 。
。
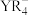 中Y原子的杂化方式为
中Y原子的杂化方式为________ , 晶体中含有
晶体中含有________  氢键。当
氢键。当 溶于水,
溶于水, 分子与水中
分子与水中 结合形成配位键,Y原子杂化方式由
结合形成配位键,Y原子杂化方式由 杂化变为
杂化变为 杂化,请用离子方程式解释
杂化,请用离子方程式解释 为一元弱酸原因
为一元弱酸原因________ 。 ,该晶体密度表达式为
,该晶体密度表达式为________  (YW的摩尔质量为
(YW的摩尔质量为 )。
)。
| 元素 | 元素性质或原子结构 |
| X | 电子只有一种自旋取向 |
| Y | 2p能级上有1个电子 |
| Z | 有6个不同运动状态的电子 |
| W | 2p轨道处于半充满状态,简单氢化物易液化,可用作制冷剂 |
| R | 仅有一个未成对电子,简单阴离子含10个电子 |
| Q | 与W位于同一主族 |
(1)基态Z原子的价电子排布式为
(2)下列说法正确的是____。
| A.氢化物的沸点:R>Z | B.分子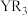 的空间构型为平面三角形 的空间构型为平面三角形 |
| C.元素的电负性:R>X>Z | D.最高价含氧酸的酸性:W>Q |
(3)试解释
 分子中X-W-X键角比
分子中X-W-X键角比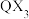 分子中X-Q-X键角大的原因
分子中X-Q-X键角大的原因(4)化合物
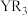 水解生成
水解生成 【也可写作
【也可写作 ,结构如图1】和
,结构如图1】和 。
。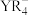 中Y原子的杂化方式为
中Y原子的杂化方式为 晶体中含有
晶体中含有 氢键。当
氢键。当 溶于水,
溶于水, 分子与水中
分子与水中 结合形成配位键,Y原子杂化方式由
结合形成配位键,Y原子杂化方式由 杂化变为
杂化变为 杂化,请用离子方程式解释
杂化,请用离子方程式解释 为一元弱酸原因
为一元弱酸原因 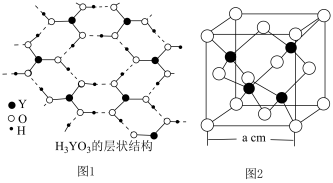
 ,该晶体密度表达式为
,该晶体密度表达式为 (YW的摩尔质量为
(YW的摩尔质量为 )。
)。
您最近一年使用:0次
名校
解题方法
7 . 焦亚硫酸钠( )在化学工业中用途广泛。其一种制备流程如下:
)在化学工业中用途广泛。其一种制备流程如下:
(1) 分子中,中心原子价层电子对数为
分子中,中心原子价层电子对数为__________ 。
(2)“ 制备”所用实验装置(夹持仪器已省略)如下图:
制备”所用实验装置(夹持仪器已省略)如下图:__________ 。
②饱和碳酸氢钠溶液的作用是__________ 。
③三颈烧瓶中生成 反应的化学方程式为
反应的化学方程式为__________ ( 为沉淀物)。
为沉淀物)。
(3)“ 制备”反应过程分四步:
制备”反应过程分四步:
步骤Ⅰ.在碳酸钠溶液中通入 至pH为4.1,生成
至pH为4.1,生成 溶液;
溶液;
步骤Ⅱ.停止通 ,向
,向 溶液中再加入
溶液中再加入 溶液调至pH为7~8,转化为
溶液调至pH为7~8,转化为 ;
;
步骤Ⅲ.继续通入 ,至pH达4.1,又生成
,至pH达4.1,又生成 溶液;
溶液;
步骤Ⅳ.当溶液中 含量达到过饱和浓度时析出
含量达到过饱和浓度时析出 。
。
①步骤Ⅰ测量溶液的pH=4.1所用仪器是__________ 。
②写出步骤Ⅱ中反应的离子方程式:__________ 。
③写出Ⅰ~Ⅳ步骤中总反应的化学方程式:__________ 。
 )在化学工业中用途广泛。其一种制备流程如下:
)在化学工业中用途广泛。其一种制备流程如下:
(1)
 分子中,中心原子价层电子对数为
分子中,中心原子价层电子对数为(2)“
 制备”所用实验装置(夹持仪器已省略)如下图:
制备”所用实验装置(夹持仪器已省略)如下图: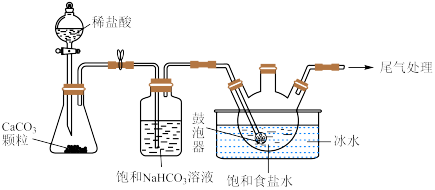
②饱和碳酸氢钠溶液的作用是
③三颈烧瓶中生成
 反应的化学方程式为
反应的化学方程式为 为沉淀物)。
为沉淀物)。(3)“
 制备”反应过程分四步:
制备”反应过程分四步:步骤Ⅰ.在碳酸钠溶液中通入
 至pH为4.1,生成
至pH为4.1,生成 溶液;
溶液;步骤Ⅱ.停止通
 ,向
,向 溶液中再加入
溶液中再加入 溶液调至pH为7~8,转化为
溶液调至pH为7~8,转化为 ;
;步骤Ⅲ.继续通入
 ,至pH达4.1,又生成
,至pH达4.1,又生成 溶液;
溶液;步骤Ⅳ.当溶液中
 含量达到过饱和浓度时析出
含量达到过饱和浓度时析出 。
。①步骤Ⅰ测量溶液的pH=4.1所用仪器是
②写出步骤Ⅱ中反应的离子方程式:
③写出Ⅰ~Ⅳ步骤中总反应的化学方程式:
您最近一年使用:0次
2024-03-30更新
|
292次组卷
|
5卷引用:广西壮族自治区部分学校2023-2024学年高三下学期教学质量监测联考(二模)化学试题
名校
解题方法
8 . Ⅰ.工业生产纯碱的工艺流程示意图如图:
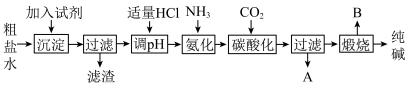
(1)为除去粗盐水中的
 、
、 、
、 等杂质离子,加入试剂顺序合理的是______。
等杂质离子,加入试剂顺序合理的是______。| A.碳酸钠、氢氧化钠、氯化钡 | B.碳酸钠、氯化钡、氢氧化钠 |
| C.氢氧化钠、碳酸钠、氯化钡 | D.氯化钡、氢氧化钠、碳酸钠 |
(2)工业生产纯碱工艺流程中,碳酸化时产生的现象是
(3)工业生产纯碱工艺流程中,先“氨化”后“碳酸化”的目的是
(4)碳酸化后过滤,滤液A最主要的成分是
Ⅱ.纯碱在生产生活中有广泛的用途。
(5)工业上,可用纯碱代替烧碱生产某些化工产品。如用饱和纯碱溶液与氯气反应可制得有效成分为次氯酸钠的消毒液,其反应的离子方程式为
您最近一年使用:0次
名校
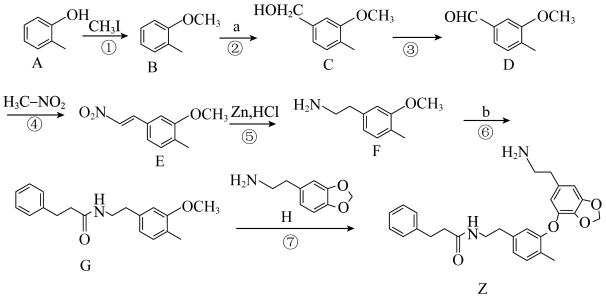
9 . 千金藤素常用于防治肿瘤病患者白细胞减少症、抗疟疾、调节免疫功能等,制备其关键中间体(Ⅰ)的一种合成路线如下:
(1)化合物A的名称为___________ ,碳原子的杂化方式为___________ 。
(2)反应②是原子利用率100%的反应,写出化合物a的一种用途___________ 。
(3)化合物C中含有的官能团名称为___________ ,请写出C转化为D的化学方程式___________ ,反应类型为___________ 。
(4)b能与碳酸氢钠溶液反应生成气体。芳香化合物X为b的同分异构体,能发生水解反应又能发生银镜反应,核磁共振氢谱中4组峰的面积之比为6∶2∶1∶1,X的结构简式为___________ (写出一种)。
(5)参照上述路线,以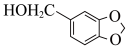 与流程中某些试剂为原料(其他无机试剂任选),合成流程中的H,请写出合成路线图
与流程中某些试剂为原料(其他无机试剂任选),合成流程中的H,请写出合成路线图_______ 。
(1)化合物A的名称为
(2)反应②是原子利用率100%的反应,写出化合物a的一种用途
(3)化合物C中含有的官能团名称为
(4)b能与碳酸氢钠溶液反应生成气体。芳香化合物X为b的同分异构体,能发生水解反应又能发生银镜反应,核磁共振氢谱中4组峰的面积之比为6∶2∶1∶1,X的结构简式为
(5)参照上述路线,以
 与流程中某些试剂为原料(其他无机试剂任选),合成流程中的H,请写出合成路线图
与流程中某些试剂为原料(其他无机试剂任选),合成流程中的H,请写出合成路线图
您最近一年使用:0次
名校
解题方法
10 . 以含钴废料(主要成分为 ,含有少量
,含有少量 、
、 、
、 )为原料制备
)为原料制备 的流程如图所示:
的流程如图所示:_____________ 。“滤渣1”的化学式为___________ 。
(2)“酸浸”时 与
与 反应的化学方程式为
反应的化学方程式为__________________ 。如果用浓盐酸代替硫酸和 的混液,也可实现Co元素价态的转化,但弊端是
的混液,也可实现Co元素价态的转化,但弊端是______________________ (任答一点)。
(3)“操作2”所得副产品的一种用途为_____________ 。
(4)“沉钴”时温度不能太高,原因是_____________________________ 。
(5)“沉钴”步骤中同时还会产生 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为_________________ 。
(6)实验室模拟“操作1”,需要将 转移到
转移到________ (填仪器名称)中加热分解,得到 。
。
 ,含有少量
,含有少量 、
、 、
、 )为原料制备
)为原料制备 的流程如图所示:
的流程如图所示: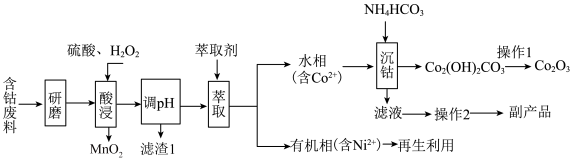
(2)“酸浸”时
 与
与 反应的化学方程式为
反应的化学方程式为 的混液,也可实现Co元素价态的转化,但弊端是
的混液,也可实现Co元素价态的转化,但弊端是(3)“操作2”所得副产品的一种用途为
(4)“沉钴”时温度不能太高,原因是
(5)“沉钴”步骤中同时还会产生
 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为(6)实验室模拟“操作1”,需要将
 转移到
转移到 。
。
您最近一年使用:0次



