解题方法
1 . 在一烧杯中盛有 和
和 的混合物2.36g,先向其中加入过量稀硫酸使其完全溶解,再逐滴加入
的混合物2.36g,先向其中加入过量稀硫酸使其完全溶解,再逐滴加入 溶液,产生沉淀的质量与加入
溶液,产生沉淀的质量与加入 溶液的质量关系如图所示:
溶液的质量关系如图所示:
(1)图中OA段发生反应的化学方程式为___________ 。
(2)图中B点所示溶液的溶质为___________ (填化学式)。
(3)该 溶液的溶质质量分数为
溶液的溶质质量分数为___________ 。
(4)混合物中 和
和 的质量比为
的质量比为___________ (填最简整数比)。
 和
和 的混合物2.36g,先向其中加入过量稀硫酸使其完全溶解,再逐滴加入
的混合物2.36g,先向其中加入过量稀硫酸使其完全溶解,再逐滴加入 溶液,产生沉淀的质量与加入
溶液,产生沉淀的质量与加入 溶液的质量关系如图所示:
溶液的质量关系如图所示: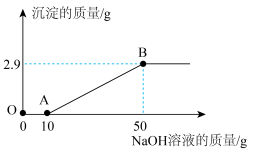
(1)图中OA段发生反应的化学方程式为
(2)图中B点所示溶液的溶质为
(3)该
 溶液的溶质质量分数为
溶液的溶质质量分数为(4)混合物中
 和
和 的质量比为
的质量比为
您最近一年使用:0次
名校
解题方法
2 . 某实验小组用氯酸钾和二氧化锰为原料制取氧气,在试管中加入少量二氧化锰和适量氯酸钾,反应过程中测量的有关数据记录如下:
(1)反应到___________ min时,氯酸钾就完全分解。
(2)计算反应前氯酸钾的质量是多少?__________ (写出解题步骤)
| 反应时间(min) | 0 | 1 | 2 | 3 | 4 |
| 试管中固体质量(g) | 14.25 | 12.65 | 11.05 | 9.45 | 9.45 |
(2)计算反应前氯酸钾的质量是多少?
您最近一年使用:0次
解题方法
3 . 甲乙两同学分别取A、B两份等物质的量浓度的NaOH溶液各10mL,分别向A、B溶液中通入不等量的CO2,充分反应后再继续向两溶液中逐滴加入0.5 盐酸,生气体的物质的量与所加盐酸的体积的关系如图所示,请回答下列问题:
盐酸,生气体的物质的量与所加盐酸的体积的关系如图所示,请回答下列问题:___________ (填“离子”或“共价”化合物;CO2的电子式为___________
(2)a点对应的溶液中溶质为___________ (填化学式)。
(3)ab段反应的离子方程式为___________ ;忽略溶液混合造成的体积变化,b点NaCl的物质的量浓度为___________  ;d点生成的CO2的总体积为
;d点生成的CO2的总体积为___________ mL(换算成标准状况)。
(4)原NaOH溶液的物质的量浓度为___________  。
。
 盐酸,生气体的物质的量与所加盐酸的体积的关系如图所示,请回答下列问题:
盐酸,生气体的物质的量与所加盐酸的体积的关系如图所示,请回答下列问题: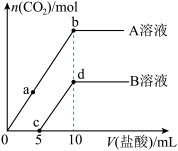
(2)a点对应的溶液中溶质为
(3)ab段反应的离子方程式为
 ;d点生成的CO2的总体积为
;d点生成的CO2的总体积为(4)原NaOH溶液的物质的量浓度为
 。
。
您最近一年使用:0次
4 . 请回答下列问题:
(1)已知:二元酸 的电离方程式是:
的电离方程式是: ,
, ,若
,若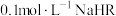 溶液的
溶液的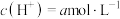 ,则
,则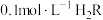 溶液中
溶液中
_______  (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。
(2)室温下,电离平衡常数是衡量弱电解质电离程度的物理量,请依据下表完成填空。
①等浓度的 、
、 和
和 溶液,pH由大到小的顺序为
溶液,pH由大到小的顺序为_______ (用化学式表示)。
②常温下,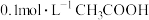 溶液加水稀释过程中,下列表达式的数据变大的是
溶液加水稀释过程中,下列表达式的数据变大的是_______ 。
A. B.
B. C.
C. D.
D. E.
E.
③25℃时,若测得 与
与 的混合溶液的
的混合溶液的 ,则溶液中
,则溶液中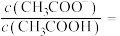
_______ 。
(3)①25℃时, 电离常数
电离常数 ,
, 的溶度积常数
的溶度积常数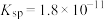 ,在某
,在某 溶液中加入一定量的某浓度的氨水后,测得混合液
溶液中加入一定量的某浓度的氨水后,测得混合液 ,计算此温度下残留在溶液中的
,计算此温度下残留在溶液中的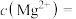
_______ 。
②常温下将 氨水与
氨水与 的盐酸等体积混合,所得溶液呈中性,则氨水的电离常数
的盐酸等体积混合,所得溶液呈中性,则氨水的电离常数
_______ (用含a的式子表示,忽略混合过程中溶液体积的变化,保留两位有效数字)。
③常温下,将 的弱酸HA溶液与
的弱酸HA溶液与 的
的 溶液等体积混合后
溶液等体积混合后 ,则依据三大守恒
,则依据三大守恒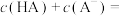
_______  ,
,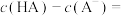
_______  (列式即可)。
(列式即可)。
④当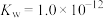 时,将
时,将 的
的 溶液aL与
溶液aL与 的
的 溶液bL混合,若所得混合液
溶液bL混合,若所得混合液 ,则
,则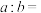
_______ 。
(1)已知:二元酸
 的电离方程式是:
的电离方程式是: ,
, ,若
,若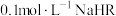 溶液的
溶液的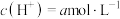 ,则
,则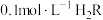 溶液中
溶液中
 (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。(2)室温下,电离平衡常数是衡量弱电解质电离程度的物理量,请依据下表完成填空。
| 化学式 |  |  |  |
| 电离常数(25℃) | 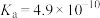 |  |   |
 、
、 和
和 溶液,pH由大到小的顺序为
溶液,pH由大到小的顺序为②常温下,
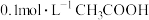 溶液加水稀释过程中,下列表达式的数据变大的是
溶液加水稀释过程中,下列表达式的数据变大的是A.
 B.
B. C.
C. D.
D. E.
E.
③25℃时,若测得
 与
与 的混合溶液的
的混合溶液的 ,则溶液中
,则溶液中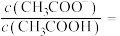
(3)①25℃时,
 电离常数
电离常数 ,
, 的溶度积常数
的溶度积常数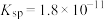 ,在某
,在某 溶液中加入一定量的某浓度的氨水后,测得混合液
溶液中加入一定量的某浓度的氨水后,测得混合液 ,计算此温度下残留在溶液中的
,计算此温度下残留在溶液中的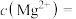
②常温下将
 氨水与
氨水与 的盐酸等体积混合,所得溶液呈中性,则氨水的电离常数
的盐酸等体积混合,所得溶液呈中性,则氨水的电离常数
③常温下,将
 的弱酸HA溶液与
的弱酸HA溶液与 的
的 溶液等体积混合后
溶液等体积混合后 ,则依据三大守恒
,则依据三大守恒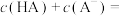
 ,
,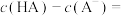
 (列式即可)。
(列式即可)。④当
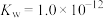 时,将
时,将 的
的 溶液aL与
溶液aL与 的
的 溶液bL混合,若所得混合液
溶液bL混合,若所得混合液 ,则
,则
您最近一年使用:0次
名校
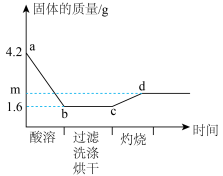
5 . 取一定量铜粉、铁粉的混合物,加入过量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗净、烘干后在足量氧气中充分灼烧(金属元素在产物中显+2价)。固体质量与各步实验的时间关系如图。_______ 。
(2)原粉状混合物中铁粉的质量为_________ 克。
(3)求m的值_______ 。(写出计算过程)
(2)原粉状混合物中铁粉的质量为
(3)求m的值
您最近一年使用:0次
6 . 将12.8 g Cu投入50 mL某浓度的浓硝酸中,随着Cu的不断减少,反应生成气体的颜色逐渐变浅(假设硝酸对应的还原产物只有 和NO),当Cu全部溶解时,硝酸恰好完全消耗,共收集到气体3.36L(标准状况),参加反应的硝酸的物质的量为
和NO),当Cu全部溶解时,硝酸恰好完全消耗,共收集到气体3.36L(标准状况),参加反应的硝酸的物质的量为____ ,相同条件下,NO和 的体积比
的体积比___ ,要想使溶液中的 完全沉淀,至少需要滴加2 mol·L
完全沉淀,至少需要滴加2 mol·L 的NaOH溶液
的NaOH溶液___ mL。
 和NO),当Cu全部溶解时,硝酸恰好完全消耗,共收集到气体3.36L(标准状况),参加反应的硝酸的物质的量为
和NO),当Cu全部溶解时,硝酸恰好完全消耗,共收集到气体3.36L(标准状况),参加反应的硝酸的物质的量为 的体积比
的体积比 完全沉淀,至少需要滴加2 mol·L
完全沉淀,至少需要滴加2 mol·L 的NaOH溶液
的NaOH溶液
您最近一年使用:0次
7 . 计算
(1)在25℃时,Ksp(AgBr)=c(Ag+)•c(Br﹣)=1.0×10﹣12,若取0.188g的AgBr(相对分子质量188)固体放入100mL水中(忽略溶液体积的变化),则溶液中Br﹣的物质的量浓度为_______ 。
(2)在某温度下,重水(D2O)的离子积常数为1×10﹣12.若用pH一样的定义来规定pD值,则pD=﹣lg{C(D+)},1L溶有0.01mol的NaOD的D2O溶液,其pD=_______ 。
(3)在定容容器内加入一定量A(g),发生反应2A(g)⇌B(g)+xC(g),在一定条件下从开始达到平衡后,压强增大了p%时,A的转化率也为p%,则x的值为_______ 。
(4)已知在25℃时,醋酸的Ka=1.75×10﹣5.在此温度下,0.2moL/L醋酸与0.1mol/L NaOH溶液等体积混合后,溶液显_______ 性,此溶液中离子浓度大到小的顺序是_______ 。
(1)在25℃时,Ksp(AgBr)=c(Ag+)•c(Br﹣)=1.0×10﹣12,若取0.188g的AgBr(相对分子质量188)固体放入100mL水中(忽略溶液体积的变化),则溶液中Br﹣的物质的量浓度为
(2)在某温度下,重水(D2O)的离子积常数为1×10﹣12.若用pH一样的定义来规定pD值,则pD=﹣lg{C(D+)},1L溶有0.01mol的NaOD的D2O溶液,其pD=
(3)在定容容器内加入一定量A(g),发生反应2A(g)⇌B(g)+xC(g),在一定条件下从开始达到平衡后,压强增大了p%时,A的转化率也为p%,则x的值为
(4)已知在25℃时,醋酸的Ka=1.75×10﹣5.在此温度下,0.2moL/L醋酸与0.1mol/L NaOH溶液等体积混合后,溶液显
您最近一年使用:0次
8 . 物质的量是贯穿整个高中化学计算的核心物理量。请按要求填空:
(1)下列物质在标准状况下的体积从大到小的顺序为_______ (填序号)。
①16gO2 ②标准状况下 8.96LCO2 ③18gH2O ④含有 1. 806×1023个H原子的NH3
(2)标准状况下,16.4g由CO2与O2组成的混合气体的总体积为8. 96 L,该混合气体中O2的体积分数为_____ 。
(3)等质量的CO2和SO2的分子个数比为_________ ,同温同压下,等体积的N2和O2的密度比为_________ 。
(4)40 g某三价金属的硫酸盐中含有0.3 mol ,则此硫酸盐的摩尔质量为
,则此硫酸盐的摩尔质量为__________ 。
(5)将标准状况下VLHCl溶于1L水中,形成ρg·cm-3的溶液,则所得溶液中溶质的物质的量浓度为______ (用含V、ρ的代数式表示,不用化简)mol/L。
(1)下列物质在标准状况下的体积从大到小的顺序为
①16gO2 ②标准状况下 8.96LCO2 ③18gH2O ④含有 1. 806×1023个H原子的NH3
(2)标准状况下,16.4g由CO2与O2组成的混合气体的总体积为8. 96 L,该混合气体中O2的体积分数为
(3)等质量的CO2和SO2的分子个数比为
(4)40 g某三价金属的硫酸盐中含有0.3 mol
 ,则此硫酸盐的摩尔质量为
,则此硫酸盐的摩尔质量为(5)将标准状况下VLHCl溶于1L水中,形成ρg·cm-3的溶液,则所得溶液中溶质的物质的量浓度为
您最近一年使用:0次
2024高三·江苏·专题练习
9 . 测定Na2S2O8样品的纯度:称取0.2500g样品,用蒸馏水溶解,加入20.00mL0.4000mol/LFeSO4溶液(过量),加热,再加入20.00mL硫磷混合酸,滴入二苯胺磺酸钠指示剂5~6滴,用0.1000mol/LK2Cr2O7标准溶液滴定过量的FeSO4至溶液呈紫色(终点),消耗K2Cr2O7标准溶液10.00mL。计算Na2S2O8样品的纯度_____ (写出计算过程)。
您最近一年使用:0次
解题方法
10 . 设 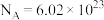 表示阿伏加德罗常数的值,请回答下列问题:
表示阿伏加德罗常数的值,请回答下列问题:
(1)O2的摩尔质量为________ g/mol。
(2)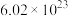 个 Na+约含有
个 Na+约含有________ mol Na⁺,其质量为________ g。
(3)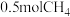 约含有
约含有________ 个 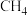 ,其标准状况的气体体积
,其标准状况的气体体积________ L。
(4)0.2molAl含有________ 个铝原子,质量是________ g。
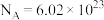 表示阿伏加德罗常数的值,请回答下列问题:
表示阿伏加德罗常数的值,请回答下列问题:(1)O2的摩尔质量为
(2)
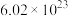 个 Na+约含有
个 Na+约含有(3)
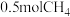 约含有
约含有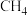 ,其标准状况的气体体积
,其标准状况的气体体积(4)0.2molAl含有
您最近一年使用:0次



