1 . 钒是我国丰产元素,储量占全球11%,居第四位。在光纤通讯系统中,光纤将信息导入离光源lkm外的用户就需用5片钒酸钇晶体(钇是第39号元素)。我国福州是全球钒酸钇晶体主要供应地,每年出口几十万片钒酸钇晶体,年创汇近千万美元(1999年)。钒酸钇是四方晶体,晶胞参数a=712pm, c= 629pm,密度d=4.22g/cm3,含钒25%,求钒酸钇的化学式以及在一个晶胞中有几个原子。给出计算过程。钒酸钛的化学式:_____ 一个晶胞中的原子数:_____ 计算过程:_____ 。
您最近一年使用:0次
2 . 目前家用小型制氧机大多以变压吸附方式工作,其原理是以空气为原料,在加压时吸附剂将空气中大部分氮气吸附,氧气和未被吸附的少量氮气被收集起来,得到富氧空气。被吸附的氮气在减压条件下通过尾气管排至大气。某小型家用常压制氧机的标称参数为额定功率100W,输出富氧空气中氧气浓度91%(体积分数),输出富氧空气流量为1.8L·min-1,工作温度为25%℃。以空气进气量10mol为对象,计算达到分离效果所需要的最小能量以及该家用制氧机的能量效率_______ 、______ 。空气由体积分数为20%的氧气和80%的氮气组成,排出的尾气中只有氮气。所有气体均视作理想气体。
您最近一年使用:0次
3 . 铁卟啉(FeP)是细胞色素(P-450)的活性中心,具有将各种氧供体的氧原子活化并转移至底物的能力。研究人员为模拟活体内的加氧酶催化β-胡萝卜素(P)分解为维生素A(VA)的反应,以FeP为催化剂、间氯过氧化苯甲酸(CPBA)为氧化剂,研究了β-胡萝卜素的分解反应动力学。研究中FeP和CPBA的浓度可视为不变。无论是否存在催化剂FeP,该分解反应对一胡萝卜素均为一级反应。
已知:若y=ax+b,则出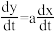 。式中,a,b均为与t无关的常数。
。式中,a,b均为与t无关的常数。
实验A:在无FeP情况下,β-胡萝卜素-间氯过氧化苯甲酸反应体系(β-CPBA)的反应机理1如下(其中β*CPBA为反应中间物,CBA为间氯苯甲酸):
(i)β+CPBA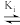 β*CPBA平衡
β*CPBA平衡
(ii)β*CPBA VA+CBA
VA+CBA
实验B.以FeP为催化剂,β-胡萝卜素-间氯过氧化苯甲酸——啉反应体系(β-CPBA-FeP)的反应机理2如下(其中FeOP*CBA、β*FeOP*CBA、β*CPBA为反应中间物):
(iii)FeP+CPBA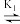 FeOP*CBA(快速平衡)
FeOP*CBA(快速平衡)
(iv)FeOP*CBA+β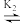 β*FeOP*CBA(快速平衡)
β*FeOP*CBA(快速平衡)
(v)β*FeOP*CBA VA+FeP+CBA
VA+FeP+CBA
(vi)β+CPBA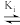 β*CPBA(快速平衡)
β*CPBA(快速平衡)
(vi)β*CPBA VA+CBA
VA+CBA
对该体系的实验结果进行曲线拟合,可得下表数据( 为反应的表观速率常数);
为反应的表观速率常数);
(1)对β-CBPA体系,根据实验测得的表观速率常数 (293.2K)=4.795×10-4s-1,
(293.2K)=4.795×10-4s-1, (301.2K)=8.285×10-4s-1,求反应的表观活化能
(301.2K)=8.285×10-4s-1,求反应的表观活化能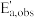
_____ 。
(2)根据反应机理2推导 与[β]间关系的速率方程
与[β]间关系的速率方程______ ,并给出 的表达式
的表达式________ 。
(3)已知β-CPBA-FeP体系反应的表观活化能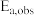 =47.07kJ·mol-1和机理2中(v)步的活化能Ea,1=42.43kJ·mol-1,计算(vii)步的活化能Ea,2
=47.07kJ·mol-1和机理2中(v)步的活化能Ea,1=42.43kJ·mol-1,计算(vii)步的活化能Ea,2___________ 。
(4)分别根据以下条件,说明β-CPBA和β-CPBA-FeP中哪一个体系反应更为有利。
①Ea,1与Ea,2的结果及题中所给其他数据_______ 。
②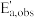 与
与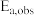 的结果及题中所给其他数据
的结果及题中所给其他数据________ 。
实验C.在金属卟啉催化氧化反应体系中加入一些含氮小分子,会加速反成。为揭示反应机理,研究了FeP与咪唑类(Im)含氮小分子的配位反应热力学。
FeP+2lm⇌FePlm2(1)
实验测得反应(1)的标准平衡常数 见下表。
见下表。
(5)请根据上表中293.2K和301.2K的平衡常数计算反应(1)的 =
=_____ ,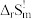 =
=_____ 。已知2730~400K间 =0。
=0。
(6)用上表中所给数据和(5)的计算结果分别解释温度对反应(1)的影响______ 、________ 。
(7)已知在一定温度下反应方向会发生变化,请计算反应的转向温度_________ 。
已知:若y=ax+b,则出
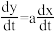 。式中,a,b均为与t无关的常数。
。式中,a,b均为与t无关的常数。实验A:在无FeP情况下,β-胡萝卜素-间氯过氧化苯甲酸反应体系(β-CPBA)的反应机理1如下(其中β*CPBA为反应中间物,CBA为间氯苯甲酸):
(i)β+CPBA
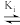 β*CPBA平衡
β*CPBA平衡(ii)β*CPBA
 VA+CBA
VA+CBA实验B.以FeP为催化剂,β-胡萝卜素-间氯过氧化苯甲酸——啉反应体系(β-CPBA-FeP)的反应机理2如下(其中FeOP*CBA、β*FeOP*CBA、β*CPBA为反应中间物):
(iii)FeP+CPBA
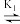 FeOP*CBA(快速平衡)
FeOP*CBA(快速平衡)(iv)FeOP*CBA+β
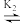 β*FeOP*CBA(快速平衡)
β*FeOP*CBA(快速平衡)(v)β*FeOP*CBA
 VA+FeP+CBA
VA+FeP+CBA(vi)β+CPBA
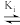 β*CPBA(快速平衡)
β*CPBA(快速平衡)(vi)β*CPBA
 VA+CBA
VA+CBA对该体系的实验结果进行曲线拟合,可得下表数据(
 为反应的表观速率常数);
为反应的表观速率常数);| T/K | k1/s-1 | k1/s-1 |  /s-1 /s-1 |
| 293.2 301.2 | 4.869×10-3 7.731×10-3 | 1.350×10-4 2.398×10-4 | 5.865×10-4 9.795×10-4 |
 (293.2K)=4.795×10-4s-1,
(293.2K)=4.795×10-4s-1, (301.2K)=8.285×10-4s-1,求反应的表观活化能
(301.2K)=8.285×10-4s-1,求反应的表观活化能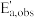
(2)根据反应机理2推导
 与[β]间关系的速率方程
与[β]间关系的速率方程 的表达式
的表达式(3)已知β-CPBA-FeP体系反应的表观活化能
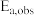 =47.07kJ·mol-1和机理2中(v)步的活化能Ea,1=42.43kJ·mol-1,计算(vii)步的活化能Ea,2
=47.07kJ·mol-1和机理2中(v)步的活化能Ea,1=42.43kJ·mol-1,计算(vii)步的活化能Ea,2(4)分别根据以下条件,说明β-CPBA和β-CPBA-FeP中哪一个体系反应更为有利。
①Ea,1与Ea,2的结果及题中所给其他数据
②
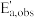 与
与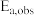 的结果及题中所给其他数据
的结果及题中所给其他数据实验C.在金属卟啉催化氧化反应体系中加入一些含氮小分子,会加速反成。为揭示反应机理,研究了FeP与咪唑类(Im)含氮小分子的配位反应热力学。
FeP+2lm⇌FePlm2(1)
实验测得反应(1)的标准平衡常数
 见下表。
见下表。| T/K | 293.2 | 297.2 | 301.2 | 305.2 |
 | 2.775×105 | 1.012×105 | 4.080×104 | 1.458×104 |
 =
=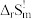 =
= =0。
=0。(6)用上表中所给数据和(5)的计算结果分别解释温度对反应(1)的影响
(7)已知在一定温度下反应方向会发生变化,请计算反应的转向温度
您最近一年使用:0次
4 . 将1mol水在100 ℃, 101.3 kPa下全部蒸发为水蒸气,再沿着p/V=a (常数)的可逆过程压缩,终态压力为152.0kPa.设水蒸气为理想气体,在此过程温度范围内,它的摩尔等压热容Cpm=33.20Jmol-1K-1.水的气化热为40.66J ·mol-1 (假设-定温度范围内水的气化热不变)。
(1)计算整个过程终态的热力学温度T2___________ 。
(2)通过计算,判断终态时体系中是否存在液态水,若存在,液态水的量是多少___________ 。
(3)计算整个过程发生后,体系的焓变 ΔH___________ 。
(4)若整个过程的熵变为132.5JK-1,推算可逆过程的熵变ΔS___________ 。
(1)计算整个过程终态的热力学温度T2
(2)通过计算,判断终态时体系中是否存在液态水,若存在,液态水的量是多少
(3)计算整个过程发生后,体系的焓变 ΔH
(4)若整个过程的熵变为132.5JK-1,推算可逆过程的熵变ΔS
您最近一年使用:0次
5 . 某酸碱催化反应(E和S是反应物,P是产物)机理如下:

K1=1.0 ×107 mol-1 dm3s-1, k2=1.0 ×102 mol-1 dm3s-1, pKa=5.0, 反应决速步骤为中间物HES*和ES*之生成。
(1)推导表观反应速率常数kexp的表达式___________ ,式中只能含有基元反应的速率常数k1和k2以及氢离子浓度[H+]和E的电离平衡常数Ka。
(2)推断上述反应属于酸催化还是碱催化。若控制此反应缓慢进行,通过计算,判断pH在什么范围___________ ,kexp基本不随pH发生变化 (在1%以内)。

K1=1.0 ×107 mol-1 dm3s-1, k2=1.0 ×102 mol-1 dm3s-1, pKa=5.0, 反应决速步骤为中间物HES*和ES*之生成。
(1)推导表观反应速率常数kexp的表达式
(2)推断上述反应属于酸催化还是碱催化。若控制此反应缓慢进行,通过计算,判断pH在什么范围
您最近一年使用:0次
6 . 某铅合金中含有Pb, Bi, Ni等元素,称取此合金试样2.420g,用HNO3溶解并定容至250mL。移取50.00 mL上述试液于250mL锥形瓶中,调节pH=1,以二甲酚橙为指示剂,用0.07500 mol·L-1 EDTA标准溶液滴定,消耗5.25mL。然后,用六次甲基四胺缓冲溶液将pH调至5,再以上述EDTA标准溶液滴定,消耗28.76 mL。加入邻二氨菲,置换出镍配合物中的EDTA, 用0.04500 mol ·L-1Pb(NO3)2标准溶液滴定置换出的EDTA,消耗8.76mL。计算此合金试样中Pb, Bi, Ni的质量分数________ 。(lgKBiY= 27.94, lgKPbY = 18.04, IgKNiY = 18.62)
您最近一年使用:0次
7 . X是金属M的碱式碳酸盐,不含结晶水。称取质量相等的样品两份,分别进行处理:一份在H2中充分处理(反应1),收集得0.994g水,剩余残渣为金属M的单质,重2.356g;另一份则在CO中处理(反应2),完全反应后得到1.245LCO2(101.325kPa,0°C),剩余残渣和反应1完全相同。
(1)通过计算,推出X的化学式______ 。
(2)写出X分别和H2、CO反应的方程式______ (要求系数为最简整数比)
(1)通过计算,推出X的化学式
(2)写出X分别和H2、CO反应的方程式
您最近一年使用:0次
2011高三·全国·竞赛
8 . NO2和N2O4混合气体的针管实验是高中化学的经典素材。理论估算和实测发现,混合气体体积由V压缩为V/2,温度由298K升至311K。已知这两个温度下N2O4(g) 2NO2(g)的压力平衡常数Kp分别为0.141和0.363。
2NO2(g)的压力平衡常数Kp分别为0.141和0.363。
(1)通过计算回答,混合气体经上述压缩后,NO2的浓度比压缩前增加了_______ 倍。
(2)动力学实验证明,上述混合气体几微秒内即可达成化学平衡。压缩后的混合气体在室温下放置,颜色如何变化?____________ 为什么?_______________
 2NO2(g)的压力平衡常数Kp分别为0.141和0.363。
2NO2(g)的压力平衡常数Kp分别为0.141和0.363。(1)通过计算回答,混合气体经上述压缩后,NO2的浓度比压缩前增加了
(2)动力学实验证明,上述混合气体几微秒内即可达成化学平衡。压缩后的混合气体在室温下放置,颜色如何变化?
您最近一年使用:0次



