解题方法
1 . 某研究小组用工业钛白副产品为原料制备纳米级电池材料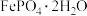 ,按如下流程开展实验。
,按如下流程开展实验。 ,含少量的
,含少量的 、
、 、
、 等杂质。
等杂质。
②已知 和
和 的氧化性随酸性的增强而增强。
的氧化性随酸性的增强而增强。
请回答:
(1)常温下步骤Ⅰ所得料液其pH___________ 7(填“>”、“<”)。
(2)下列说法不正确 的是___________。
(3)步骤Ⅴ中Mn元素的去除率及滤液中Mn元素含量随着溶液pH值的关系如图1所示,___________ 。
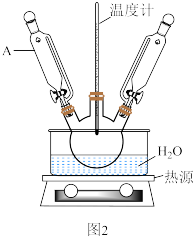
(4)步骤Ⅵ操作之一采用如图2所示装置进行(忽略夹持装置),仪器A的名称是___________ ;该操作不宜用酒精灯直接加热的原因是___________ 。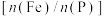 是衡量磷酸铁品质最关键的指标。
是衡量磷酸铁品质最关键的指标。
Fe元素的定量测定:①配制一系列pH=3~5, 浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺(
浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺( )溶液,调pH=3~5,加入邻菲罗啉。③进行比色
)溶液,调pH=3~5,加入邻菲罗啉。③进行比色
①通过比色能获得Fe元素浓度的原理是___________ 。
②测得产品中铁磷比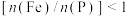 ,可能原因是
,可能原因是___________ 。
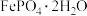 ,按如下流程开展实验。
,按如下流程开展实验。
 ,含少量的
,含少量的 、
、 、
、 等杂质。
等杂质。②已知
 和
和 的氧化性随酸性的增强而增强。
的氧化性随酸性的增强而增强。请回答:
(1)常温下步骤Ⅰ所得料液其pH
(2)下列说法
| A.步骤Ⅱ,加入Fe粉的目的是调节溶液pH值,以便Ti元素水解沉淀 |
B.步骤Ⅲ,加入 的目的是除去Mg元素 的目的是除去Mg元素 |
| C.为了提高实验效率,可以将Ⅱ、Ⅲ、Ⅴ的过滤操作合并 |
D.步骤Ⅳ中过量的 可在步骤Ⅴ中被氧化去除 可在步骤Ⅴ中被氧化去除 |
(3)步骤Ⅴ中Mn元素的去除率及滤液中Mn元素含量随着溶液pH值的关系如图1所示,
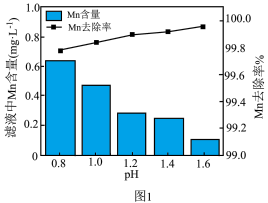
(4)步骤Ⅵ操作之一采用如图2所示装置进行(忽略夹持装置),仪器A的名称是
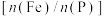 是衡量磷酸铁品质最关键的指标。
是衡量磷酸铁品质最关键的指标。Fe元素的定量测定:①配制一系列pH=3~5,
 浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺(
浓度由低到高的与邻菲罗啉的橙红色络合物的标准液。②称取一定量产品,用适量盐酸溶解,再加入足量的盐酸羟胺( )溶液,调pH=3~5,加入邻菲罗啉。③进行比色
)溶液,调pH=3~5,加入邻菲罗啉。③进行比色①通过比色能获得Fe元素浓度的原理是
②测得产品中铁磷比
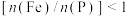 ,可能原因是
,可能原因是
您最近一年使用:0次
解题方法
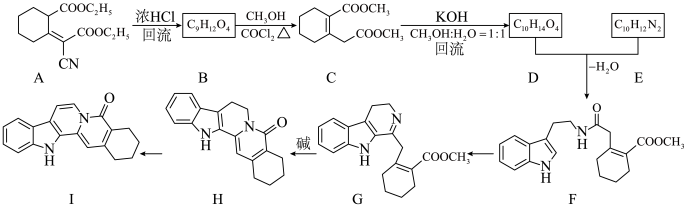
2 . 化合物Ⅰ具有良好的降血压、减肥以及治疗心脏疾病等功效,其合成路线如下(部分反应条件省略)
(1)化合物A的非全碳 官能团名称是___________ 。
(2)下列说法不正确 的是___________。
(3)化合物E的结构简式是___________ 。
(4)写出G→H的化学方程式___________ 。
(5)写出同时符合下列条件的化合物C的一种同分异构体的结构简式___________ 。
①分子中含有苯环且与 溶液发生显色反应
溶液发生显色反应
②核磁共振氢谱和红外光谱检测表明:分子中共有4种不同化学环境的氢原子,不含 键
键
(6)写出以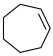 、
、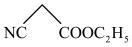 以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。___________
已知:①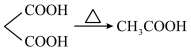
②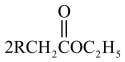
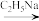
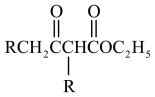
③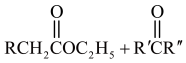

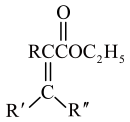
(1)化合物A的
(2)下列说法
| A.A→B的转变只是官能团种类和数量的变化 |
B.在B→C的反应中, 作催化剂 作催化剂 |
C.化合物G的分子式为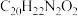 |
| D.化合物I可在酸性或碱性条件下发生水解反应 |
(3)化合物E的结构简式是
(4)写出G→H的化学方程式
(5)写出同时符合下列条件的化合物C的一种同分异构体的结构简式
①分子中含有苯环且与
 溶液发生显色反应
溶液发生显色反应②核磁共振氢谱和红外光谱检测表明:分子中共有4种不同化学环境的氢原子,不含
 键
键(6)写出以
 、
、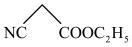 以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
以及乙醇为原料制备化合物A的合成路线图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
您最近一年使用:0次
3 . 以锗石矿A(化学式为 )为原料,可以实现如下转化。
)为原料,可以实现如下转化。
请回答:
(1)D的化学式为___________ ,液体E的沸点___________  (填“高于”或“低于”)。
(填“高于”或“低于”)。
(2)下列说法不正确 的是___________。
(3)已知液体E以物质的量之比1∶1与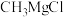 反应,该反应可用来构建
反应,该反应可用来构建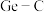 键,写出步骤Ⅲ的化学方程式
键,写出步骤Ⅲ的化学方程式___________ 。
(4)写出溶液G中所有的阴离子___________ ,设计实验证明溶液G中含有Cu元素___________ 。
 )为原料,可以实现如下转化。
)为原料,可以实现如下转化。
请回答:
(1)D的化学式为
 (填“高于”或“低于”)。
(填“高于”或“低于”)。(2)下列说法
| A.气体B是形成酸雨的成分之一 | B.固体C中可能含有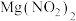 |
C. 也能与浓盐酸反应 也能与浓盐酸反应 | D.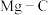 键强于 键强于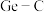 键 键 |
(3)已知液体E以物质的量之比1∶1与
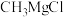 反应,该反应可用来构建
反应,该反应可用来构建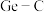 键,写出步骤Ⅲ的化学方程式
键,写出步骤Ⅲ的化学方程式(4)写出溶液G中所有的阴离子
您最近一年使用:0次
4 . S8与NH3在无水条件下反应,得到一种二元化合物A,元素分析可知,A中含S元素69.60%。A进行如下反应:
(1)A、B、C、D的化学式分别为___________ 、___________ 、___________ 、___________ 。
(2)A与SnCl2的乙醇溶液反应除生成B外,还生成一种含Sn(IV)化合物,试写出A→B的化学方程式___________ 。
(3)D与一种无色液体(该液体是由常见的红棕色气体在加压下形成的)互为等电子体,但D与无色液体的几何构型完全不同,为环状结构,试画出D的最稳定的Lewis结构式___________ ,理由是___________ ,该Lewis结构式中,S原子的电子构型是___________ 。

(1)A、B、C、D的化学式分别为
(2)A与SnCl2的乙醇溶液反应除生成B外,还生成一种含Sn(IV)化合物,试写出A→B的化学方程式
(3)D与一种无色液体(该液体是由常见的红棕色气体在加压下形成的)互为等电子体,但D与无色液体的几何构型完全不同,为环状结构,试画出D的最稳定的Lewis结构式
您最近一年使用:0次
名校
解题方法
5 . 石墨和金刚石均属于碳的同素异形体,物理性质相差很大,归根结底是晶体结构不同造成的。已知石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如下图所示,图中用虚线标出了石墨的一个六方晶胞。___________ 。
(2)已知石墨的层间距为334.8 pm,C-C键长为142 pm,计算石墨晶体的密度为___________ (单位:g·cm-3)。
(3)石墨可用作锂离子电池的负极材料,充电时发生下述反应:Li1-xC6+x Li++x e-→ LiC6 其结果是,Li+嵌入石墨的A、B层间,导致石墨的层堆积方式发生改变,形成化学式为LiC6的嵌入化合物。
Ⅰ.下图给出了一个Li+沿C轴投影在A层上的位置,试在下图上标出与该离子临近的其他6个Li+的投影位置___________ 。
Ⅱ.在LiC6中,Li+与相邻石墨六元环的作用力属于何种键型___________ ?
Ⅲ.某石墨嵌入化合物每个六元环都对应一个Li+,写出它的化学式___________ 。
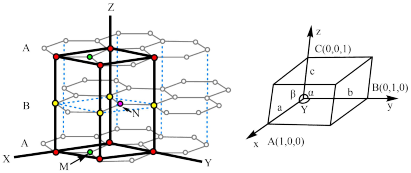
(2)已知石墨的层间距为334.8 pm,C-C键长为142 pm,计算石墨晶体的密度为
(3)石墨可用作锂离子电池的负极材料,充电时发生下述反应:Li1-xC6+x Li++x e-→ LiC6 其结果是,Li+嵌入石墨的A、B层间,导致石墨的层堆积方式发生改变,形成化学式为LiC6的嵌入化合物。
Ⅰ.下图给出了一个Li+沿C轴投影在A层上的位置,试在下图上标出与该离子临近的其他6个Li+的投影位置
Ⅱ.在LiC6中,Li+与相邻石墨六元环的作用力属于何种键型
Ⅲ.某石墨嵌入化合物每个六元环都对应一个Li+,写出它的化学式
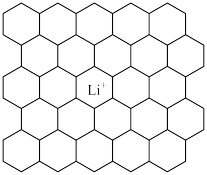
您最近一年使用:0次
6 . 利用1-甲基萘(1-MN)制备四氢萘类物质(MTLs,包括1-MTL和5-MTL)。反应过程中伴有生成十氢萘(1-MD)的副反应,涉及反应如图:
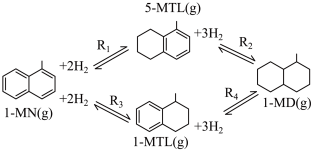
回答下列问题:
(1)1-甲基萘(1-MN)的组成元素电负性由小到大的顺序为___________ 。
(2)已知一定条件下反应 、
、 、
、 的焓变分别为
的焓变分别为 、
、 、
、 ,则反应
,则反应 的焓变为
的焓变为___________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(3)四个平衡体系的平衡常数与温度的关系如图甲所示。
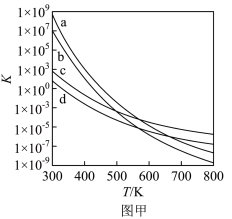
①c、d分别为反应 和
和 的平衡常数随温度变化的曲线,则表示反应
的平衡常数随温度变化的曲线,则表示反应 的平衡常数随温度变化曲线为
的平衡常数随温度变化曲线为___________ 。
②已知反应 的速率方程
的速率方程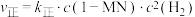 ,
,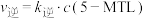 (
( 、
、 分别为正、逆反应速率常数,只与温度、催化剂有关)。温度
分别为正、逆反应速率常数,只与温度、催化剂有关)。温度 下反应达到平衡时
下反应达到平衡时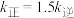 ,温度
,温度 下反应达到平衡时
下反应达到平衡时 。由此推知,
。由此推知,
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③下列说法不正确的是___________ (填标号)。
A.四个反应均为放热反应
B.反应体系中1-MD最稳定
C.压强越大,温度越低越有利于生成四氢萘类物质
D.由上述信息可知,400K时反应 速率最快
速率最快
(4)1-MN在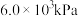 的高压
的高压 氛围下反应(
氛围下反应( 压强近似等于总压)。不同温度下达平衡时各产物的选择性
压强近似等于总压)。不同温度下达平衡时各产物的选择性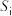 (某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数
(某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数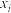 (
(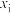 表示物种i与除
表示物种i与除 外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应
外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应 的平衡常数
的平衡常数
___________  (列出计算式)。
(列出计算式)。

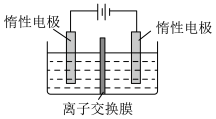
(5)利用膜电解技术(装置如图所示),以 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: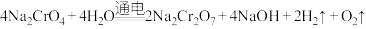 。则
。则 在
在___________ (填“阴”或“阳”)极室制得,电解时通过膜的离子主要为___________ 。

回答下列问题:
(1)1-甲基萘(1-MN)的组成元素电负性由小到大的顺序为
(2)已知一定条件下反应
 、
、 、
、 的焓变分别为
的焓变分别为 、
、 、
、 ,则反应
,则反应 的焓变为
的焓变为 、
、 、
、 的代数式表示)。
的代数式表示)。(3)四个平衡体系的平衡常数与温度的关系如图甲所示。

①c、d分别为反应
 和
和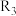 的平衡常数随温度变化的曲线,则表示反应
的平衡常数随温度变化的曲线,则表示反应 的平衡常数随温度变化曲线为
的平衡常数随温度变化曲线为②已知反应
 的速率方程
的速率方程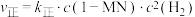 ,
,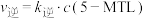 (
( 、
、 分别为正、逆反应速率常数,只与温度、催化剂有关)。温度
分别为正、逆反应速率常数,只与温度、催化剂有关)。温度 下反应达到平衡时
下反应达到平衡时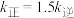 ,温度
,温度 下反应达到平衡时
下反应达到平衡时 。由此推知,
。由此推知,
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③下列说法不正确的是
A.四个反应均为放热反应
B.反应体系中1-MD最稳定
C.压强越大,温度越低越有利于生成四氢萘类物质
D.由上述信息可知,400K时反应
 速率最快
速率最快(4)1-MN在
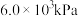 的高压
的高压 氛围下反应(
氛围下反应( 压强近似等于总压)。不同温度下达平衡时各产物的选择性
压强近似等于总压)。不同温度下达平衡时各产物的选择性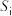 (某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数
(某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数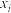 (
(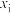 表示物种i与除
表示物种i与除 外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应
外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图乙所示,y为65%时反应 的平衡常数
的平衡常数
 (列出计算式)。
(列出计算式)。
(5)利用膜电解技术(装置如图所示),以
 为主要原料制备
为主要原料制备 的总反应方程式为:
的总反应方程式为: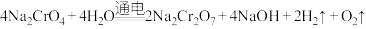 。则
。则 在
在
您最近一年使用:0次
7 . MAX相是-大类具有层状结构的金属碳化物或氮化物的总称,其中M为Ti、V、Nb等前过渡金属,X为碳或氮,A为Al、Sn、Ge、Sb等p区元素。MAX的结构中,M原子形成理想的密置层,M层之间采取密堆积(可连续分布)与简单六方堆积(通常以单层呈现)按一定方式有序堆叠形成三维结构。结构中,X填充在M层密堆积形成的所有八面体空隙中,A则有序占据M层简单六方堆积所形成空隙的一半,将其中的A元素选择性除去,可以分离得到二维的层状结构,称为MXene.MXene层中,最外层M可进一步与卤素、羟基等-1价端基T按1:1结合,形成端基T功能化的MXene(T-MXene)。因此,MXene的组成和结构多样且可调控,是当前二维材料的研究热点。
(1)若MAX相中,M和A的原子数比为n,写出MAX相(O)、二维MXene层(P)和T-MXene(Q)的组成通式。Q中T为-1价端基_____ 。
(2)某碳化物MAX相TI_AI,C结构属六方晶系,Ti层的排列方式为ABCCBAABCCBA。
①写出TixAlyCz晶胞的组成_____ 。
②已知TixAlyCz晶胞参数a=0.306nm,c=1.856nm。将M层密堆积形成的八面体近似为正八面体,计算简单六方排布相邻层的间距d(单位:m)_____ 。
③TixAlyCz结构中,碳原子处在Ti密堆积形成的八面体中心。若将晶胞原点选在处于堆积中B层的Ti上,此时所有的Al恰好均处在c轴上。写出晶胞中所有碳原子的坐标参数_____ 。
④将TixAlyCz在HF溶液中超声处理,可选择性去除其中的Al层,得到二维结构的MXene片层TixCx(反应1),TixCx进一步步与F-反应,形成F-MXene(反应2)。写出反应1和2的化学方程式_____ 。
⑤T-MXene的性质与端基T密切相关。利用熔融ZnCl2与TixAlyCz在550°C反应5h,可以得到Cl为端基的CI-MXene(反应3)。将Cl-MXene在CsCI-KCl-LiCl混合熔盐与Li2Se反应18h,可以得到端基为Se的Se-MXene(反应4)。写出反应3和4的化学方程式_____ 。
⑥对于6-2-4中用HF水溶液处理得到的F-MXene,能否发生与6-2-5中反应4类似的反应?简述原因_____ 。
生命体中,各种物质的结构和功能都与基础化学密切相关。磷脂和蛋白质就是其中的重要代表。
(1)若MAX相中,M和A的原子数比为n,写出MAX相(O)、二维MXene层(P)和T-MXene(Q)的组成通式。Q中T为-1价端基
(2)某碳化物MAX相TI_AI,C结构属六方晶系,Ti层的排列方式为ABCCBAABCCBA。
①写出TixAlyCz晶胞的组成
②已知TixAlyCz晶胞参数a=0.306nm,c=1.856nm。将M层密堆积形成的八面体近似为正八面体,计算简单六方排布相邻层的间距d(单位:m)
③TixAlyCz结构中,碳原子处在Ti密堆积形成的八面体中心。若将晶胞原点选在处于堆积中B层的Ti上,此时所有的Al恰好均处在c轴上。写出晶胞中所有碳原子的坐标参数
④将TixAlyCz在HF溶液中超声处理,可选择性去除其中的Al层,得到二维结构的MXene片层TixCx(反应1),TixCx进一步步与F-反应,形成F-MXene(反应2)。写出反应1和2的化学方程式
⑤T-MXene的性质与端基T密切相关。利用熔融ZnCl2与TixAlyCz在550°C反应5h,可以得到Cl为端基的CI-MXene(反应3)。将Cl-MXene在CsCI-KCl-LiCl混合熔盐与Li2Se反应18h,可以得到端基为Se的Se-MXene(反应4)。写出反应3和4的化学方程式
⑥对于6-2-4中用HF水溶液处理得到的F-MXene,能否发生与6-2-5中反应4类似的反应?简述原因
生命体中,各种物质的结构和功能都与基础化学密切相关。磷脂和蛋白质就是其中的重要代表。
您最近一年使用:0次
名校
8 . 镓的化合物
(1)半导体工业中通过刻蚀制造微纳结构,GaN是重要的半导体材料,通常采用含氯气体在放电条件下进行刻蚀。写出利用Ar-Cl2混合气体放电刻蚀GaN的化学方程式_____ 。
(2)金属镓熔点很低但沸点很高其中存在二聚体Ga.1990年,科学家将液态Ga和l2在甲苯中超声处理,得到了组成为Gal的物质。该物质中含有多种不同氧化态的Ga,具有两种可能的结构,分子式分别为Ga4I4(A)和Ga6I6(B),二者对应的阴离子分别为C和D,两种阴离子均由Ga和I构成且其中所有原子的价层均满足8电子。写出示出A和B组成特点的结构笱式并标出Ga的氧化态_____ ,画出C和D的结构_____ 。
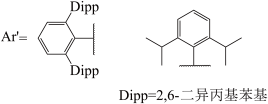
(3)GaI常用于合成低价Ga的化合物。将GaI与Ar’Li(Ar’基如图所示,解答中直接采用简写Ar’)在-78℃的甲苯溶液中反应,得到晶体E,E中含有2个Ga原子:E在乙醚溶液中与金属钠反应得到晶体F,X射线晶体学表明,F中的Ga-Ga键长比E中短0.028nm。关于F中Ga-Ga的键级历史上曾有过争议,其中一种观点认为,F中的Ca价层满足8电子。基于该观点,画出E和F的结构式_____ 。
(1)半导体工业中通过刻蚀制造微纳结构,GaN是重要的半导体材料,通常采用含氯气体在放电条件下进行刻蚀。写出利用Ar-Cl2混合气体放电刻蚀GaN的化学方程式
(2)金属镓熔点很低但沸点很高其中存在二聚体Ga.1990年,科学家将液态Ga和l2在甲苯中超声处理,得到了组成为Gal的物质。该物质中含有多种不同氧化态的Ga,具有两种可能的结构,分子式分别为Ga4I4(A)和Ga6I6(B),二者对应的阴离子分别为C和D,两种阴离子均由Ga和I构成且其中所有原子的价层均满足8电子。写出示出A和B组成特点的结构笱式并标出Ga的氧化态

(3)GaI常用于合成低价Ga的化合物。将GaI与Ar’Li(Ar’基如图所示,解答中直接采用简写Ar’)在-78℃的甲苯溶液中反应,得到晶体E,E中含有2个Ga原子:E在乙醚溶液中与金属钠反应得到晶体F,X射线晶体学表明,F中的Ga-Ga键长比E中短0.028nm。关于F中Ga-Ga的键级历史上曾有过争议,其中一种观点认为,F中的Ca价层满足8电子。基于该观点,画出E和F的结构式
您最近一年使用:0次
2023-09-07更新
|
322次组卷
|
2卷引用:2023年第37届中国化学奥林匹克(初赛)化学试题
解题方法
9 . 硅可以和多种金属形成组成各异、结构丰富的二元化合物。例如,在Ca-Si体系中,有Ca₅Si,Ca2Si,CaSi2,CaSi3等等。随着高压科学和技术的发展,总来越多的新物相新结构得以发现且呈现出有趣的成键特点。在20GPa条件下得到的二元Ca-Si化合物D属四方晶系,晶胞参数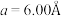 ,
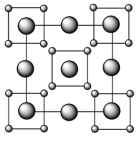
,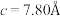 ,结构沿c方向的投影如图所示,虚线围出晶胞,浅色大球代表
,结构沿c方向的投影如图所示,虚线围出晶胞,浅色大球代表 ,深色小球代表硅原子,硅形成平面正方形的四聚硅簇,其中Si-Si键长为
,深色小球代表硅原子,硅形成平面正方形的四聚硅簇,其中Si-Si键长为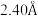 。Ca离子在用平面四方形排列形成垂直于c的层(同层离子即可给出图中投影)与四聚硅阴离子所形成的层沿c方向均衡交替排布,有一半Ca离子投影在平面正方形硅簇的中心位置。
。Ca离子在用平面四方形排列形成垂直于c的层(同层离子即可给出图中投影)与四聚硅阴离子所形成的层沿c方向均衡交替排布,有一半Ca离子投影在平面正方形硅簇的中心位置。
(1)写出化合物D晶体的点阵型式和结构基元___________ 。(提示:注意同号电荷相斥!)
(2)若将晶胞原点取在四聚硅簇平面正方形的中心,写出晶胞中所有原子的坐标参数_______ 。
(3)写出Si的氧化数并画出四聚硅阴离子的经典Lewis结构___________ 。
(4)化学物D不稳定,大气压下可发生分解。其产物之一便是CaSi2.CaSi2也有丰富的结构,其中一种结构中,硅通过三连接方式形成二维延伸,硅只有一种化学环境且所有硅原子的价层均满足八电子。画出该结构的示意图___________ 。(要求:示出结构特征,至少包含20个硅原子,并勾勒出二维晶胞)
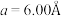 ,
,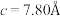 ,结构沿c方向的投影如图所示,虚线围出晶胞,浅色大球代表
,结构沿c方向的投影如图所示,虚线围出晶胞,浅色大球代表 ,深色小球代表硅原子,硅形成平面正方形的四聚硅簇,其中Si-Si键长为
,深色小球代表硅原子,硅形成平面正方形的四聚硅簇,其中Si-Si键长为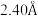 。Ca离子在用平面四方形排列形成垂直于c的层(同层离子即可给出图中投影)与四聚硅阴离子所形成的层沿c方向均衡交替排布,有一半Ca离子投影在平面正方形硅簇的中心位置。
。Ca离子在用平面四方形排列形成垂直于c的层(同层离子即可给出图中投影)与四聚硅阴离子所形成的层沿c方向均衡交替排布,有一半Ca离子投影在平面正方形硅簇的中心位置。
(1)写出化合物D晶体的点阵型式和结构基元
(2)若将晶胞原点取在四聚硅簇平面正方形的中心,写出晶胞中所有原子的坐标参数
(3)写出Si的氧化数并画出四聚硅阴离子的经典Lewis结构
(4)化学物D不稳定,大气压下可发生分解。其产物之一便是CaSi2.CaSi2也有丰富的结构,其中一种结构中,硅通过三连接方式形成二维延伸,硅只有一种化学环境且所有硅原子的价层均满足八电子。画出该结构的示意图
您最近一年使用:0次
10 . nesteretal A是一种从某菌体中提取出来的笼状聚半缩酮,在2021年,化学家Yuichiro Kawamoto等人提出了nesteretal A的一种全合成路线。下面展示了该全合成路线的部分反应。
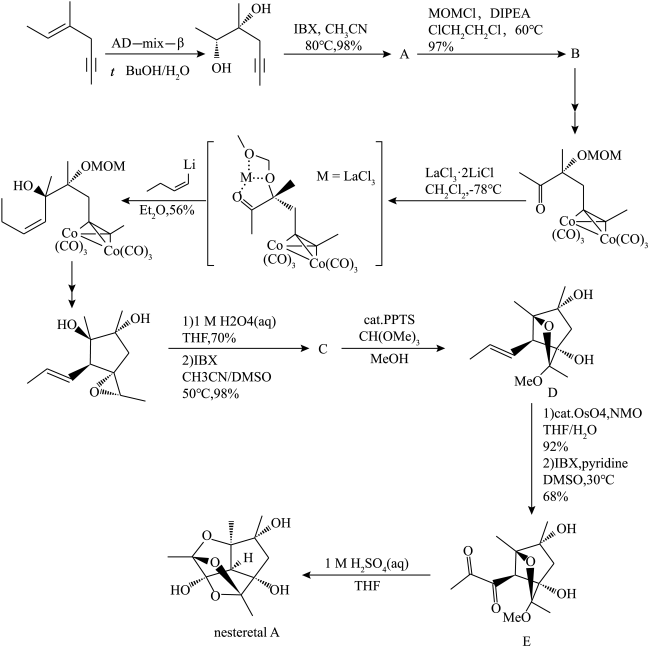
(1)已知IBX是一种氧化剂,可以将醇氧化为酮;环氧乙烷在酸性水溶液中会水解为乙二醇。请画出A、C的键线式______ 、______ 。
(2)根据前后反应,写出MOMCl的键线式______ ,并说明A到B的反应类型______ 。
(3)加入反应物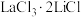 的目的是什么
的目的是什么______ ?
(4)试画出D到E的第一步反应产物的键线式______ 。(不要求立体构型)
(5)请写出nesteretal A的分子式_______ 。

(1)已知IBX是一种氧化剂,可以将醇氧化为酮;环氧乙烷在酸性水溶液中会水解为乙二醇。请画出A、C的键线式
(2)根据前后反应,写出MOMCl的键线式
(3)加入反应物
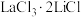 的目的是什么
的目的是什么(4)试画出D到E的第一步反应产物的键线式
(5)请写出nesteretal A的分子式
您最近一年使用:0次



