解题方法
1 . 某学生准备用质量分数为98%、密度为 的浓硫酸配制500mL约0.2mol/L的硫酸溶液。
的浓硫酸配制500mL约0.2mol/L的硫酸溶液。
(1)从下列用品中选出实验所需要的仪器:_______ (填序号)。
A. 500mL烧杯 B. 100mL烧杯 C. 10mL量筒 D. 100mL量筒 E. 500mL容量瓶 F.1000mL容量瓶 G.胶头滴管 H.托盘天平 I.玻璃棒
(2)请设计简单的实验方案,写出实验步骤。______
 的浓硫酸配制500mL约0.2mol/L的硫酸溶液。
的浓硫酸配制500mL约0.2mol/L的硫酸溶液。(1)从下列用品中选出实验所需要的仪器:
A. 500mL烧杯 B. 100mL烧杯 C. 10mL量筒 D. 100mL量筒 E. 500mL容量瓶 F.1000mL容量瓶 G.胶头滴管 H.托盘天平 I.玻璃棒
(2)请设计简单的实验方案,写出实验步骤。
您最近一年使用:0次
名校
2 . 已知X、Y、Z、W、R五种元素中,X是宇宙中最丰富的元素,Y元素原子最外层电子数是内层电子总数的2倍;Z元素原子最外层电子数比其次外层电子数多4个;W元素原子K层和M层电子总数等于其L层电子数;R元素原子最外层有1个电子,其阳离子与Z的阴离子核外电子总数相同。请完成下列问题。
(1)R元素的原子结构示意图为_______ ;Z元素形成的阴离子的结构示意图为_______ 。
(2)含X、Y、Z、R四种元素的化合物的化学式为_______ 。
(3)W的两种氧化物的分子式是_______ 、_______ 。
(4)化合物 与
与 反应的化学方程式为
反应的化学方程式为_______ 。
(1)R元素的原子结构示意图为
(2)含X、Y、Z、R四种元素的化合物的化学式为
(3)W的两种氧化物的分子式是
(4)化合物
 与
与 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
2022-11-24更新
|
272次组卷
|
2卷引用:苏教2020版化学必修第一册专题2 研究物质的基本方法 第三单元 人类对原子结构的认识课后习题
23-24高一上·全国·假期作业
解题方法
3 . 已知氨可以与灼热的氧化铜反应生成氮气和金属铜,用下面示意图中的装置可以实现该反应。
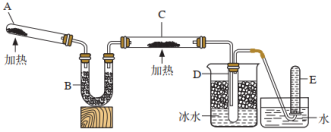
A中装有的NH4Cl和Ca(OH)2混合物在加热条件下,可以发生反应生成CaCl2、NH3和H2O。
试回答下列问题:
(1)B中加入的物质是碱石灰(CaO和NaOH的混合物),其作用是____ 。
(2)实验时在C中观察到的现象是____ ,发生反应的化学方程式是_____ 。
(3)实验时在D中观察到的现象是____ ,收集到的物质是____ 。

A中装有的NH4Cl和Ca(OH)2混合物在加热条件下,可以发生反应生成CaCl2、NH3和H2O。
试回答下列问题:
(1)B中加入的物质是碱石灰(CaO和NaOH的混合物),其作用是
(2)实验时在C中观察到的现象是
(3)实验时在D中观察到的现象是
您最近一年使用:0次
解题方法
4 . 利用身边的物品(如废金属片、水果等)制作一个简易电池,测试是否有电流产生。找一个发光二极管,与同学比比看谁制作的电池能使发光二极管更亮__________ 。
您最近一年使用:0次
解题方法
5 . 随着原子序数的递增, 种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
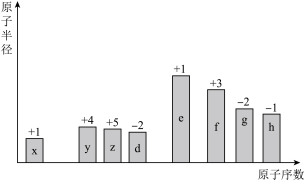
请回答下列问题:
(1) 在元素周期表中的位置是
在元素周期表中的位置是_______ 。
(2)比较 、
、 常见离子的半径大小:
常见离子的半径大小:_______ >_______ ;比较 、
、 的最高价氧化物的水化物的酸性强弱:
的最高价氧化物的水化物的酸性强弱:_______ >_______ 。(用化学式表示,下同)
(3) 、
、 的单质分别与
的单质分别与 的单质化合时,较容易的是
的单质化合时,较容易的是_______ ,形成的化合物热稳定性较差的是_______ 。
(4) 元素的原子间连接方式多样,两个原子间可通过共用电子对形成
元素的原子间连接方式多样,两个原子间可通过共用电子对形成_______ 键、_______ 键或_______ 键;多个原子之间可以通过共价键彼此结合形成_______ ,也可以连接形成_______ ,这也是有机化合物种类繁多的原因之一。
(5)任选上述元素形成一种四原子共价化合物,写出其电子式:_______ 。
 种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
种短周期元素(用字母表示)原子半径的相对大小、最高正化合价或最低负化合价的变化如图所示。
请回答下列问题:
(1)
 在元素周期表中的位置是
在元素周期表中的位置是(2)比较
 、
、 常见离子的半径大小:
常见离子的半径大小: 、
、 的最高价氧化物的水化物的酸性强弱:
的最高价氧化物的水化物的酸性强弱:(3)
 、
、 的单质分别与
的单质分别与 的单质化合时,较容易的是
的单质化合时,较容易的是(4)
 元素的原子间连接方式多样,两个原子间可通过共用电子对形成
元素的原子间连接方式多样,两个原子间可通过共用电子对形成(5)任选上述元素形成一种四原子共价化合物,写出其电子式:
您最近一年使用:0次
解题方法
6 . 实验室有一瓶放置已久的盐酸,标签中没有说明其物质的量浓度。
(1)A同学发现标签中标有该盐酸的密度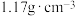 、溶质质量分数
、溶质质量分数 。能否根据这些信息计算出该盐酸的物质的量浓度
。能否根据这些信息计算出该盐酸的物质的量浓度_______ ?
(2)B同学认为该盐酸已经放置很久了,其中氯化氢或许已经挥发了一部分。他打算通过定量实验来测出该盐酸的物质的量浓度,请你帮助他设计一个简单的实验方案_______ 。
(1)A同学发现标签中标有该盐酸的密度
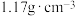 、溶质质量分数
、溶质质量分数 。能否根据这些信息计算出该盐酸的物质的量浓度
。能否根据这些信息计算出该盐酸的物质的量浓度(2)B同学认为该盐酸已经放置很久了,其中氯化氢或许已经挥发了一部分。他打算通过定量实验来测出该盐酸的物质的量浓度,请你帮助他设计一个简单的实验方案
您最近一年使用:0次
解题方法
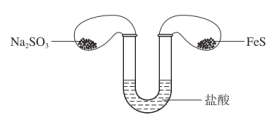
7 . 如下图所示,将两只气球中少量的 和
和 粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式
粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式_______ 。
 和
和 粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式
粉末同时倒入足量的盐酸中,写出反应的现象和有关的化学方程式
您最近一年使用:0次
解题方法
8 . 历史上曾用绿矾( )制备硫酸。高温条件下
)制备硫酸。高温条件下 发生如下分解反应:
发生如下分解反应: 。为检验
。为检验 高温分解的气体产物,进行如下实验:将
高温分解的气体产物,进行如下实验:将 高温分解产生的气体通入下图所示的装置中,以检验产生的气体中是否含有
高温分解产生的气体通入下图所示的装置中,以检验产生的气体中是否含有 、
、 。
。
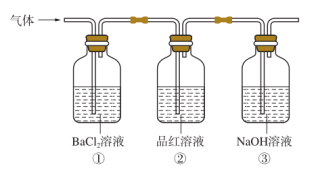
(1)请写出试剂瓶①和③中反应的化学方程式_______ 。
(2)为什么要将通过品红溶液的气体再通入 溶液中
溶液中_______ 。
 )制备硫酸。高温条件下
)制备硫酸。高温条件下 发生如下分解反应:
发生如下分解反应: 。为检验
。为检验 高温分解的气体产物,进行如下实验:将
高温分解的气体产物,进行如下实验:将 高温分解产生的气体通入下图所示的装置中,以检验产生的气体中是否含有
高温分解产生的气体通入下图所示的装置中,以检验产生的气体中是否含有 、
、 。
。
(1)请写出试剂瓶①和③中反应的化学方程式
(2)为什么要将通过品红溶液的气体再通入
 溶液中
溶液中
您最近一年使用:0次
解题方法
9 . 某硫酸厂周围的空气中含有较多的二氧化硫,环保部门为了测定空气中二氧化硫的体积分数,做了如下实验。取标准状况下的空气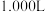 (含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,反应的化学方程式为:
(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,反应的化学方程式为: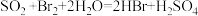 。在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为
。在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为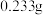 。试回答:
。试回答:
(1)加入过量氯化钡溶液的目的是_______ 。
(2)过滤时,如何除去沉淀中附着的少量
_______ 。
(3)计算该空气样品中二氧化硫的体积分数_______ 。
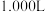 (含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,反应的化学方程式为:
(含氮气、氧气、二氧化碳、二氧化硫等),缓慢通过足量溴水,反应的化学方程式为: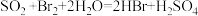 。在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为
。在所得溶液中加入过量的氯化钡溶液,产生白色沉淀,将沉淀洗涤、干燥,称得其质量为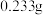 。试回答:
。试回答:(1)加入过量氯化钡溶液的目的是
(2)过滤时,如何除去沉淀中附着的少量

(3)计算该空气样品中二氧化硫的体积分数
您最近一年使用:0次
解题方法
10 . 实验室可以用硫酸和亚硫酸钠反应来制备二氧化硫。写出反应的化学方程式_______ ,画出制备和收集二氧化硫气体的实验装置简图_______ 。
您最近一年使用:0次



