解题方法
1 . 动手实践
请按以下方法制作肥皂。
①向烧杯中加入20g油脂、10 无水乙醇和
无水乙醇和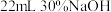 溶液,加热搅拌。当液面出现泡沫后,加强搅拌;当泡沫覆盖整个液面时,停止加热。
溶液,加热搅拌。当液面出现泡沫后,加强搅拌;当泡沫覆盖整个液面时,停止加热。
②向皂化产物中缓缓加入适量的饱和食盐水(或食盐细粒)并搅拌,冷却后分离出上层的高级脂肪酸钠。
③向分离出的高级脂肪酸钠中加入4 饱和
饱和 溶液(或4g松香),倒入模具中,冷凝固化。
溶液(或4g松香),倒入模具中,冷凝固化。
请回答下列问题。
(1)在制作过程中,加入乙醇和饱和食盐水的作用分别是什么?________
(2)有的同学制作出的肥皂中仍含有油脂,你认为这是什么原因造成的________ ?可采取哪些措施来避免这种情况的出现?________
请按以下方法制作肥皂。
①向烧杯中加入20g油脂、10
 无水乙醇和
无水乙醇和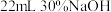 溶液,加热搅拌。当液面出现泡沫后,加强搅拌;当泡沫覆盖整个液面时,停止加热。
溶液,加热搅拌。当液面出现泡沫后,加强搅拌;当泡沫覆盖整个液面时,停止加热。②向皂化产物中缓缓加入适量的饱和食盐水(或食盐细粒)并搅拌,冷却后分离出上层的高级脂肪酸钠。
③向分离出的高级脂肪酸钠中加入4
 饱和
饱和 溶液(或4g松香),倒入模具中,冷凝固化。
溶液(或4g松香),倒入模具中,冷凝固化。请回答下列问题。
(1)在制作过程中,加入乙醇和饱和食盐水的作用分别是什么?
(2)有的同学制作出的肥皂中仍含有油脂,你认为这是什么原因造成的
您最近一年使用:0次
2 . 下图表示的是丙酸与其他物质间的转化关系,请在括号内填写有关物质的名称,并写出与序号①②④对应的反应的化学方程式。
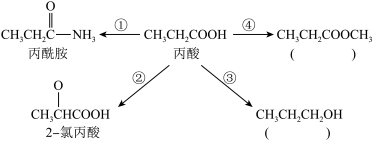
(1)写出有关物质的名称,CH3CH2COOCH3___________ ;CH3CH2CH2OH__________
(2)写出下列步骤的反应方程式为①___________ ;②___________ ;④___________ ;

(1)写出有关物质的名称,CH3CH2COOCH3
(2)写出下列步骤的反应方程式为①
您最近一年使用:0次
解题方法
3 . 两种有机化合物A和B互为同分异构体,分子式皆为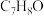 。A能与氢溴酸反应,生成物的分子式为
。A能与氢溴酸反应,生成物的分子式为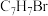 ,而B不能与氢溴酸反应;A不溶于
,而B不能与氢溴酸反应;A不溶于 溶液,而B能溶于
溶液,而B能溶于 溶液;B能使适量溴水褪色并产生白色沉淀,而A不能。B的一溴代物有三种。写出A、B的结构简式
溶液;B能使适量溴水褪色并产生白色沉淀,而A不能。B的一溴代物有三种。写出A、B的结构简式_____ 、_____ ,名称_____ 、_____ ,以及有关反应的化学方程式_________ 。
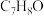 。A能与氢溴酸反应,生成物的分子式为
。A能与氢溴酸反应,生成物的分子式为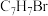 ,而B不能与氢溴酸反应;A不溶于
,而B不能与氢溴酸反应;A不溶于 溶液,而B能溶于
溶液,而B能溶于 溶液;B能使适量溴水褪色并产生白色沉淀,而A不能。B的一溴代物有三种。写出A、B的结构简式
溶液;B能使适量溴水褪色并产生白色沉淀,而A不能。B的一溴代物有三种。写出A、B的结构简式
您最近一年使用:0次
解题方法
4 . 乙酸苯甲酯可提高花或果的芳香气味,故常用于化妆品工业和食品工业。乙酸苯甲酯可以用下面的设计方案合成。
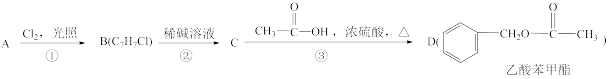
(1)写出A、B、C三种有机化合物的结构简式:A_____ ,B_____ ,C_____ 。
(2)分别写出①②③三个步骤发生反应的化学方程式,并指明所属的有机反应类型_____ 、_____ 、_____ 。
(3)化合物D分子中的官能团是如何形成的_____ ?

(1)写出A、B、C三种有机化合物的结构简式:A
(2)分别写出①②③三个步骤发生反应的化学方程式,并指明所属的有机反应类型
(3)化合物D分子中的官能团是如何形成的
您最近一年使用:0次
解题方法
5 . 香豆素是一种用途广泛的香料,可用于配制香精以及制造日用化妆品和香皂等。某同学设计的香豆素的合成路线为:
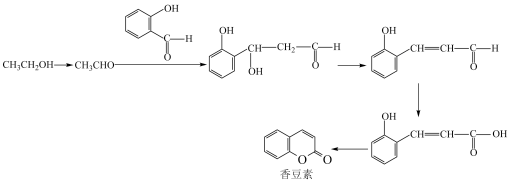
结合本节教材中“拓展视野”栏目分析:上述合成过程中,碳骨架是通过什么反应构建的_________ ,官能团是通过什么反应转化的_________ 。

结合本节教材中“拓展视野”栏目分析:上述合成过程中,碳骨架是通过什么反应构建的
您最近一年使用:0次
解题方法
6 . 通过本章学习,你对各类烃的衍生物都有哪些新的认识?它们的官能团各有什么结构特点?官能团的结构决定了它们具有怎样的性质?各类物质之间的转化关系如何?请根据你的理解画出本章的知识网络图_________ 。
您最近一年使用:0次
解题方法
7 . 钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)K和 属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属
属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属 低,试解释原因。
低,试解释原因。_____
(2) 晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为
晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为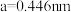 ,晶胞中K、I、O分别处于顶点、体心、面心位置,如图所示。与K紧邻的O有
,晶胞中K、I、O分别处于顶点、体心、面心位置,如图所示。与K紧邻的O有_____ 个?试说明分析思路。_____
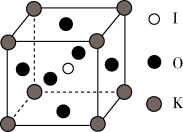
(3)计算K与O间的最短距离_____ 。
(1)K和
 属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属
属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属 低,试解释原因。
低,试解释原因。(2)
 晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为
晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为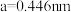 ,晶胞中K、I、O分别处于顶点、体心、面心位置,如图所示。与K紧邻的O有
,晶胞中K、I、O分别处于顶点、体心、面心位置,如图所示。与K紧邻的O有
(3)计算K与O间的最短距离
您最近一年使用:0次
解题方法
8 . 金刚砂( )是重要的工业制品,可由二氧化硅与碳的反应制得:
)是重要的工业制品,可由二氧化硅与碳的反应制得: 。
。 的晶体结构与金刚石的相似,如本章如图所示,其中C原子和
的晶体结构与金刚石的相似,如本章如图所示,其中C原子和 原子的位置是交替的。
原子的位置是交替的。

(1)X是______ ?
(2)写出基态 原子的电子排布式
原子的电子排布式______ ; 中
中 的化合价是
的化合价是______ ?
(3)X可与氧气反应生成Y,判断Y分子的中心原子杂化轨道类型和键角______
(4) 晶体与晶体硅相比,熔点较高的是
晶体与晶体硅相比,熔点较高的是______ 晶体?请分析原因______
(5)在 中最小的环上有
中最小的环上有______ 个原子,已知 键的键能为a
键的键能为a ,理论上分解1
,理论上分解1
 形成气态原子所需要的能量是
形成气态原子所需要的能量是______ 。
 )是重要的工业制品,可由二氧化硅与碳的反应制得:
)是重要的工业制品,可由二氧化硅与碳的反应制得: 。
。 的晶体结构与金刚石的相似,如本章如图所示,其中C原子和
的晶体结构与金刚石的相似,如本章如图所示,其中C原子和 原子的位置是交替的。
原子的位置是交替的。
(1)X是
(2)写出基态
 原子的电子排布式
原子的电子排布式 中
中 的化合价是
的化合价是(3)X可与氧气反应生成Y,判断Y分子的中心原子杂化轨道类型和键角
(4)
 晶体与晶体硅相比,熔点较高的是
晶体与晶体硅相比,熔点较高的是(5)在
 中最小的环上有
中最小的环上有 键的键能为a
键的键能为a ,理论上分解1
,理论上分解1
 形成气态原子所需要的能量是
形成气态原子所需要的能量是
您最近一年使用:0次
9 . 金属和非金属分界线附近的元素(如 、
、 、
、 ),可用于制造半导体材料,是科学研究的热点。试回答下列问题:
),可用于制造半导体材料,是科学研究的热点。试回答下列问题:
(1)锗( )是一种重要的半导体材料,写出基态
)是一种重要的半导体材料,写出基态 原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。
原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。________
(2) 是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是
是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是________ ?
(3) 等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个
等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个 原子周围有
原子周围有________ 个距离最近的 原子?每个晶胞中有
原子?每个晶胞中有________ 个 原子?
原子?

 、
、 、
、 ),可用于制造半导体材料,是科学研究的热点。试回答下列问题:
),可用于制造半导体材料,是科学研究的热点。试回答下列问题:(1)锗(
 )是一种重要的半导体材料,写出基态
)是一种重要的半导体材料,写出基态 原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。
原子的价层电子排布式,说明价电子在其最高能级上的分布遵循的原则。(2)
 是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是
是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是(3)
 等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个
等是人工合成的新型半导体材料,其晶体结构与金刚石相似,如图所示。每个 原子周围有
原子周围有 原子?每个晶胞中有
原子?每个晶胞中有 原子?
原子?
您最近一年使用:0次
解题方法
10 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如表实验。
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
(1)实验目的是____ 。
(2)请解释实验②中加入4.0mL蒸馏水的原因:____ 。
(3)据实验资料记载,Mn2+对该反应有催化作用。某小组同学计划设计实验验证Mn2+对该反应有催化作用,请填写表中空白。
若所加固体对反应确有催化作用,应观察到的现象是____ 。
【实验原理】2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
【实验内容及记录】
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色时所需时间/min | |||
| 0.6mol•L-1H2C2O4溶液 | H2O | 0.2mol•L-1KMnO4溶液 | 3.0mol•L-1稀硫酸 | ||
| ① | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
| ② | 1.0 | 4.0 | 3.0 | 2.0 | 6.4 |
(2)请解释实验②中加入4.0mL蒸馏水的原因:
(3)据实验资料记载,Mn2+对该反应有催化作用。某小组同学计划设计实验验证Mn2+对该反应有催化作用,请填写表中空白。
| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 向试管中加入少量固体 | 室温下溶液颜色褪至色时所需时间/min | |||
| 0.6mol•L-1H2C2O4溶液 | H2O | 0.2mol•L-1KMnO4溶液 | 3.0mol•L-1稀硫酸 | |||
| ③ | 3.0 | t | ||||
您最近一年使用:0次



