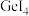名校
解题方法
1 . 碳元素的单质有多种形式,下图依次是 、石墨和金刚石的结构图:
、石墨和金刚石的结构图:
(1)金刚石、石墨、 、碳纳米管等都是碳元素的单质形式,它们互为
、碳纳米管等都是碳元素的单质形式,它们互为__________ 。
(2)石墨烯(指单层石墨)中碳原子的杂化形式_____________ 。
(3) 属于
属于__________ 晶体。
(4)石墨晶体中,层内C-C键的键长为142pm,而金刚石中C-C键的键长为154pm。其原因是金刚石中只存在C-C间的σ键,而石墨层内的C-C间不仅存在σ键,还有__________ 键。
(5)Ge与C是同族元素,比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________ 。
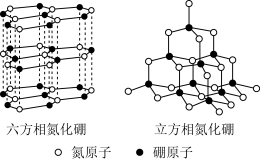
(6)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。_____ (填序号)。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
② (氟硼酸铵)是合成氮化硼纳米管的原料之一、1mol
(氟硼酸铵)是合成氮化硼纳米管的原料之一、1mol  含有
含有_____ mol配位键。
 、石墨和金刚石的结构图:
、石墨和金刚石的结构图:
(1)金刚石、石墨、
 、碳纳米管等都是碳元素的单质形式,它们互为
、碳纳米管等都是碳元素的单质形式,它们互为(2)石墨烯(指单层石墨)中碳原子的杂化形式
(3)
 属于
属于(4)石墨晶体中,层内C-C键的键长为142pm,而金刚石中C-C键的键长为154pm。其原因是金刚石中只存在C-C间的σ键,而石墨层内的C-C间不仅存在σ键,还有
(5)Ge与C是同族元素,比较下列锗卤化物的熔点和沸点,分析其变化规律及原因
|
|
| |
熔点/℃ | -49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(6)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图所示。
a.立方相氮化硼含有σ键和π键,所以硬度大
b.六方相氮化硼层间作用力小,所以质地软
c.两种晶体中的B-N键均为共价键
d.两种晶体均为分子晶体
②
 (氟硼酸铵)是合成氮化硼纳米管的原料之一、1mol
(氟硼酸铵)是合成氮化硼纳米管的原料之一、1mol  含有
含有
您最近一年使用:0次
名校
2 . 酚类化合物在医疗、环保、工业等方面有着广泛的用途。

已知部分弱酸的电离平衡常数如下表所示:
(1)室温下,0.1mol/L苯酚钠溶液的pH___________ 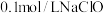 溶液的pH。
溶液的pH。
a.大于 b.小于 c.等于
(2)向苯酚钠水溶液中通入少量SO2,写出反应的离子方程式___________ 。
Ⅱ.石油加工、造纸等企业易产生含有苯酚的工业废水,可通过 氧化法进行处理,其原理为
氧化法进行处理,其原理为 (非可逆反应,反应未配平)。在
(非可逆反应,反应未配平)。在 和
和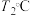 时,分别向含有苯酚的水样中加入等量的
时,分别向含有苯酚的水样中加入等量的 溶液,再以相同的流速向水样中通入
溶液,再以相同的流速向水样中通入 ,测得水样中苯酚的含量随时间变化的曲线如图所示。
,测得水样中苯酚的含量随时间变化的曲线如图所示。 时,
时,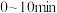 内,
内, 的平均反应速率为
的平均反应速率为___________ 。
(4)请判断 和
和 的大小:
的大小:
___________  。
。
a.大于 b.小于 c.等于
(5) 时对工业废水中苯酚的去除率低于
时对工业废水中苯酚的去除率低于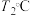 时的原因可能是
时的原因可能是___________ (写一种即可)。
(6)利用 溶液与苯酚的显色反应,可定性检测工业废水中的苯酚,其反应原理为
溶液与苯酚的显色反应,可定性检测工业废水中的苯酚,其反应原理为 。反应到达平衡时,下列说法正确的有___________。
。反应到达平衡时,下列说法正确的有___________。
Ⅲ.绿原酸是一种新型高效的酚型天然抗氧化剂,在食品行业有着广泛的用途。 发生反应,则绿原酸的分子式为
发生反应,则绿原酸的分子式为___________ 。
(8)1mol化合物Ⅰ与足量金属钠反应生成标准状况下氢气体积为___________ 。
(9)化合物Ⅲ有如下特点:①与化合物Ⅱ互为同分异构体;②遇 溶液显色;③1mol化合物Ⅲ与足量银氨溶液反应生成
溶液显色;③1mol化合物Ⅲ与足量银氨溶液反应生成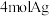 ;④苯环上的一卤代物只有一种。写出化合物Ⅲ的一种可能的结构简式:
;④苯环上的一卤代物只有一种。写出化合物Ⅲ的一种可能的结构简式:___________ 。

已知部分弱酸的电离平衡常数如下表所示:
| 弱酸 | 次氯酸 | 亚硫酸 | 苯酚 |
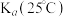 | 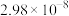 | 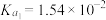  |  |
(1)室温下,0.1mol/L苯酚钠溶液的pH
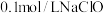 溶液的pH。
溶液的pH。a.大于 b.小于 c.等于
(2)向苯酚钠水溶液中通入少量SO2,写出反应的离子方程式
Ⅱ.石油加工、造纸等企业易产生含有苯酚的工业废水,可通过
 氧化法进行处理,其原理为
氧化法进行处理,其原理为 (非可逆反应,反应未配平)。在
(非可逆反应,反应未配平)。在 和
和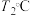 时,分别向含有苯酚的水样中加入等量的
时,分别向含有苯酚的水样中加入等量的 溶液,再以相同的流速向水样中通入
溶液,再以相同的流速向水样中通入 ,测得水样中苯酚的含量随时间变化的曲线如图所示。
,测得水样中苯酚的含量随时间变化的曲线如图所示。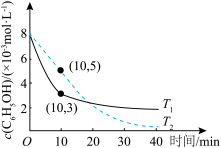
 时,
时,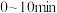 内,
内, 的平均反应速率为
的平均反应速率为(4)请判断
 和
和 的大小:
的大小:
 。
。a.大于 b.小于 c.等于
(5)
 时对工业废水中苯酚的去除率低于
时对工业废水中苯酚的去除率低于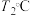 时的原因可能是
时的原因可能是(6)利用
 溶液与苯酚的显色反应,可定性检测工业废水中的苯酚,其反应原理为
溶液与苯酚的显色反应,可定性检测工业废水中的苯酚,其反应原理为 。反应到达平衡时,下列说法正确的有___________。
。反应到达平衡时,下列说法正确的有___________。| A.加水稀释,溶液pH减小 |
B.滴入几滴浓盐酸,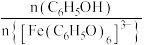 增大 增大 |
| C.加入少量NaOH固体,反应平衡常数增大 |
| D.加入少量Cu粉,溶液紫色变浅 |
Ⅲ.绿原酸是一种新型高效的酚型天然抗氧化剂,在食品行业有着广泛的用途。

 发生反应,则绿原酸的分子式为
发生反应,则绿原酸的分子式为(8)1mol化合物Ⅰ与足量金属钠反应生成标准状况下氢气体积为
(9)化合物Ⅲ有如下特点:①与化合物Ⅱ互为同分异构体;②遇
 溶液显色;③1mol化合物Ⅲ与足量银氨溶液反应生成
溶液显色;③1mol化合物Ⅲ与足量银氨溶液反应生成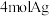 ;④苯环上的一卤代物只有一种。写出化合物Ⅲ的一种可能的结构简式:
;④苯环上的一卤代物只有一种。写出化合物Ⅲ的一种可能的结构简式:
您最近一年使用:0次
名校
3 . 二氯化二硫( )可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。
)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。 可通过硫与少量氯气在110~140℃反应制得。
可通过硫与少量氯气在110~140℃反应制得。
(1)有关 的下列说法正确的是 。
的下列说法正确的是 。
(2)选用以下装置制取少量 (加热及夹持装置略):
(加热及夹持装置略):_____________________ 。
②装置连接顺序:A→__________ →D。
③B中玻璃纤维的作用是______________________ 。
④D中的最佳试剂是__________ (选填序号)。
a.碱石灰 b.浓硫酸 c.NaOH溶液 d.无水氯化钙
(3) 遇水会生成
遇水会生成 、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中
、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中 的体积分数。
的体积分数。_________ (填标号);
a. 溶液 b.
溶液 b. 溶液(硫酸酸化) c.氯水
溶液(硫酸酸化) c.氯水
 )可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。
)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。 可通过硫与少量氯气在110~140℃反应制得。
可通过硫与少量氯气在110~140℃反应制得。(1)有关
 的下列说法正确的是 。
的下列说法正确的是 。A. 中S-Cl键的键能大于S-S键的键能 中S-Cl键的键能大于S-S键的键能 | B.固态时 属于原子晶体 属于原子晶体 |
| C.第一电离能、电负性均为:Cl>S | D. 中既有极性键又有非极性键 中既有极性键又有非极性键 |
(2)选用以下装置制取少量
 (加热及夹持装置略):
(加热及夹持装置略):
②装置连接顺序:A→
③B中玻璃纤维的作用是
④D中的最佳试剂是
a.碱石灰 b.浓硫酸 c.NaOH溶液 d.无水氯化钙
(3)
 遇水会生成
遇水会生成 、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中
、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中 的体积分数。
的体积分数。
a.
 溶液 b.
溶液 b. 溶液(硫酸酸化) c.氯水
溶液(硫酸酸化) c.氯水
您最近一年使用:0次
名校
4 . 碘及其化合物广泛用于医药、染料等方面。用沉淀滴定法快速测定NaI等碘化物溶液中 ,实验过程包括准备标准溶液和滴定待测溶液。
,实验过程包括准备标准溶液和滴定待测溶液。
一、准备标准溶液
I.准确称取 基准物
基准物 后,配制成
后,配制成 标准溶液,放在棕色试剂瓶中避光保存,备用。
标准溶液,放在棕色试剂瓶中避光保存,备用。
II.配制并标定 标准溶液,备用。
标准溶液,备用。
二、滴定的主要步骤
a.取待测NaI溶液 于锥形瓶中。
于锥形瓶中。
c.加入 溶液作指示剂。
溶液作指示剂。
d.用 溶液滴定过量的
溶液滴定过量的 ,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如下表:
f.数据处理。
(1)将称得的 配制成标准溶液,所使用的仪器不包括___________。
配制成标准溶液,所使用的仪器不包括___________。
(2)b和c两步操作是否可以颠倒___________ ,说明理由___________ 。
(3)当___________ 即达到滴定终点。消耗的 标准溶液平均体积为
标准溶液平均体积为___________  ,计算得
,计算得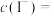
___________  ;在滴定管中装入
;在滴定管中装入 标准溶液的前一步,应进行的操作为
标准溶液的前一步,应进行的操作为___________ ;如不进行此步操作,对实验结果产生怎样的影响___________ 。
(4)若在配制 标准溶液时,烧杯中的溶液有少量溅出,则测定结果___________。
标准溶液时,烧杯中的溶液有少量溅出,则测定结果___________。
(5)若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果___________ 。
 ,实验过程包括准备标准溶液和滴定待测溶液。
,实验过程包括准备标准溶液和滴定待测溶液。一、准备标准溶液
I.准确称取
 基准物
基准物 后,配制成
后,配制成 标准溶液,放在棕色试剂瓶中避光保存,备用。
标准溶液,放在棕色试剂瓶中避光保存,备用。II.配制并标定
 标准溶液,备用。
标准溶液,备用。二、滴定的主要步骤
a.取待测NaI溶液
 于锥形瓶中。
于锥形瓶中。c.加入
 溶液作指示剂。
溶液作指示剂。d.用
 溶液滴定过量的
溶液滴定过量的 ,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。e.重复上述操作两次。三次测定数据如下表:
| 实验序号 | 1 | 2 | 3 |
消耗 标准溶液体积/mL 标准溶液体积/mL | 10.24 | 10.02 | 9.98 |
(1)将称得的
 配制成标准溶液,所使用的仪器不包括___________。
配制成标准溶液,所使用的仪器不包括___________。| A.烧杯 | B.胶头滴管 | C.容量瓶 | D.量筒 |
(3)当
 标准溶液平均体积为
标准溶液平均体积为 ,计算得
,计算得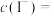
 ;在滴定管中装入
;在滴定管中装入 标准溶液的前一步,应进行的操作为
标准溶液的前一步,应进行的操作为(4)若在配制
 标准溶液时,烧杯中的溶液有少量溅出,则测定结果___________。
标准溶液时,烧杯中的溶液有少量溅出,则测定结果___________。| A.偏高 | B.偏低 | C.无影响 | D.无法判断 |
| A.偏高 | B.偏低 | C.无影响 | D.无法判断 |
您最近一年使用:0次
名校
5 . 利用 合成甲醇、二甲醚技术是有效利用
合成甲醇、二甲醚技术是有效利用 资源,实现“碳中和”目标的重要途径。
资源,实现“碳中和”目标的重要途径。
(1)开发 直接催化加氢合成二甲醚技术是很好的一个研究方向。
直接催化加氢合成二甲醚技术是很好的一个研究方向。
主反应: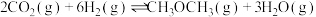

副反应:

①已知25℃和101kPa下,H2(g)、CO(g)的燃烧热 分别为-285.8kJ/mol、-283.0kJ/mol,
分别为-285.8kJ/mol、-283.0kJ/mol,
 ,则
,则
_______ kJ/mol。
②其他条件相同时,反应温度对 平衡转化率影响如图所示。温度低于280℃时,
平衡转化率影响如图所示。温度低于280℃时, 平衡转化率随温度的升高而减小的原因可能是
平衡转化率随温度的升高而减小的原因可能是_______ 。 ,反应平衡时测得
,反应平衡时测得 的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性
的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性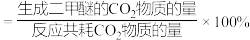 ),则副反应
),则副反应 的
的
_______ (保留两位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)利用 合成甲醇也是有效利用
合成甲醇也是有效利用 资源的重要途径。将原料气
资源的重要途径。将原料气 充入某一恒容密闭容器中,只发生
充入某一恒容密闭容器中,只发生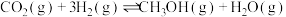
 ,在不同催化剂作用下,反应
,在不同催化剂作用下,反应 时
时 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。_______ 。
A.使用催化剂Ⅰ时,d点已达到平衡
B. 的平衡常数大于
的平衡常数大于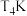 的平衡常数
的平衡常数
C.若a点时, ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度
D.c点转化率比a点低的原因一定是催化剂活性降低
②若图中a点时反应已达平衡,现原料气按 充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出
充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出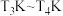 之间
之间 的平衡转化率变化曲线
的平衡转化率变化曲线______ 。
(3)水煤气变换反应的机理被广泛研究,其中有一种为羧基机理,某催化剂催化 (*表示吸附态、
(*表示吸附态、 表示活化能)步骤如下:
表示活化能)步骤如下:
Ⅰ.

Ⅱ._______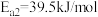
Ⅲ.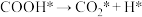

Ⅳ._______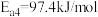
①请补充其中的一个反应式:Ⅱ_______ 。
②反应 的决速步骤是
的决速步骤是_______ (填序号)。
 合成甲醇、二甲醚技术是有效利用
合成甲醇、二甲醚技术是有效利用 资源,实现“碳中和”目标的重要途径。
资源,实现“碳中和”目标的重要途径。(1)开发
 直接催化加氢合成二甲醚技术是很好的一个研究方向。
直接催化加氢合成二甲醚技术是很好的一个研究方向。主反应:
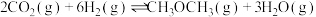

副反应:


①已知25℃和101kPa下,H2(g)、CO(g)的燃烧热
 分别为-285.8kJ/mol、-283.0kJ/mol,
分别为-285.8kJ/mol、-283.0kJ/mol,
 ,则
,则
②其他条件相同时,反应温度对
 平衡转化率影响如图所示。温度低于280℃时,
平衡转化率影响如图所示。温度低于280℃时, 平衡转化率随温度的升高而减小的原因可能是
平衡转化率随温度的升高而减小的原因可能是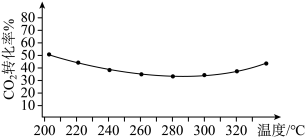
 ,反应平衡时测得
,反应平衡时测得 的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性
的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性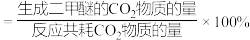 ),则副反应
),则副反应 的
的
(2)利用
 合成甲醇也是有效利用
合成甲醇也是有效利用 资源的重要途径。将原料气
资源的重要途径。将原料气 充入某一恒容密闭容器中,只发生
充入某一恒容密闭容器中,只发生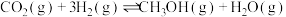
 ,在不同催化剂作用下,反应
,在不同催化剂作用下,反应 时
时 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。
A.使用催化剂Ⅰ时,d点已达到平衡
B.
 的平衡常数大于
的平衡常数大于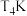 的平衡常数
的平衡常数C.若a点时,
 ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度D.c点转化率比a点低的原因一定是催化剂活性降低
②若图中a点时反应已达平衡,现原料气按
 充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出
充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出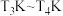 之间
之间 的平衡转化率变化曲线
的平衡转化率变化曲线(3)水煤气变换反应的机理被广泛研究,其中有一种为羧基机理,某催化剂催化
 (*表示吸附态、
(*表示吸附态、 表示活化能)步骤如下:
表示活化能)步骤如下:Ⅰ.


Ⅱ._______
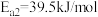
Ⅲ.
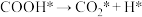

Ⅳ._______
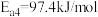
①请补充其中的一个反应式:Ⅱ
②反应
 的决速步骤是
的决速步骤是
您最近一年使用:0次
名校
解题方法
6 . 丙醛工业上主要用于制合成纤维、橡胶促进剂和防老剂等。在铑催化剂作用下与常用乙烯羰基化合成丙醛,涉及的反应如下:
主反应Ⅰ:C2H4(g)+H2(g)+CO(g) CH3CH2CHO(g) ΔH1
CH3CH2CHO(g) ΔH1
副反应Ⅱ:C2H4(g)+H2(g) CH3CH3(g) ΔH2
CH3CH3(g) ΔH2
已知:在一定条件下一氧化碳能与铑催化剂结合生成羰基铑络合物;丙醛选择性:x(CH3CH2CHO)= ×100%。
×100%。
回答下列问题:
(1)反应Ⅰ、Ⅱ以气体分压表示的平衡常数Kp与温度T变化关系如图所示。 CH3CH2CHO(g) ΔH
CH3CH2CHO(g) ΔH________ 0(填“>”、“<”或“=”), 的数值范围是
的数值范围是________ (填标号)。
A.<-1 B.-1~0 C.0~1 D.>1
(2)在T1℃、压强为150kPa条件下,在密闭反应器中,按照投料n(C2H4):n(CO):n(H2)=1:1∶1,发生上述反应,经tmin反应达到平衡,测得p(C2H4)=p(C2H6)=20kPa,则CH3CH2CHO(g)的选择性为________ %(保留小数点后一位),v(CO)=________ kPa/min(用含t的代数式表示),反应Ⅰ的逆反应的Kp=________ 。
(3)在恒压密闭容器中,在一定温度和铙催化剂作用下,发生上述反应,反应相同时间时,测得C2H4的转化率(α)和丙醛选择性随 变化关系如图所示。
变化关系如图所示。________ (填“C2H4的转化率”或“丙醛选择性”);
②当 小于1时,曲线b随
小于1时,曲线b随 的降低而降低的可能原因是
的降低而降低的可能原因是________ 。
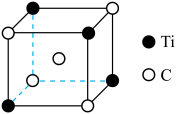
(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为______ 。
主反应Ⅰ:C2H4(g)+H2(g)+CO(g)
 CH3CH2CHO(g) ΔH1
CH3CH2CHO(g) ΔH1副反应Ⅱ:C2H4(g)+H2(g)
 CH3CH3(g) ΔH2
CH3CH3(g) ΔH2已知:在一定条件下一氧化碳能与铑催化剂结合生成羰基铑络合物;丙醛选择性:x(CH3CH2CHO)=
 ×100%。
×100%。回答下列问题:
(1)反应Ⅰ、Ⅱ以气体分压表示的平衡常数Kp与温度T变化关系如图所示。

 CH3CH2CHO(g) ΔH
CH3CH2CHO(g) ΔH 的数值范围是
的数值范围是A.<-1 B.-1~0 C.0~1 D.>1
(2)在T1℃、压强为150kPa条件下,在密闭反应器中,按照投料n(C2H4):n(CO):n(H2)=1:1∶1,发生上述反应,经tmin反应达到平衡,测得p(C2H4)=p(C2H6)=20kPa,则CH3CH2CHO(g)的选择性为
(3)在恒压密闭容器中,在一定温度和铙催化剂作用下,发生上述反应,反应相同时间时,测得C2H4的转化率(α)和丙醛选择性随
 变化关系如图所示。
变化关系如图所示。
②当
 小于1时,曲线b随
小于1时,曲线b随 的降低而降低的可能原因是
的降低而降低的可能原因是(4)最近发现一种由Ti原子和C原子构成的气态团簇分子如图所示,其化学式为
您最近一年使用:0次
解题方法
7 . 苯环的结构很稳定,常温下较难发生化学反应。某实验小组利用下列装置探究苯在一定条件下的反应产物。回答下列问题:
Ⅰ.实验室制取硝基苯常采用如图所示装置。___________ 。
②写出制取硝基苯的化学方程式:___________ 。
Ⅱ.该小组同学还设计了A、B、C三组实验装置用来制取溴苯。___________ ,三个装置中所共同发生的有机反应的化学方程式为___________ 。
(3)实验结束后,小明取装置A中锥形瓶中的水溶液少许,加入 溶液得到浅黄色沉淀,证明苯与溴发生了取代反应,该结论
溶液得到浅黄色沉淀,证明苯与溴发生了取代反应,该结论___________ (填“正确”或“错误”),原因是___________ 。
(4)装置B中足量 的作用是
的作用是___________ 。
Ⅰ.实验室制取硝基苯常采用如图所示装置。

②写出制取硝基苯的化学方程式:
Ⅱ.该小组同学还设计了A、B、C三组实验装置用来制取溴苯。

(3)实验结束后,小明取装置A中锥形瓶中的水溶液少许,加入
 溶液得到浅黄色沉淀,证明苯与溴发生了取代反应,该结论
溶液得到浅黄色沉淀,证明苯与溴发生了取代反应,该结论(4)装置B中足量
 的作用是
的作用是
您最近一年使用:0次
名校
解题方法
8 . 赤泥是氧化铝生产排放的固体废弃物。由赤泥(主要成分为 、
、 、
、 、
、 、
、 、
、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
(1)基态铝原子的核外电子排布式为_______ , 的空间构型是
的空间构型是_______ 。
(2)“焙烧”时,需将赤泥粉碎的目的是_______ 。
(3)“氧化”时发生反应的离子方程式为_______ ,向“氧化”后的溶液中滴加 溶液至
溶液至 ,生成沉淀。
,生成沉淀。
(4)为了测试所制得的聚合硫酸铝铁的性能,取某水样在不同 条件下加入PAFS
条件下加入PAFS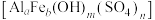 并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在偏酸性和偏碱性的
并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在偏酸性和偏碱性的 条件下,水样的去浊率均不高。试分析
条件下,水样的去浊率均不高。试分析 时,去浊率较低的可能原因为
时,去浊率较低的可能原因为_______ 。
 、
、 、
、 、
、 、
、 、
、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
(1)基态铝原子的核外电子排布式为
 的空间构型是
的空间构型是(2)“焙烧”时,需将赤泥粉碎的目的是
(3)“氧化”时发生反应的离子方程式为
 溶液至
溶液至 ,生成沉淀。
,生成沉淀。(4)为了测试所制得的聚合硫酸铝铁的性能,取某水样在不同
 条件下加入PAFS
条件下加入PAFS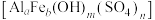 并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在偏酸性和偏碱性的
并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在偏酸性和偏碱性的 条件下,水样的去浊率均不高。试分析
条件下,水样的去浊率均不高。试分析 时,去浊率较低的可能原因为
时,去浊率较低的可能原因为
您最近一年使用:0次
名校
解题方法
9 . 化合物W是合成风湿性关节炎药物罗美昔布的一种中间体,其合成路线如下:
(1)B中具有的官能团的名称是_______ 。
(2)由C生成D的反应类型是_______ 。
(3)D→E和F→G的作用是_______ 。
(4)写出由G生成H的化学方程式_______ 。
(5)写出I的结构简式_______ 。
(6)X的同分异构体中,符合下列条件的有机物有_______ 种。
①只含两种官能团且不含甲基;②含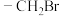 结构,不含C=C=C和环状结构。
结构,不含C=C=C和环状结构。
(7)设计由甲苯和 制备
制备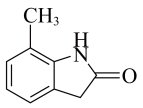 的合成路线
的合成路线_______ (试剂任选)。

已知:(ⅰ) 。
。
(ⅱ) 。
。
(1)B中具有的官能团的名称是
(2)由C生成D的反应类型是
(3)D→E和F→G的作用是
(4)写出由G生成H的化学方程式
(5)写出I的结构简式
(6)X的同分异构体中,符合下列条件的有机物有
①只含两种官能团且不含甲基;②含
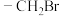 结构,不含C=C=C和环状结构。
结构,不含C=C=C和环状结构。(7)设计由甲苯和
 制备
制备 的合成路线
的合成路线
您最近一年使用:0次
名校
解题方法
10 . 烃A(结构简式:CH2=CHCH3)是有机化学工业的基本原料,可从石油中获得。烃A可发生如图所示的一系列化学反应。
(1)F的分子式为_______ 。
(2)B的名称是_______ ,可鉴别A、E两种物质的试剂是_______ (填一种)。
(3)C是A通过加聚反应制得的有机高分子材料,其结构简式为_______ 。
(4)G的官能团是_______ (填名称),D与F反应的化学方程式是_______ 。

(1)F的分子式为
(2)B的名称是
(3)C是A通过加聚反应制得的有机高分子材料,其结构简式为
(4)G的官能团是
您最近一年使用:0次