23-24高二下·全国·课前预习
解题方法
1 . 苯的分子结构
(1)分子式为_______ ,结构简式为 和
和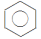 ,为
,为_______ 结构。
(2)化学键形成
苯分子中的6个碳原子均采取_______ 杂化,分别与氢原子及相邻碳原子以_______ 键结合,键间夹角均为120°,连接成六元环。每个碳碳键的键长相等,都是139 pm,介于______ 和______ 的键长之间。每个碳原子余下的_______ 轨道垂直于碳、氢原子构成的平面,相互平行重叠形成大_______ 键,均匀地对称分布在苯环平面的上下两侧。
(1)分子式为
 和
和 ,为
,为(2)化学键形成
苯分子中的6个碳原子均采取
您最近半年使用:0次
2 . 脱水反应
(1)在一定条件下,醇可以发生脱水反应,醇既可以分子内脱水得到___________ ,也可以分子间脱水得到___________ 。
(2)乙醇的脱水反应实验探究:
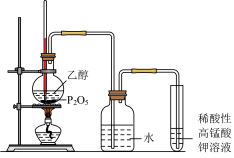
实验步骤:在圆底烧瓶中加入2 g P2O5并注入4 mL 95%的乙醇,加热,观察实验现象。
实验现象:广口瓶中有___________ 产生,酸性高锰酸钾溶液___________ 。
(3)乙醇的脱水反应:
乙醇在浓硫酸、磷酸、Al2O3(400℃左右)或P2O5等催化剂作用下发生脱水反应。实验室常采用乙醇和浓硫酸共热发生脱水反应来获得乙烯或乙醚。乙醇在浓硫酸作用下,加热到170 ℃,发生反应生成了乙烯,化学方程式为:___________ 。加热到140 ℃,发生反应生成了乙醚,化学方程式为:___________ 。
(4)消去反应:
在一定条件下,有机物分子内脱去一个或几个小分子生成不饱和化合物(含双键或三键)的反应,称为消去反应。
(1)在一定条件下,醇可以发生脱水反应,醇既可以分子内脱水得到
(2)乙醇的脱水反应实验探究:

实验步骤:在圆底烧瓶中加入2 g P2O5并注入4 mL 95%的乙醇,加热,观察实验现象。
实验现象:广口瓶中有
(3)乙醇的脱水反应:
乙醇在浓硫酸、磷酸、Al2O3(400℃左右)或P2O5等催化剂作用下发生脱水反应。实验室常采用乙醇和浓硫酸共热发生脱水反应来获得乙烯或乙醚。乙醇在浓硫酸作用下,加热到170 ℃,发生反应生成了乙烯,化学方程式为:
(4)消去反应:
在一定条件下,有机物分子内脱去一个或几个小分子生成不饱和化合物(含双键或三键)的反应,称为消去反应。
您最近半年使用:0次
解题方法
3 . 蒸馏
(1)蒸馏是分离和提纯_______ 有机化合物的常用方法。
(2)原理:利用混合物中各组分_______ 不同(一般有机物与杂质的沸点应相差30℃以上),达到分离液态混合物的目的。当液态混合物中含有多种沸点不同的有机物组分时,经过多次_______ 和_______ 可以将这些成分(馏分)逐步分离,这一过程称为分馏,如石油的分馏等。
(3)优点:蒸馏的优点是不需要使用混合物组分以外的其他溶剂,_______ 引入新的杂质。
(4)实验装置
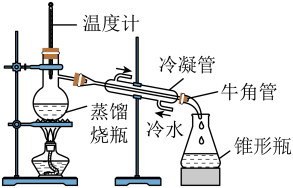
注意事项:
①温度计水银球位于_______ 。
②碎瓷片的作用:_______ 。
③冷凝管中水流的方向是下口进入,上口流出。
(1)蒸馏是分离和提纯
(2)原理:利用混合物中各组分
(3)优点:蒸馏的优点是不需要使用混合物组分以外的其他溶剂,
(4)实验装置

注意事项:
①温度计水银球位于
②碎瓷片的作用:
③冷凝管中水流的方向是下口进入,上口流出。
您最近半年使用:0次
解题方法
4 . 滴定管的使用方法
(1)检查:使用前先检查滴定管活塞___________ 。
(2)润洗:在加入酸、碱液之前,应使用待装的酸、碱溶液分别润洗滴定管内壁___________ 次。
(3)装液:注入待装的酸、碱溶液至滴定管___________ 处。
(4)排气泡:酸式滴定管快速打开活塞冲走气泡,碱式滴定管将橡胶管向上弯曲,挤压玻璃球,赶走气泡,使滴定管尖嘴部分___________ 。
(5)调液面:调整管中液面至___________ 以下,记录读数V0.滴定管的读数时,视线、刻度线、凹液面在___________ 上。
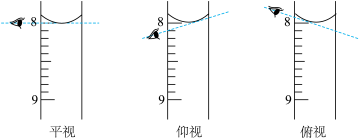
(6)滴定:左手控制活塞或玻璃小球,右手摇动锥形瓶,两眼注视___________ 的变化。滴定过程中,滴加速度___________ ,接近终点时,应逐渐___________ 滴加速度。
(7)终点的判断:最后一滴恰好使指示剂颜色发生___________ 且___________ 不变色,即为滴定终点。滴加完毕记录读数V1,消耗溶液的体积为___________ 。
(1)检查:使用前先检查滴定管活塞
(2)润洗:在加入酸、碱液之前,应使用待装的酸、碱溶液分别润洗滴定管内壁
(3)装液:注入待装的酸、碱溶液至滴定管
(4)排气泡:酸式滴定管快速打开活塞冲走气泡,碱式滴定管将橡胶管向上弯曲,挤压玻璃球,赶走气泡,使滴定管尖嘴部分
(5)调液面:调整管中液面至

(6)滴定:左手控制活塞或玻璃小球,右手摇动锥形瓶,两眼注视
(7)终点的判断:最后一滴恰好使指示剂颜色发生
您最近半年使用:0次
5 . 实验探究温度变化对化学平衡的影响
| 实验步骤 | ①取一支试管向其中加入少量CoCl2晶体,加入浓盐酸使其全部溶解; ②加水至溶液呈紫色; ③将上述溶液分别装于三支试管中,分别置于热水、冰水和室温下 |
| 实验现象 | 室温下试管内液体呈 |
| 结论(平衡移动的方向) | 室温平衡 |
您最近半年使用:0次
6 . 铜锌原电池
(1)【实验探究】
【实验1】向CuSO4溶液中加入适量锌粉,用温度计测量溶液的温度。
【实验2】将用导线与电流计相连接的锌片和铜片分别插入ZnSO4和CuSO4溶液中,将盐桥插入两只烧杯的电解质溶液中,观察实验现象;取出盐桥,再观察实验现象。
(2)结论:实验1的能量变化的主要形式为___________ 能转化为___________ 能;实验2的能量变化的主要形式为___________ 能转化为___________ 能。
(3)铜锌原电池的工作原理
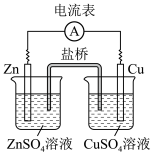
Zn片为___________ 极,电极反应式为___________ ,反应类型是___________ 反应。
Cu片为___________ 极,电极反应式为_ ,反应类型是___________ 反应。
总反应式为___________ 。
电子的流动方向:___________ →导线→___________ 。
盐桥中K+移向___________ 溶液,Cl-移向___________ 溶液。
(1)【实验探究】
【实验1】向CuSO4溶液中加入适量锌粉,用温度计测量溶液的温度。
【实验2】将用导线与电流计相连接的锌片和铜片分别插入ZnSO4和CuSO4溶液中,将盐桥插入两只烧杯的电解质溶液中,观察实验现象;取出盐桥,再观察实验现象。
| 实验现象 | 实验结论 | |
| 实验1 | ||
| 实验2 | 插入盐桥:① ② ③ | |
| 取出盐桥: |
(3)铜锌原电池的工作原理

Zn片为
Cu片为
总反应式为
电子的流动方向:
盐桥中K+移向
您最近半年使用:0次
7 . 19世纪60年代,德国化学家凯库勒在梦中“看见”苯分子中原子的排列顺序,提出了两点假设。
i.苯的六个碳原子形成闭合环状,即平面六边形;

ii.每个碳原子均连接一个氢原子,各碳原子间存在着单、双键交替形式。
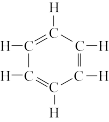
【交流研讨】
(1)如果苯分子为上述结构,则其可能具有什么重要的化学性质_________ ?若存在碳碳双键,则性质应与乙烯性质相似
(2)能否设计实验方案来证明________ ?
i.苯的六个碳原子形成闭合环状,即平面六边形;

ii.每个碳原子均连接一个氢原子,各碳原子间存在着单、双键交替形式。

【交流研讨】
(1)如果苯分子为上述结构,则其可能具有什么重要的化学性质
(2)能否设计实验方案来证明
您最近半年使用:0次
8 . 从海带中提取碘的简单流程如下:
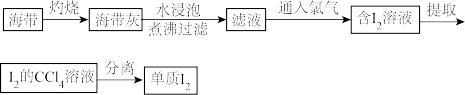
(1)灼烧时应在什么仪器中进行:________ 。
(2)滤液中通入氯气得到含I2溶液,写出反应的离子方程式________ ;氯气通常可用________ 试剂替代。
(3)如何检验通入氯气后所得溶液中含有I2:________ 。

(1)灼烧时应在什么仪器中进行:
(2)滤液中通入氯气得到含I2溶液,写出反应的离子方程式
(3)如何检验通入氯气后所得溶液中含有I2:
您最近半年使用:0次
9 . 工艺流程

相关反应的方程式
(1)分解贝壳制取氢氧化钙:①___________ ;②___________ 。
(2)沉淀镁离子:__________ 。
(3)制备氯化镁:___________ 。
(4)制取金属镁:___________ 。

相关反应的方程式
(1)分解贝壳制取氢氧化钙:①
(2)沉淀镁离子:
(3)制备氯化镁:
(4)制取金属镁:
您最近半年使用:0次
10 . 从海水中提取溴的简单工艺流程如下:
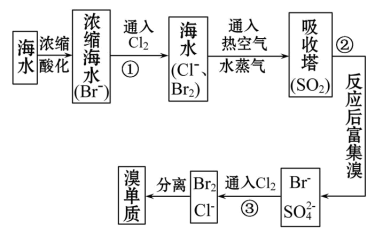
(1)上述工艺中设计步骤①、③这两步操作的目的是:___________ 。
(2)有人说步骤①通入氯气氧化后直接用有机溶剂萃取出溴即可,你认为此建议是否合理:___________ 。
(3)利用空气吹出法提取溴是利用了溴的什么性质:___________ 。

(1)上述工艺中设计步骤①、③这两步操作的目的是:
(2)有人说步骤①通入氯气氧化后直接用有机溶剂萃取出溴即可,你认为此建议是否合理:
(3)利用空气吹出法提取溴是利用了溴的什么性质:
您最近半年使用:0次



