解题方法
1 . 物质转化可以制备人类生活和生产所需要的新物质。A、B、C、D、E均为中学化学常见物质,其中A、C、D、E中含有同一种元素。A是一种有毒的气体单质,C的水溶液呈绿色(浓度低时呈蓝色),D是一种常用的调味品,E的水溶液 。它们之间的转化关系如下(部分反应物、生成物和反应条件已省略)。
。它们之间的转化关系如下(部分反应物、生成物和反应条件已省略)。

请回答下列问题:
(1)A的化学式是___________ 。
(2)A→C的反应现象是___________ 。
(3)C→D的离子方程式是___________ 。
(4)A→E的化学方程式是___________ 。
(5)E的水溶液可以与___________ 反应生成C。
 。它们之间的转化关系如下(部分反应物、生成物和反应条件已省略)。
。它们之间的转化关系如下(部分反应物、生成物和反应条件已省略)。
请回答下列问题:
(1)A的化学式是
(2)A→C的反应现象是
(3)C→D的离子方程式是
(4)A→E的化学方程式是
(5)E的水溶液可以与
您最近一年使用:0次
2 . 下列诗句中对所涉及物质的性质、现象或变化的描述错误的是
| A.“钻石恒久远,颗永流传”说明了常温下碳的化学性质稳定 |
| B.“炉火照天地,红星乱紫烟”形象地描写了金属的冶炼过程 |
| C.“掬月水在手,弄花香满衣”诗文中隐含着化学变化 |
| D.“遥知不是雪,为有暗香来”说明了分子在不停地运动 |
您最近一年使用:0次
2021-10-26更新
|
233次组卷
|
3卷引用:山西省运城市2021-2022学年高三上学期10月质量检测化学试题
名校
3 . 硫酸是一种重要的基本化工产品。接触法制硫酸生产中的氧化工序为: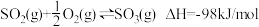 ,回答下列问题:
,回答下列问题:
(1)若将物质的量之比为2:1的SO2(g)和O2(g)通入恒温恒容反应器,下列能判断反应达到平衡的是___________。
(2)据图(a),请写出VOSO4(s)和V2O4(s)反应生成V2O5(s)与SO2(g)的热化学方程式为___________ 。
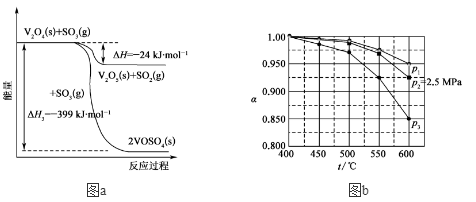
(3)若当SO2、O2、N2(不参与反应)起始的物质的量分数分别为10%、15%和75%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α随温度的变化如图(b)所示。反应在0.5MPa、550℃时的α=______ ,判断的依据是______ 。下列因素中能影响α的因素有_______ 。
A.压强B.反应物的组成 C.催化剂D.温度
(4)若将物质的量之比为2:1的SO2(g)和O2(g)通入反应器,在恒温t、恒压p条件下进行反应。平衡时,若SO2转化率为α,则SO3压强为___________ ,平衡常数Kp=___________ (以分压表示,分压=总压 物质的量分数)。
物质的量分数)。
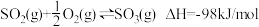 ,回答下列问题:
,回答下列问题:(1)若将物质的量之比为2:1的SO2(g)和O2(g)通入恒温恒容反应器,下列能判断反应达到平衡的是___________。
| A.SO2(g)和O2(g)的转化率为2:1时 |
| B.容器内混合气体的压强不再改变 |
| C.容器内混合气体的平均相对分子质量不再改变 |
| D.生成2mol SO3(g)的同时消耗1mol O2(g) |

(3)若当SO2、O2、N2(不参与反应)起始的物质的量分数分别为10%、15%和75%时,在0.5MPa、2.5MPa和5.0MPa压强下,SO2平衡转化率α随温度的变化如图(b)所示。反应在0.5MPa、550℃时的α=
A.压强B.反应物的组成 C.催化剂D.温度
(4)若将物质的量之比为2:1的SO2(g)和O2(g)通入反应器,在恒温t、恒压p条件下进行反应。平衡时,若SO2转化率为α,则SO3压强为
 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
2021-10-17更新
|
406次组卷
|
3卷引用:山西省运城市2021~2022学年高二上学期10月份月考化学试卷
4 . 钴( )的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是
)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是
 )的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是
)的合金材料广泛应用于航空航天、机械制造等领域。如图为水溶液中电解制备金属钴的装置示意图。下列说法正确的是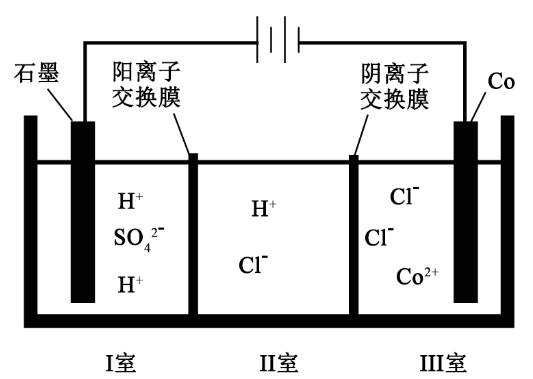
A.工作时,Ⅰ室和Ⅱ室溶液的 均增大 均增大 |
B.生成 ,Ⅰ室溶液质量理论上减少 ,Ⅰ室溶液质量理论上减少 |
| C.移除两交换膜后,石墨电极上发生的反应不变 |
D.电解总反应: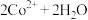  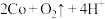 |
您最近一年使用:0次
2021-06-11更新
|
18016次组卷
|
58卷引用:山西省晋城市第一中学2021-2022学年高二上学期12月月考化学试题
山西省晋城市第一中学2021-2022学年高二上学期12月月考化学试题2021年新高考广东化学高考真题(已下线)课时31 新型电解池装置-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点22 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第17讲 电解池 金属的腐蚀与防护(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题讲座(四)新型电源及电极反应式的书写 (讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)考向20 电解池 金属的腐蚀与防护-备战2022年高考化学一轮复习考点微专题山东省枣庄市薛城区2021-2022学年高二上学期期中考试化学试题(已下线)专题08 电化学之电解池-【微专题·大素养】备战2022年高考化学讲透提分要点河北省石家庄市第二中学2022届高三上学期11月第三次考试化学试题(已下线)专题11 电化学-备战2022年高考化学学霸纠错(全国通用)2021年广东省高考化学试卷变式题11-21山东省济南市莱芜第一中学2021-2022学年高三上学期期中考试化学试题(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密08 化学反应与能量(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-讲义(已下线)专题11 电化学-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)卷08 电化学及其应用-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点03 电化学基础知识-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)押新高考卷12题 电化学基础-备战2022年高考化学临考题号押题(新高考通版)湖南省岳阳市湘阴县第一中学2021-2022学年高三下学期期中考试化学试题江苏省镇江市五校2021-2022学年高二下学期期末考试化学试题(已下线)专题08 电化学及其应用-三年(2020-2022)高考真题分项汇编(已下线)微专题10 “守恒法”在氧化还原反应计算中的应用-备战2023年高考化学一轮复习考点微专题(已下线)考点19 电解池-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第35练 电解池-2023年高考化学一轮复习小题多维练(全国通用)(已下线)微专题32 电化学中的交换膜-备战2023年高考化学一轮复习考点微专题(已下线)微专题33 四步敲定高考新情景电池电极反应式的书写-备战2023年高考化学一轮复习考点微专题广东省深圳市重点中学2021-2022学年高二上学期期末考试化学试题第二节 电解池 第2课时 电解原理的应用(已下线)微专题35 电化学“多池和多室”串联问题及计算-备战2023年高考化学一轮复习考点微专题(已下线)第17讲 电解池 金属的腐蚀与防护 (讲)-2023年高考化学一轮复习讲练测(新教材新高考)陕西省渭南高级中学2021-2022学年高一下学期第三阶段考试化学试题山东省青岛第一中学2022-2023学年高二上学期期中考试化学试题重庆市永川北山中学校2022-2023学年高三上学期期中质量监测化学试题(已下线)专题05 化学能与电能的转化(练)-2023年高考化学二轮复习讲练测(新高考专用)广东省广州大学附属中学2022-2023学年高二上学期期末考试化学试题(已下线)专题16 新型电化学装置分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第六章 化学反应与能量 第39讲 多池、多室的电化学装置(已下线)题型21 三室膜电解装置及其应用(已下线)专题七 电化学中“离子交换膜”的应用(练习)吉林省吉林市普通高中友好学校2022-2023学年高二上学期期末考试化学试题(已下线)专题卷16 离子隔膜在电化学中的应用-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)题型20 三室膜电解装置及其应用(已下线)专题12 电化学的综合应用(已下线)专题12 电化学的综合应用微专题(16) 电解在物质制备和提纯中的应用(已下线)考点19 电解池(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第4讲 电解池 金属的电化学腐蚀与防护(已下线)考点2 原电池 新型电源(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点3 电解池 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)福建省三明第一中学2022-2023学年高三上学期期中考试化学试题云南省中央民族大学附属中学昆明五华实验学校2023-2024学年高二上学期期中考试化学试题北京市中国人民大学附属中学2021-2022学年高三下学期开学考试化学试卷四川省绵阳市东辰学校2023-2024学年高二上学期第四次月考化学试题 2023届河南省南阳市六校高三下学期第一次联考化学试卷
5 . 在实验室采用如图装置制备气体,合理的是
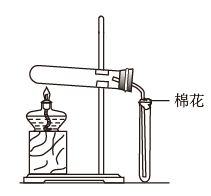
| 化学试剂 | 制备的气体 | |
| A | 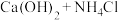 |  |
| B | 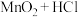 (浓) (浓) |  |
| C | 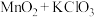 |  |
| D | 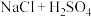 (浓) (浓) |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-09更新
|
21804次组卷
|
50卷引用:山西省实验中学2021-2022学年高二下学期开学分班素质测试化学试题
山西省实验中学2021-2022学年高二下学期开学分班素质测试化学试题山西省实验中学2021-2022学年高二上学期开学考试化学试题2021年高考全国乙卷化学真题河南省三门峡市实验高中2020-2021学年高二下学期6月月考化学试题河北省辛集中学 2020-2021学年高二下学期期末考试化学试题(已下线)第29讲 化学综合实验(精练)-2022年高考化学一轮复习讲练测(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点34 物质的制备与合成-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时53 简单实验方案的设计与评价-2022年高考化学一轮复习小题多维练(全国通用)四川省眉山市彭山区第一中学2021-2022学年高二上学期入学考试化学试题宁夏中卫市中宁县第一中学2021-2022学年高三上学期第一次月考化学试题四川省邻水实验学校2021-2022学年高二上学期第一次月考化学试题内蒙古北京八中乌兰察布分校2021-2022学年高三上学期学科素养评估一化学试题(已下线)专题13 化学实验-备战2022年高考化学学霸纠错(全国通用)(已下线)第29讲 常见气体的制备与性质实验(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)2021年高考全国乙卷化学试题变式题(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练安徽省亳州市第五完全中学2021-2022学年高三上学期期中考试化学试题(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题05 化学基础实验—2022年高考化学二轮复习讲练测(全国版)-练习陕西省西北农林科技大学附属中学2021-2022学年高一上学期期末考试化学试题(已下线)秘籍04 实验仪器使用与基本操作-备战2022年高考化学抢分秘籍(全国通用)(已下线)卷01 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押全国卷理综第9题 化学实验基础-备战2022年高考化学临考题号押题(课标全国卷)(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题11 基本实验专练(已下线)专题11化学实验基础-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题11化学实验基础-五年(2018~2022)高考真题汇编(全国卷)(已下线)微专题24 氯气、氨气、二氧化硫的实验室制备与应用-备战2023年高考化学一轮复习考点微专题(已下线)考点51 物质的制备-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(练)-2023年高考化学一轮复习讲练测(全国通用)安徽省砀山县第四中学2022-2023学年高三上学期第一次月考化学试题(已下线)第27讲 物质的制备与性质实验(讲)-2023年高考化学一轮复习讲练测(新教材新高考)甘肃省张掖市高台县第一中学2022-2023学年高一上学期期中考试化学试题湖南省郴州市汝城县第一中学2022-2023学年高一上学期期中考试化学试题安徽省六安市裕安区新安中学2022-2023学年高三上学期第三次月考化学试题(已下线)专题23 化学实验基础性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价第四章 非金属及其化合物 第24讲 常见气体的实验室制备、净化和收集(已下线)素养卷07 微型物质制备方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题04 常见气体的实验室制取(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)(已下线)微专题 常见气体的实验室制备、净化和收集(已下线)考点44 化学实验基础(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)云南省开远市第一中学校2023-2024学年高一上学期9月半月考试化学试题(已下线)第3讲 物质制备实验的设计与评价章末知识整合黑龙江省大庆市肇州县第二中学2023-2024学年高三上学期11月月考化学试题吉林省通化市辉南县第六中学2023-2024学年高一下学期3月半月考化学试卷
名校
解题方法
6 . 化合物H是丁苯酞在体内代谢的一种产物,其保有丁苯酞的生物活性,具有增加缺血区的血流量、缩小脑梗塞面积以及修复神经功能性缺失症状的功能,其合成路线如下:

已知:①氯铬酸吡啶盐(Pyridinium Chlorochromate;PCC)是一种氧化剂。
②N-溴代丁二酰亚胺(NBS)是一种溴代试剂,有反应条件温和、操作方便、反应选择性高、副反应少的优点。
(1)A可由化合物 (I)在高温条件下发生分子内脱水形成,化合物I的化学名称为
(I)在高温条件下发生分子内脱水形成,化合物I的化学名称为___________ 。
(2)G中官能团的名称是___________ 。
(3)B→C的反应类型为___________ ,F→G的反应类型为___________ 。
(4)用*号标出化合物H中的手性碳原子___________ ,写出H与NaOH溶液反应的化学方程式:___________ 。
(5)化合物D的同分异构体中能同时满足以下条件的是___________ (写出其中一种的结构简式)。
I.能发生银镜反应;II.遇FeCl3溶液显紫色;III.在核磁共振氢谱中有6组峰,且峰面积相同。
(6)根据所学知识及题给信息,以丙酮为原料合成BrCH2CH=CH2(无机试剂和有机溶剂任选,合成路线示例见本题题干)___________ 。

已知:①氯铬酸吡啶盐(Pyridinium Chlorochromate;PCC)是一种氧化剂。
②N-溴代丁二酰亚胺(NBS)是一种溴代试剂,有反应条件温和、操作方便、反应选择性高、副反应少的优点。
(1)A可由化合物
 (I)在高温条件下发生分子内脱水形成,化合物I的化学名称为
(I)在高温条件下发生分子内脱水形成,化合物I的化学名称为(2)G中官能团的名称是
(3)B→C的反应类型为
(4)用*号标出化合物H中的手性碳原子
(5)化合物D的同分异构体中能同时满足以下条件的是
I.能发生银镜反应;II.遇FeCl3溶液显紫色;III.在核磁共振氢谱中有6组峰,且峰面积相同。
(6)根据所学知识及题给信息,以丙酮为原料合成BrCH2CH=CH2(无机试剂和有机溶剂任选,合成路线示例见本题题干)
您最近一年使用:0次
2021-05-11更新
|
236次组卷
|
2卷引用:山西省晋中市2021届高三下学期5月统一模拟考试(三模) 理综化学试题
7 . 元素周期表中第四周期某些过渡元素(如Ti、Mn、Zn等)在生产生活中有着广泛的应用。回答下列问题:
(1)钛的应用越来越受到人们的关注。
①第四周期元素中,基态原子的未成对电子数与钛相同的有___________ (填元素符号)。
②钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是___________ 。
(2)锰及其化合物的应用研究是前沿科学之一
①已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列___________ (选填字母编号)。
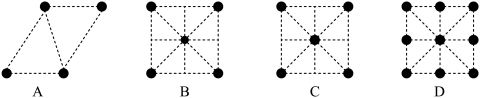
②三醋酸锰[(CH3COO)3Mn]是一种很好的有机反应氧化剂。三醋酸锰[(CH3COO)3Mn]中阳离子的价层电子排布式中电子的自旋状态___________ (填“相同”或“相反”)。
③Mn2+能形成配离子为八面体的配合物MnClm·nNH3,在该配合物的配离子中,Mn2+位于八面体的中心。若含1 mol该配合物的溶液与足量AgNO3溶液作用可生成l mol AgCl沉淀,则该配离子化学式为___________ 。
(3)比较Fe和Mn的第三电离能,I3(Fe)___________ I3(Mn)(填“大于”或“小于”),原因是___________ 。
(4)某钙钛型复合氧化物如图,以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有巨磁电阻效应。

已知La为+3价,当被钙等+2价元素A替代时,可形成复合钙钛矿化合物LaxA1-xMnO3,(x>0.9),此时一部分+3价锰转变为+4价,导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁转变及金属-半导体的转变,则复合钙钛矿化合物中+3价锰与+4价锰的物质的量之比为___________ (用含x的代数式表示)。
(5)具有较高催化活性的材料金红石的晶胞结构如图所示。已知该晶体的密度为d g·cm-3,Ti、O原子半径分别为a pm和b pm,阿伏加德罗常数的值为NA,则金红石晶体的空间利用率为___________ (列出计算式)。

(1)钛的应用越来越受到人们的关注。
①第四周期元素中,基态原子的未成对电子数与钛相同的有
②钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是
(2)锰及其化合物的应用研究是前沿科学之一
①已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列

②三醋酸锰[(CH3COO)3Mn]是一种很好的有机反应氧化剂。三醋酸锰[(CH3COO)3Mn]中阳离子的价层电子排布式中电子的自旋状态
③Mn2+能形成配离子为八面体的配合物MnClm·nNH3,在该配合物的配离子中,Mn2+位于八面体的中心。若含1 mol该配合物的溶液与足量AgNO3溶液作用可生成l mol AgCl沉淀,则该配离子化学式为
(3)比较Fe和Mn的第三电离能,I3(Fe)
(4)某钙钛型复合氧化物如图,以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有巨磁电阻效应。

已知La为+3价,当被钙等+2价元素A替代时,可形成复合钙钛矿化合物LaxA1-xMnO3,(x>0.9),此时一部分+3价锰转变为+4价,导致材料在某一温度附近有反铁磁-铁磁、铁磁-顺磁转变及金属-半导体的转变,则复合钙钛矿化合物中+3价锰与+4价锰的物质的量之比为
(5)具有较高催化活性的材料金红石的晶胞结构如图所示。已知该晶体的密度为d g·cm-3,Ti、O原子半径分别为a pm和b pm,阿伏加德罗常数的值为NA,则金红石晶体的空间利用率为

您最近一年使用:0次
2021-04-28更新
|
717次组卷
|
4卷引用:山西省临汾市2021届高三下学期3月考前适应性训练考试(二)化学试题
山西省临汾市2021届高三下学期3月考前适应性训练考试(二)化学试题(已下线)押全国卷理综第35题 物质结构与性质-备战2021年高考化学临考题号押题湖南省大联考雅礼十六校2021-2022学年高三第二次联考化学试题(已下线)专题二十一物质结构与性质解题策略



