1 . 实验室可用如图装置(略去部分夹持仪器)制取 并验证其性质。
并验证其性质。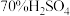 溶液的仪器名称为
溶液的仪器名称为_______ 。
(2)装置 的作用之一是通过观察产生气泡的多少判断
的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择_______(填字母)。
生成的快慢,其中的液体最好选择_______(填字母)。
(3) 试管中的试剂可以验证二氧化硫的氧化性,现象为
试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。经测定,产物中还有一种相对分子质量为104的酸式盐,则该反应的离子方程式为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管 中的溶液分成三份,分别进行如下实验:
中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案_______ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管 中
中 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(5)装置 的作用是
的作用是_______ 。装置 中为
中为_______ 溶液。
 并验证其性质。
并验证其性质。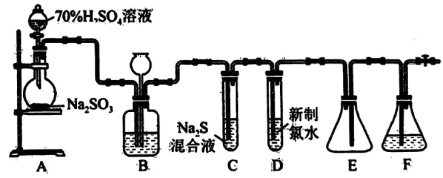
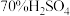 溶液的仪器名称为
溶液的仪器名称为(2)装置
 的作用之一是通过观察产生气泡的多少判断
的作用之一是通过观察产生气泡的多少判断 生成的快慢,其中的液体最好选择_______(填字母)。
生成的快慢,其中的液体最好选择_______(填字母)。| A.蒸馏水 | B.饱和 溶液 溶液 | C.饱和 溶液 溶液 | D.饱和 溶液 溶液 |
 试管中的试剂可以验证二氧化硫的氧化性,现象为
试管中的试剂可以验证二氧化硫的氧化性,现象为(4)为验证二氧化硫的还原性,充分反应后,取试管
 中的溶液分成三份,分别进行如下实验:
中的溶液分成三份,分别进行如下实验:方案Ⅰ:向第一份溶液中加入
 溶液,有白色沉淀生成;
溶液,有白色沉淀生成;方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。上述方案中能达到实验目的的是方案
 中
中 发生反应的离子方程式为
发生反应的离子方程式为(5)装置
 的作用是
的作用是 中为
中为
您最近一年使用:0次
名校
解题方法
2 . 下图中实验装置能达到相应实验目的的是
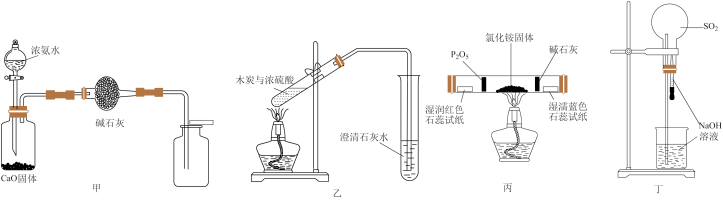
| A.装置甲可用于制备并收集少量干燥氨气 |
B.装置乙可用于验证反应是否有 生成 生成 |
| C.装置丙可用于检验氯化铵受热分解生成的两种气体 |
| D.装置丁可进行喷泉实验 |
您最近一年使用:0次
2023-03-18更新
|
992次组卷
|
8卷引用:安徽省淮南二中2023-2024学年高一下学期期中教学检测化学试题
名校
3 . 用下列装置能达到实验目的的是
A. 清洗铜与浓硫酸反应后有残液的试管 清洗铜与浓硫酸反应后有残液的试管 |
B. 配制一定物质的量浓度的溶液实验中,为定容时的操作 配制一定物质的量浓度的溶液实验中,为定容时的操作 |
C.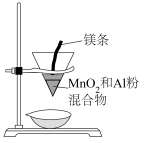 装置制取金属锰 装置制取金属锰 |
D.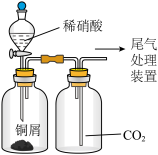 装置为制备并用排气法收集NO气体的装置 装置为制备并用排气法收集NO气体的装置 |
您最近一年使用:0次
2019-05-28更新
|
630次组卷
|
4卷引用:安徽省淮南四中2020届高三年级上学期第三次段考理综化学试题
安徽省淮南四中2020届高三年级上学期第三次段考理综化学试题【市级联考】河南省新乡市2019届高三下学期第三次模拟测试理科综合化学试题(已下线)第3章 金属及其化合物 单元测试(测)——2020年高考化学一轮复习讲练测上海理工大学附属储能中学2021-2022学年高三下学期第三次模拟考试化学试题
名校
解题方法
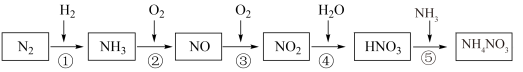
4 . 氮元素及其化合物的转化关系如图所示:___________ ,写出 的电子式
的电子式___________ 。
(2)浓、稀 的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:
的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:___________ 。
(3)氮氧化物 是大气污染物之一,处理
是大气污染物之一,处理 对于环境保护具有重要的意义。在一定条件下
对于环境保护具有重要的意义。在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。 ,反应的化学方程式为
,反应的化学方程式为___________ ;装置B内的试剂是___________ 。
②在装置 中
中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中  和
和 的物质的量之比为
的物质的量之比为___________ 。
③工厂里常采用 溶液吸收
溶液吸收 的混合气体,使其转化为化工产品
的混合气体,使其转化为化工产品 ,试写出其化学方程式:
,试写出其化学方程式:___________ 。
④用不同浓度的 溶液吸收
溶液吸收 含量不同的尾气,关系如图:(
含量不同的尾气,关系如图:( 表示尾气里
表示尾气里 中
中 的含量)
的含量) 含量越大,氮氧化物的吸收率越大,当
含量越大,氮氧化物的吸收率越大,当 小于
小于 时,加入
时,加入  能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是___________ 。
(4) 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:___________ (写出操作步骤、现象和结论)。
 的电子式
的电子式(2)浓、稀
 的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:
的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:(3)氮氧化物
 是大气污染物之一,处理
是大气污染物之一,处理 对于环境保护具有重要的意义。在一定条件下
对于环境保护具有重要的意义。在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。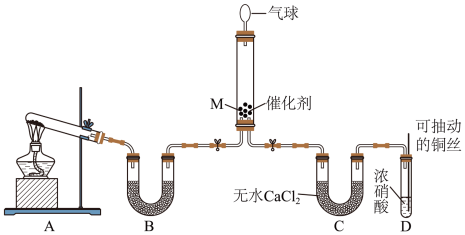
 ,反应的化学方程式为
,反应的化学方程式为②在装置
 中
中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中  和
和 的物质的量之比为
的物质的量之比为③工厂里常采用
 溶液吸收
溶液吸收 的混合气体,使其转化为化工产品
的混合气体,使其转化为化工产品 ,试写出其化学方程式:
,试写出其化学方程式:④用不同浓度的
 溶液吸收
溶液吸收 含量不同的尾气,关系如图:(
含量不同的尾气,关系如图:( 表示尾气里
表示尾气里 中
中 的含量)
的含量)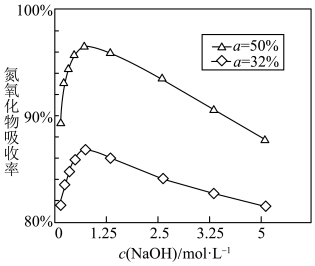
 含量越大,氮氧化物的吸收率越大,当
含量越大,氮氧化物的吸收率越大,当 小于
小于 时,加入
时,加入  能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是(4)
 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
您最近一年使用:0次
5 . 铜在生活中有广泛的应用。CuCl2和CuCl是两种常见的盐,广泛应用于工业生产。
I. CuCl2固体遇水易水解。实验室用如图所示的实验仪器及药品来制备纯净、干燥的氯气,并与粗铜(含杂质铁)反应制备氯化铜(铁架台、铁夹及酒精灯省略)。
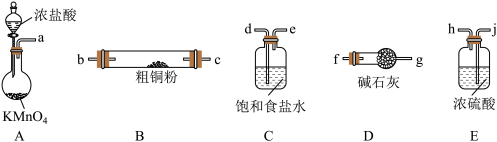
(1)写出装置A中,发生反应的化学反应方程式:____ ,装置C的作用是____
(2)完成上述实验,按气流方向连接各仪器接口的顺序是a→___ 。(每种仪器限使用一次)
(3)上述D装置的作用是____
Ⅱ. CuCl是应用广泛的有机合成催化剂,可采取不同方法制取。CuCl晶体呈白色,露置于潮湿空气中易被氧化。
方法一:向上述制得的氯化铜溶液中通入SO2,加热一段时间即可制得CuCl,写出该反应的离子方程式:___ 。
方法二:铜粉还原CuSO4溶液

已知:CuCl难溶于水和乙醇,在水溶液中存在平衡:CuCl(白色)+2Cl-⇌[CuCl3]2-(无色溶液)。
(1)①中,“加热”温度不宜过高和过低,目的是___ ,当观察到__ 现象,即表明反应已经完全。
(2)②中,加入大量水的作用是___ 。(从平衡角度解释)
I. CuCl2固体遇水易水解。实验室用如图所示的实验仪器及药品来制备纯净、干燥的氯气,并与粗铜(含杂质铁)反应制备氯化铜(铁架台、铁夹及酒精灯省略)。

(1)写出装置A中,发生反应的化学反应方程式:
(2)完成上述实验,按气流方向连接各仪器接口的顺序是a→
(3)上述D装置的作用是
Ⅱ. CuCl是应用广泛的有机合成催化剂,可采取不同方法制取。CuCl晶体呈白色,露置于潮湿空气中易被氧化。
方法一:向上述制得的氯化铜溶液中通入SO2,加热一段时间即可制得CuCl,写出该反应的离子方程式:
方法二:铜粉还原CuSO4溶液

已知:CuCl难溶于水和乙醇,在水溶液中存在平衡:CuCl(白色)+2Cl-⇌[CuCl3]2-(无色溶液)。
(1)①中,“加热”温度不宜过高和过低,目的是
(2)②中,加入大量水的作用是
您最近一年使用:0次
2019-09-23更新
|
331次组卷
|
4卷引用:安徽省淮南市寿县一中2020 届高三素质测试化学试题
名校
解题方法
6 . 下列装置用于实验室制氨气或验证氨气的化学性质,其中能达到实验目的的是
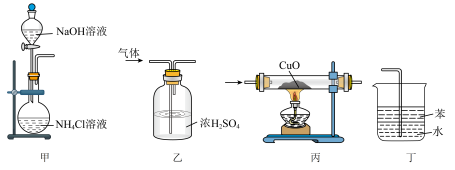
| A.用装置甲制取氨气 | B.用装置乙除去氨气中的水蒸气 |
| C.用装置丙验证氨气具有还原性 | D.用装置丁吸收尾气 |
您最近一年使用:0次
2024-05-05更新
|
263次组卷
|
13卷引用:安徽省淮南市第二中2023-2024学年高一下学期第一次月考化学试题
安徽省淮南市第二中2023-2024学年高一下学期第一次月考化学试题云南省开远市第一中学校2022-2023学年高一下学期期中考试化学试题四川省什邡中学2022-2023学年高一下学期第一次月考化学试题江苏省泰州市2023-2024学年高一上学期1月期末化学试题(已下线)专题03 常见气体的实验室制取(考点清单)(讲+练)-2023-2024学年高一化学下学期期中考点大串讲(人教版2019必修第二册)湖北省武汉市第十二中学2023-2024学年高一下学期3月月考化学试题广东省潮州市饶平县第二中学2023-2024学年高一下学期第一次月考化学试题江西省南昌十九中2022-2023学年高一下学期3月第一次月考化学试卷山东省济宁市微山县第二中学2023-2024学年高一下学期第一次月考化学试题江苏省扬州中学2023-2024学年高一下学期4月期中考试化学试题四川省射洪中学校2023-2024学年高一下学期4月第一次月考化学试题北京市育英学校2023-2024学年高一上学期期末考试化学试题湖北省咸宁市崇阳县第二高级中学2023-2024学年高一下学期3月月考化学试题
名校
解题方法
7 . 下列实验装置或操作正确,且能达到相应实验目的的是
| 选项 | A | B | C | D |
| 实验装置或操作 |  | 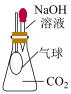 | 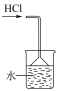 |  |
| 实验目的 | 证明NaHCO3受热易分解 | 证明CO2能与烧碱溶液反应 | 防止倒吸 | 制备O2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 下面甲、乙、丙、丁四个实验,实验现象和结论均正确的是


| A.装置甲中红布条均褪色,说明氯气具有漂白性 |
| B.装置乙中分别滴入酚酞,碳酸钠溶液呈红色,碳酸氢钠溶液呈浅红色,说明碳酸钠的水解程度大于碳酸氢钠 |
| C.装置丙用Cu与浓硫酸反应制取SO2,紫色石蕊、品红、酸性高锰酸钾均褪色,说明SO2具有酸性、漂白性和还原性 |
| D.装置丁中导管红墨水下降,说明铁丝发生吸氧腐蚀 |
您最近一年使用:0次
2023-04-29更新
|
596次组卷
|
2卷引用:安徽省淮南2023届市高三第一次模拟考试理综化学试题
名校
解题方法
9 .  化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究
化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究 与
与 的反应机理,实验步骤如下:
的反应机理,实验步骤如下:

ⅰ.通过注射器注入适量蒸馏水,使 固体全部溶解,并检验是否有
固体全部溶解,并检验是否有 生成;
生成;
ⅱ.向装置A的试管中滴加几滴酚酞试液;
ⅲ.取装置A中剩余溶液于另一试管中,加入少量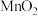 粉末。
粉末。
回答下列问题:
(1)“步骤ⅰ”中检验是否有 生成的实验操作是
生成的实验操作是_______ 。
(2)“步骤ⅱ”得到的实验现象为_______ ,证明 与
与 反应生成碱性物质时,还生成了一种具有漂白性的物质。
反应生成碱性物质时,还生成了一种具有漂白性的物质。
(3)“步骤ⅲ”加入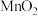 时,有大量气泡产生。
时,有大量气泡产生。
①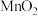 在该反应中的作用为
在该反应中的作用为_______ 。
② 与
与 反应的机理是
反应的机理是_______ 、_______ (用化学方程式表示,分为两步书写)。
(4)向包裹着适量 的脱脂棉(放在陶土网上)上滴加3~4滴水,结果脱脂棉剧烈燃烧。由此可得出与该反应相关的结论是
的脱脂棉(放在陶土网上)上滴加3~4滴水,结果脱脂棉剧烈燃烧。由此可得出与该反应相关的结论是_______ 。
(5)根据 与
与 反应机理推测,干燥的
反应机理推测,干燥的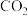 能否与
能否与 反应,并说明原因:
反应,并说明原因:_______ 。
 化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究
化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究 与
与 的反应机理,实验步骤如下:
的反应机理,实验步骤如下:
ⅰ.通过注射器注入适量蒸馏水,使
 固体全部溶解,并检验是否有
固体全部溶解,并检验是否有 生成;
生成;ⅱ.向装置A的试管中滴加几滴酚酞试液;
ⅲ.取装置A中剩余溶液于另一试管中,加入少量
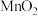 粉末。
粉末。回答下列问题:
(1)“步骤ⅰ”中检验是否有
 生成的实验操作是
生成的实验操作是(2)“步骤ⅱ”得到的实验现象为
 与
与 反应生成碱性物质时,还生成了一种具有漂白性的物质。
反应生成碱性物质时,还生成了一种具有漂白性的物质。(3)“步骤ⅲ”加入
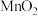 时,有大量气泡产生。
时,有大量气泡产生。①
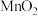 在该反应中的作用为
在该反应中的作用为②
 与
与 反应的机理是
反应的机理是(4)向包裹着适量
 的脱脂棉(放在陶土网上)上滴加3~4滴水,结果脱脂棉剧烈燃烧。由此可得出与该反应相关的结论是
的脱脂棉(放在陶土网上)上滴加3~4滴水,结果脱脂棉剧烈燃烧。由此可得出与该反应相关的结论是(5)根据
 与
与 反应机理推测,干燥的
反应机理推测,干燥的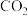 能否与
能否与 反应,并说明原因:
反应,并说明原因:
您最近一年使用:0次
2022-10-27更新
|
83次组卷
|
2卷引用:安徽省淮南市部分学校2022-2023学年高一上学期10月联考化学(B)试题
名校
解题方法
10 . 绿矾是含有一定量结晶水的硫酸亚铁,在工农业生产中具有重要的用途。某化学兴趣小组对绿矾的一些性质进行探究。回答下列问题:
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:____ 。
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。
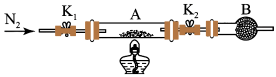
①仪器B的名称是____ 。
②将下列实验操作步骤正确排序____ (填标号);重复上述操作步骤,直至A恒重,记为m3g。
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A
f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=____ (列式表示)。
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。
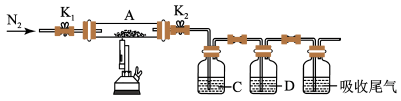
①C、D中的溶液依次为____ (填标号)。C、D有气泡,并可观察到的现象分别为____ 。
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式____ 。
(1)在试管中加入少量绿矾样品,加水溶解,滴加KSCN溶液,溶液颜色无明显变化。再向试管中通入空气,溶液逐渐变红。由此可知:
(2)为测定绿矾中结晶水含量,将石英玻璃管(带两端开关K1和K2)(设为装置A)称重,记为m1g。将样品装入石英玻璃管中,再次将装置A称重,记为m2g。按下图连接好装置进行实验。

①仪器B的名称是
②将下列实验操作步骤正确排序
a.点燃酒精灯,加热
b.熄灭酒精灯
c.关闭K1和K2
d.打开K1和K2,缓缓通入N2 e.称量A
f.冷却到室温
③根据实验记录,计算绿矾化学式中结晶水数目x=
(3)为探究硫酸亚铁的分解产物,将(2)中已恒重的装置A接入下图所示的装置中,打开K1和K2,缓缓通入N2,加热。实验后反应管中残留固体为红色粉末。

①C、D中的溶液依次为
a.品红 b.NaOH c.BaCl2 d.Ba(NO3)2 e.浓H2SO4
②写出硫酸亚铁高温分解反应的化学方程式
您最近一年使用:0次
2019-10-21更新
|
202次组卷
|
4卷引用:安徽省淮南市寿县一中2020 届高三素质测试化学试题



