1 . 某校化学兴趣小组为制备纯净的Cl2并研究Cl2的部分性质,设计了如图所示的实验仪器和药品。其中Ⅰ为干燥的红色试纸,Ⅱ为湿润的红色试纸。

(1)按气流从左到右的方向连接各仪器接口,正确的顺序是a→___________ (填小写字母)。
(2)装置A中盛放MnO2的仪器名称是___________ ,装置A中制备氯气的化学方程式为___________ 。
(3)装置B的作用是___________ 。
(4)若通入足量Cl2,实验过程中装置E中的实验现象___________ 。
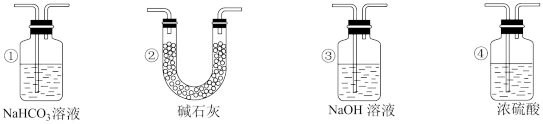
(5)实验结束后,该组同学在装置D中观察到Ⅱ的红色褪去,但是并未观察到“Ⅰ无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置D之前添加图中的___________ 装置(填序号)。
(6)1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图(反应温度为450℃):
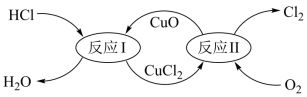
①反应Ⅱ的化学方程式为___________ 。
②该方法制取氯气,主要消耗的原料是___________ ,每生成标准状况下22.4L氯气转移的电子数目是___________ 。

(1)按气流从左到右的方向连接各仪器接口,正确的顺序是a→
(2)装置A中盛放MnO2的仪器名称是
(3)装置B的作用是
(4)若通入足量Cl2,实验过程中装置E中的实验现象
(5)实验结束后,该组同学在装置D中观察到Ⅱ的红色褪去,但是并未观察到“Ⅰ无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在装置D之前添加图中的

(6)1868年狄肯和洪特发明用地康法制氯气,反应原理图示如图(反应温度为450℃):

①反应Ⅱ的化学方程式为
②该方法制取氯气,主要消耗的原料是
您最近一年使用:0次
2024-01-05更新
|
240次组卷
|
4卷引用:河南省许昌高级中学2023-2024学年高一下学期开学化学试题
名校
2 . 利用下列实验装置进行实验,操作正确且能达到实验目的的是
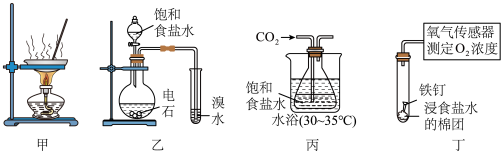
A.用装置甲蒸干 溶液制无水 溶液制无水 晶体 晶体 | B.用装置乙证明乙炔可使溴水褪色 |
C.用装置丙制备 固体 固体 | D.用装置丁验证铁钉吸氧腐蚀 |
您最近一年使用:0次
2024-06-04更新
|
321次组卷
|
4卷引用:2024届河南省许昌部分高中高三下学期模拟考试(三)理科综合试题-高中化学
名校
解题方法
3 . 亚硝酸钙[ ]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。

①已知: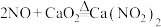 ;
;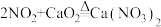 ;
;
②酸性条件下,NO能与 溶液反应生成
溶液反应生成 和
和 。
。
回答下列问题:
(1)检查装置的气密性,装入药品,实验开始前通入一段时间 ,然后关闭弹簧夹,再滴加稀硝酸,通入
,然后关闭弹簧夹,再滴加稀硝酸,通入 的作用是
的作用是___________ 。
(2)为达到实验目的,请把上述装置按气流方向进行连接:______
A→___________→B→___________→___________
(3)E装置的作用是___________ 。
(4)C装置中反应的离子方程式为___________ 。
(5)工业上可用石灰乳和硝酸工业的尾气(含 ,NO)反应,既能净化尾气,又能获得广泛的
,NO)反应,既能净化尾气,又能获得广泛的 ,反应原理为
,反应原理为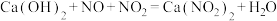 ,若
,若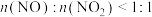 ,则会导致
,则会导致___________ 。
(6)将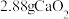 完全转化为
完全转化为 ,理论上需要铜的物质的量至少为
,理论上需要铜的物质的量至少为___________ mol。
 ]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
]是水泥混凝土外加剂的主要原料,可配制成混凝土防冻剂、钢筋阻锈剂等。某学习小组用如图所示实验装置及药品来制备亚硝酸钙(夹持装置略去)。
①已知:
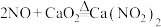 ;
;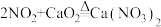 ;
;②酸性条件下,NO能与
 溶液反应生成
溶液反应生成 和
和 。
。回答下列问题:
(1)检查装置的气密性,装入药品,实验开始前通入一段时间
 ,然后关闭弹簧夹,再滴加稀硝酸,通入
,然后关闭弹簧夹,再滴加稀硝酸,通入 的作用是
的作用是(2)为达到实验目的,请把上述装置按气流方向进行连接:
A→___________→B→___________→___________
(3)E装置的作用是
(4)C装置中反应的离子方程式为
(5)工业上可用石灰乳和硝酸工业的尾气(含
 ,NO)反应,既能净化尾气,又能获得广泛的
,NO)反应,既能净化尾气,又能获得广泛的 ,反应原理为
,反应原理为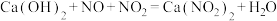 ,若
,若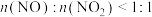 ,则会导致
,则会导致(6)将
 完全转化为
完全转化为 ,理论上需要铜的物质的量至少为
,理论上需要铜的物质的量至少为
您最近一年使用:0次
2024-03-15更新
|
587次组卷
|
3卷引用:河南省许昌高级中学2023-2024学年高一下学期开学化学试题
4 . 实验室制取 时,下列装置能达到相应实验目的的是
时,下列装置能达到相应实验目的的是
 时,下列装置能达到相应实验目的的是
时,下列装置能达到相应实验目的的是A.制备 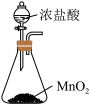 | B.净化 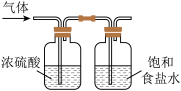 |
C.收集 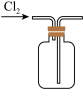 | D.尾气处理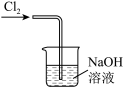 |
您最近一年使用:0次
名校
解题方法
5 . 如图所示的实验装置图正确且能达到相应实验目的的是


| A.图1装置除去Cl2中的HCl |
| B.图2装置实验室制NH3 |
| C.图3装置分离MnO2和KCl |
| D.图4装置蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
您最近一年使用:0次
2019-01-20更新
|
234次组卷
|
3卷引用:河南省长葛市第一高级中学2020-2021学年高一上学期阶段性测试试卷化学试题
6 . 1.Ⅰ.铁是使用最广泛的金属。我国目前发现最早的人工冶铁制品是河南三门峡出土的西周晚期的玉柄铁剑。
(1)在铁器制造中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理。用化学方程式解释其原因为__________________ 。
1.(2)检验 溶液蚀覆铜板后混合溶液中是否存在
溶液蚀覆铜板后混合溶液中是否存在 ,最好选择下列试剂中的
,最好选择下列试剂中的________ (填编号,下同)进行检验,现象和结论是__________________ 。
A. KSCN溶液 B. 酸性 溶液 C. 新制氯水 D. NaOH溶液
溶液 C. 新制氯水 D. NaOH溶液
(2)高铁酸钠( )是一种新型净水剂,遇酸会发生分解反应。其一种制备原理如下:
)是一种新型净水剂,遇酸会发生分解反应。其一种制备原理如下:
______ ______
______ ______=______
______=______ ______
______ ______
______
补充完整并配平后的离子方程式为__________________ 。
Ⅱ.氯是一种重要的成盐元素,氯的单质氯气是一种重要的化工原料。实验室利用下图所示装置制取并收集氯气。回答有关问题。
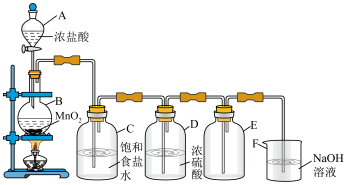
(3)装置A的名称是______ 。装置C的作用是__________________ 。
(4)该实验中收集氯气的方法叫做______ 。氯气还可以用排______ 溶液的方法收集。
(5)制备时装置B中发生反应的化学方程式为____________ ,F装置中发生反应的离子方程式为____________ 。
(1)在铁器制造中,炽热的铁水注入模具之前,必须对模具进行充分的干燥处理。用化学方程式解释其原因为
1.(2)检验
 溶液蚀覆铜板后混合溶液中是否存在
溶液蚀覆铜板后混合溶液中是否存在 ,最好选择下列试剂中的
,最好选择下列试剂中的A. KSCN溶液 B. 酸性
 溶液 C. 新制氯水 D. NaOH溶液
溶液 C. 新制氯水 D. NaOH溶液(2)高铁酸钠(
 )是一种新型净水剂,遇酸会发生分解反应。其一种制备原理如下:
)是一种新型净水剂,遇酸会发生分解反应。其一种制备原理如下:______
 ______
______ ______=______
______=______ ______
______ ______
______
补充完整并配平后的离子方程式为
Ⅱ.氯是一种重要的成盐元素,氯的单质氯气是一种重要的化工原料。实验室利用下图所示装置制取并收集氯气。回答有关问题。

(3)装置A的名称是
(4)该实验中收集氯气的方法叫做
(5)制备时装置B中发生反应的化学方程式为
您最近一年使用:0次
名校
解题方法
7 . 金属Ti是制备飞机发动机叶片的重要材料,其一种制备方法是利用氯气与TiO2反应制备TiCl4,然后使用Mg还原法制备金属Ti,某化学小组在实验室中制备TiCl4并测定其纯度。回答下列问题:
Ⅰ.TiCl4的制备。
已知:TiCl4的沸点为136.4℃,易水解,高温时易与氧气发生反应。_______ (用小写字母表示,装置根据需要可重复使用)。
(2)装置A中盛放的固体药品名称为_______ ,装置D中试剂的作用为_______ 。
(3)若装置F中碳粉被完全氧化为CO2气体,则反应的化学方程式为_______ 。
Ⅱ.TiCl4的纯度测定。
实验步骤:①取5.20 g TiCl4粗品溶于浓盐酸中,过滤,将滤液稀释至250 mL,取25.00 mL溶液于锥形瓶中;②向其中加入稍过量金属铝丝将TiCl4全部还原为TiCl3(具有较强还原性,在空气中易被氧化),静置一段时间,向其中加入适量碳酸氢钠溶液待不再产生气泡,塞上橡胶塞密封冷却至室温;③向锥形瓶中滴加2滴KSCN溶液,用
0.100 0 mol/L(NH4)Fe(SO4)2标准溶液滴定至终点,平行进行三次实验,测得平均消耗标准溶液25.00 mL。
(4)步骤②中加入适量碳酸氢钠溶液的目的为_______ 。
(5)达到滴定终点的现象为_______ 。
(6)TiCl4粗品的纯度为_______ (保留三位有效数字),若滴定前正确读数,滴定终点俯视读数,则测定结果将_______ (填“偏大”“偏小”或“无影响”)。
Ⅰ.TiCl4的制备。
已知:TiCl4的沸点为136.4℃,易水解,高温时易与氧气发生反应。

(2)装置A中盛放的固体药品名称为
(3)若装置F中碳粉被完全氧化为CO2气体,则反应的化学方程式为
Ⅱ.TiCl4的纯度测定。
实验步骤:①取5.20 g TiCl4粗品溶于浓盐酸中,过滤,将滤液稀释至250 mL,取25.00 mL溶液于锥形瓶中;②向其中加入稍过量金属铝丝将TiCl4全部还原为TiCl3(具有较强还原性,在空气中易被氧化),静置一段时间,向其中加入适量碳酸氢钠溶液待不再产生气泡,塞上橡胶塞密封冷却至室温;③向锥形瓶中滴加2滴KSCN溶液,用
0.100 0 mol/L(NH4)Fe(SO4)2标准溶液滴定至终点,平行进行三次实验,测得平均消耗标准溶液25.00 mL。
(4)步骤②中加入适量碳酸氢钠溶液的目的为
(5)达到滴定终点的现象为
(6)TiCl4粗品的纯度为
您最近一年使用:0次
2024-03-09更新
|
122次组卷
|
3卷引用:河南省许昌市禹州市高级中学2023-2024学年高三下学期4月月考理综试题-高中化学
8 . FTO导电玻璃为掺杂氟的SnO2透明导电玻璃,广泛用于液晶显示屏、薄膜太阳能电池基底等方面,SnCl4可用于制作FTO导电玻璃。实验室可用熔融的锡与Cl2反应制备SnCl4,此反应放热,生成的SnCl4易水解生成SnO2·xH2O。回答下列问题:

有关物理性质如下表:
(1)II装置中发生反应的离子方程式为_______ 。
(2)将上述装置用玻璃管连接,组装成一套制备SnCl4的实验装置(每个装置最多使用一次),正确的顺序是(填各接口字母序号):B_______ N,A_______ 。
(3)检查装置气密性并装好药品后,应先打开II中的分液漏斗活塞,待出现______ 现象后,再点燃I处的酒精灯。
(4)VI 装置的作用是_______ 。若没有VI装置,可能发生的化学反应方程式为_______ 。
(5)实验制得30g溶有氯气的SnCl4,其中氯气质量分数为13.0%,则需向I中通入氯气的物质的量为_______ mol(保留2位小数)。提纯该SnCl4的方法是_______ 。
a.用NaOH溶液洗涤再蒸馏 b.升华 c.重结晶 d.蒸馏 e.过滤

有关物理性质如下表:
| 物质 | 颜色、状态 | 熔点/℃ | 沸点/℃ |
| Sn | 银白色固体 | 231.9 | 2 260 |
| SnCl4 | 无色液体 | -33 | 114 |
| SnCl2 | 无色晶体 | 246 | 652 |
(2)将上述装置用玻璃管连接,组装成一套制备SnCl4的实验装置(每个装置最多使用一次),正确的顺序是(填各接口字母序号):B
(3)检查装置气密性并装好药品后,应先打开II中的分液漏斗活塞,待出现
(4)VI 装置的作用是
(5)实验制得30g溶有氯气的SnCl4,其中氯气质量分数为13.0%,则需向I中通入氯气的物质的量为
a.用NaOH溶液洗涤再蒸馏 b.升华 c.重结晶 d.蒸馏 e.过滤
您最近一年使用:0次
名校
解题方法
9 .  在常温下化学性质非常稳定,但在加热条件下可以体现氧化性或还原性。
在常温下化学性质非常稳定,但在加热条件下可以体现氧化性或还原性。
I.某实验小组计划使用 与浓盐酸制备并收集少量
与浓盐酸制备并收集少量 ,实验装置如下所示:
,实验装置如下所示:

(1)仪器m的名称为__________ ,A装置中发生的反应中氧化剂和还原剂之比为__________ 。
(2)装置B的作用为__________ ,装置F的作用为__________ 。
(3)在实验进行过程中,小组成员观察到装置E中的现象:___________ 。
II.实验室中可以利用 碱熔法来制备
碱熔法来制备 晶体,其步骤如下所示:
晶体,其步骤如下所示:
(4)高温条件下坩埚中发生反应的化学方程式为__________ ;为了加快水浸时固体的溶解速率,可以采取的措施有__________ (写一条)。
(5)操作X中空缺的内容为__________ ;使用恒温烘箱对所得的 晶体进行干燥时,仪器内部温度一般不宜超过120℃,这是由于
晶体进行干燥时,仪器内部温度一般不宜超过120℃,这是由于__________ 。
 在常温下化学性质非常稳定,但在加热条件下可以体现氧化性或还原性。
在常温下化学性质非常稳定,但在加热条件下可以体现氧化性或还原性。I.某实验小组计划使用
 与浓盐酸制备并收集少量
与浓盐酸制备并收集少量 ,实验装置如下所示:
,实验装置如下所示:
(1)仪器m的名称为
(2)装置B的作用为
(3)在实验进行过程中,小组成员观察到装置E中的现象:
II.实验室中可以利用
 碱熔法来制备
碱熔法来制备 晶体,其步骤如下所示:
晶体,其步骤如下所示:     溶液 溶液  晶体 晶体①碱熔:在铁制坩埚中将一定量的  与 与 的混合物用酒精喷灯加热至熔化后,向其中逐步加入 的混合物用酒精喷灯加热至熔化后,向其中逐步加入 粉末并用铁棒搅拌,待加热至5分钟时关闭酒精喷灯,冷却到室温后可见坩埚中存在墨绿色的块状固体,其中主要成分为 粉末并用铁棒搅拌,待加热至5分钟时关闭酒精喷灯,冷却到室温后可见坩埚中存在墨绿色的块状固体,其中主要成分为 与 与 。 。②水浸:将坩埚中的块状固体转移至烧杯中,加足量水溶解。 ③歧化:向所得的  溶液中通入适量的 溶液中通入适量的 ,促使 ,促使 歧化为 歧化为 与 与 。 。④过滤:除去溶液中的不溶性物质。 ⑤操作X:加热浓缩、冷却结晶、过滤、_______、干燥。 |
(5)操作X中空缺的内容为
 晶体进行干燥时,仪器内部温度一般不宜超过120℃,这是由于
晶体进行干燥时,仪器内部温度一般不宜超过120℃,这是由于
您最近一年使用:0次
解题方法
10 . 某实验小组用浓盐酸和 制取
制取 并探究其化学性质,设计装置如图:
并探究其化学性质,设计装置如图:
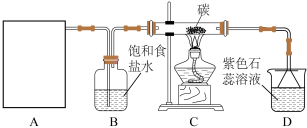
(1)制备 的化学反应离子方程式是
的化学反应离子方程式是_______ ,A是氯气发生装置(省略未画),A装置除了酒精灯、圆底烧瓶外还用到的玻璃仪器有_______
(2)从C装置出来的气体中含有 和HCl,则在C装置中发生的化学反应方程式为
和HCl,则在C装置中发生的化学反应方程式为_______ 。
(3)若装置D中用足量的 溶液吸收多余氯气,试写出相应的离子方程式:
溶液吸收多余氯气,试写出相应的离子方程式:_______ 。
(4)同学们在实验中发现,若用稀盐酸代替浓盐酸与 混合加热没有氯气生成,于是开始探究该条件下不能生成氯气的原因。
混合加热没有氯气生成,于是开始探究该条件下不能生成氯气的原因。
①提出合理假设。
假设1: 的浓度不够大;
的浓度不够大;
假设2:_______ ;
假设3:_______ 。
②设计实验方案,进行实验。在下表中写出实验步骤以及预期现象和结论。_______
限选实验试剂:蒸馏水、浓 固体、
固体、 固体、稀盐酸、
固体、稀盐酸、 溶液、淀粉-KI溶液。
溶液、淀粉-KI溶液。
 制取
制取 并探究其化学性质,设计装置如图:
并探究其化学性质,设计装置如图:
(1)制备
 的化学反应离子方程式是
的化学反应离子方程式是(2)从C装置出来的气体中含有
 和HCl,则在C装置中发生的化学反应方程式为
和HCl,则在C装置中发生的化学反应方程式为(3)若装置D中用足量的
 溶液吸收多余氯气,试写出相应的离子方程式:
溶液吸收多余氯气,试写出相应的离子方程式:(4)同学们在实验中发现,若用稀盐酸代替浓盐酸与
 混合加热没有氯气生成,于是开始探究该条件下不能生成氯气的原因。
混合加热没有氯气生成,于是开始探究该条件下不能生成氯气的原因。①提出合理假设。
假设1:
 的浓度不够大;
的浓度不够大;假设2:
假设3:
②设计实验方案,进行实验。在下表中写出实验步骤以及预期现象和结论。
限选实验试剂:蒸馏水、浓
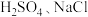 固体、
固体、 固体、稀盐酸、
固体、稀盐酸、 溶液、淀粉-KI溶液。
溶液、淀粉-KI溶液。| 实验步骤 | 预期现象与结论 |
步骤1:取少量1mol/L稀盐酸于试管A中,加入少量 ,_______ ,_______ | _______ |
步骤2:取少量1mol/L稀盐酸于试管B中,加入少量 ,_______ ,_______ | _______ |
您最近一年使用:0次



