名校
1 . 设NA表示阿伏加德罗常数的值。下列说法不正确的是
| A.0.1NASO2与足量氧气反应生成SO3的质量为8克 |
| B.标准状况下,11.2LCH4含共用电子对数为2NA |
| C.100mL0.1mol·L−1的NaHCO3溶液中含有H原子数为0.01NA |
| D.常温常压下,22g由N2O与CO2组成的混合气体含有的原子数目为1.5NA |
您最近一年使用:0次
名校
解题方法
2 . 双极膜(BP)可以在电场作用下,使水分子快速解离为OH⁻和H+,并透过阴、阳离子膜进入溶液。用此工艺捕获烟道气中的CO2过程如图所示,已知盐室中生成CaCO3实现捕获,下列说法正确的是
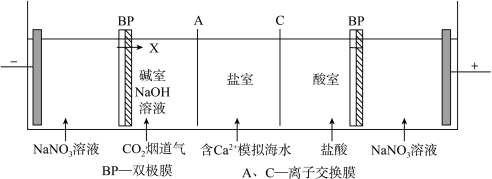

A.捕获装置中,阴极反应为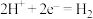 |
| B.溶液中的X为H+ |
| C.交换膜A为阴离子交换膜 |
| D.捕获1.12LCO2转化为沉淀,则转移电子2mol |
您最近一年使用:0次
名校
3 . 铁、铜混合粉末18.0g加入100mL5.0mol·L-1FeCl3溶液中,剩余固体质量为3.2g。下列说法正确的是
| A.剩余固体是铁、铜混合物 | B.反应后溶液中n(Fe2+)+n(Cu2+)=0.75mol |
| C.原固体混合物中铜的质量是9.6g | D.反应后溶液中n(Fe3+)=0.10mol |
您最近一年使用:0次
名校
解题方法
4 . 设 NA 表示阿伏加德罗常数的值,下列说法正确的是
| A.3.2g O2 与 O3 的混合物中含有氧原子个数为0.2NA |
B.1mol  所含质子数为 10NA 所含质子数为 10NA |
| C.常温常压下,11.2L CH4 含有的氢原子数小于 2NA |
| D.5.6g 金属铁与足量稀硫酸反应转移的电子数为 0.3NA |
您最近一年使用:0次
名校
解题方法
5 . 一定温度和压强下,用质量相等的CH4、CO2、O2、SO2四种气体分别吹出四个体积大小不同的气球,下列说法中不正确的是
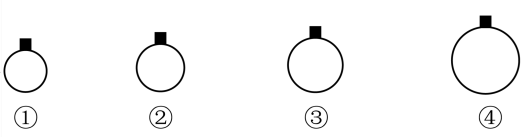

| A.气球②中装的是CO2 |
| B.气球①和气球③中气体分子数相等 |
| C.气球①和气球②中原子数之比为16:11 |
| D.气球③和气球④中气体体积之比为1:2 |
您最近一年使用:0次
2023-09-09更新
|
545次组卷
|
2卷引用:山东省枣庄市第三中学2022-2023学年高一上学期10月月考化学试题
名校
解题方法
6 . 下列说法中,正确的是
| A.在标准状况下,2.24 L Cl2与过量NaOH溶液反应,转移的电子数约为0.2×6.02×1023 |
| B.1 mol Cl2与足量Fe反应,转移的电子数约为2×6.02×1023 |
| C.常温常压下的33.6 L Cl2与27 g Al充分反应,转移电子数约为3×6.02×1023 |
| D.在反应H2O2+Cl2=2HCl+O2中,每生成32 g O2,转移约2×6.02×1023个电子 |
您最近一年使用:0次
7 . 我国科研团队在人工合成淀粉方面取得突破性进展,通过CO2、H2制得CH3OH,进而合成了淀粉[(C6H10O5)n]。用NA表示阿伏加德罗常数的值,下列说法正确的是
A.标准状况下, 中含有电子数为 中含有电子数为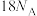 |
B.16.2g淀粉 中含C原子数为 中含C原子数为 |
C.常温常压下,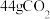 中含有 中含有 的C=O键 的C=O键 |
D.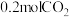 和 和 混合气体的分子数为 混合气体的分子数为 |
您最近一年使用:0次
名校
8 . NA 为阿伏加德罗常数的值。下列叙述正确的是
| A.0.1 mol/L Na2CO3 溶液中,含有的 Na+数目为 0.2 NA |
| B.标准状况下,22.4 L CH4 和 22.4 L Cl2 在光照下充分反应后的分子数为 2NA |
| C.1 mol Na2O2 晶体和 1 mol CaH2 晶体含有的离子数目均为 2NA |
| D.一定条件下,5.6 g Fe 与 0.1 mol Cl2 充分反应,转移的电子数为 0.2NA |
您最近一年使用:0次
名校
解题方法
9 . 将agNH3溶于水得到VmL溶液,假设该溶液的密度为ρg/cm3,质量分数为w,溶液中NH 为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
 为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是
为bmol。已知氨水的密度比水小且浓度越大密度越小。下列叙述正确的是A.据电荷守恒知:溶液中c(OH-)=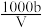 +c(H+) +c(H+) |
B.溶质的质量分数为w= ×100% ×100% |
C.溶质的物质的量浓度c=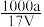 mol/L mol/L |
| D.上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w |
您最近一年使用:0次
解题方法
10 . 一个密闭容器,中间有一可自由滑动的隔板(厚度不计),将容器分成两部分,当左侧充入1molN2,右侧充入一定量的CO时,隔板处于如图位置(保持温度不变),下列说法不正确的是


| A.左侧与右侧原子数之比为4∶1 |
| B.右侧CO的质量为5.6g |
| C.右侧气体密度是相同条件下氢气密度的28倍 |
| D.保持温度不变,若改变右侧CO的充入量而使隔板处于容器正中间,则应再充入0.75molCO |
您最近一年使用:0次



