解题方法
1 . 苯乙酮(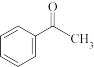 )是一种重要的化工原料,可用于制造香皂和塑料的增塑剂。其实验室制备流程和有关数据如下所示:
)是一种重要的化工原料,可用于制造香皂和塑料的增塑剂。其实验室制备流程和有关数据如下所示:
| 名称 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度g/mL | 溶解度 |
| 乙酸酐 | 102 | -73 | 140 | 1.082 | 微溶于水,易水解 |
| 苯 | 78 | 5.5 | 80.5 | 0.879 | 不溶水 |
| 苯乙酮 | 120 | 20.5 | 202 | 1.028 | 微溶水 |
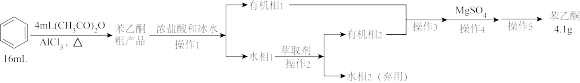
(1)制备苯乙酮粗产品的装置如图所示(加热和夹持装置已略去)。

②无水
 固体的作用是
固体的作用是(2)从绿色化学角度考虑,操作2中萃取剂宜采用_______。
| A.乙醇 | B.乙酸乙酯 | C.苯 | D.乙醚 |
(4)操作4中加入无水
 的目的是
的目的是(5)将操作5(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和沸石,
(6)本实验苯乙酮的产率最接近于_______。
| A.80% | B.70% | C.60% | D.50% |
您最近一年使用:0次
名校
解题方法
2 . KMnO4广泛用作氧化剂,可以氧化HCl、FeSO4等。某兴趣小组用Cl2氧化K2MnO4制备KMnO4的装置如下图所示。
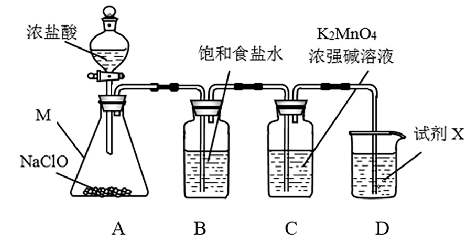
(1)仪器M的名称是_______ 。
(2)装置B的作用是_______ 。
(3)为提高Cl2在装置C中的利用率,在装置A的操作中可采取的措施是_______ 。
(4)试剂X常用浓NaOH溶液,而不用澄清石灰水的主要原因是_______ 。
(5)利用KMnO4测定CuI样品中CuI质量分数(杂质不参与反应)的方法如下:
步骤一:称取CuI样品0.500g,向其中加入足量Fe2(SO4)3溶液,发生反应4Fe3++2CuI=4Fe2++2Cu2++I2。
步骤二:待充分反应后,滴加5.000×10−2mol·L−1KMnO4溶液,发生反应 +5Fe2++8H+=Mn2++5Fe3++4H2O,至恰好完全反应消耗KMnO4溶液20.00mL。
+5Fe2++8H+=Mn2++5Fe3++4H2O,至恰好完全反应消耗KMnO4溶液20.00mL。
计算该样品中碘化亚铜的质量分数(写出计算过程)。_______

(1)仪器M的名称是
(2)装置B的作用是
(3)为提高Cl2在装置C中的利用率,在装置A的操作中可采取的措施是
(4)试剂X常用浓NaOH溶液,而不用澄清石灰水的主要原因是
(5)利用KMnO4测定CuI样品中CuI质量分数(杂质不参与反应)的方法如下:
步骤一:称取CuI样品0.500g,向其中加入足量Fe2(SO4)3溶液,发生反应4Fe3++2CuI=4Fe2++2Cu2++I2。
步骤二:待充分反应后,滴加5.000×10−2mol·L−1KMnO4溶液,发生反应
 +5Fe2++8H+=Mn2++5Fe3++4H2O,至恰好完全反应消耗KMnO4溶液20.00mL。
+5Fe2++8H+=Mn2++5Fe3++4H2O,至恰好完全反应消耗KMnO4溶液20.00mL。计算该样品中碘化亚铜的质量分数(写出计算过程)。
您最近一年使用:0次
2021-01-05更新
|
228次组卷
|
4卷引用:2020年山东卷化学高考真题变式题16-20
(已下线)2020年山东卷化学高考真题变式题16-20江苏省扬州市2021年普通高中学业水平检测模拟化学试题江苏省盐城市伍佑中学2022-2023学年高二上学期期中考试化学(必修)试题江苏省宿迁市沭阳县潼阳中学2021-2022学年高二上学期期中考试化学试题
3 . 实验室制备氧气也常用加热分解 制得,发生反应:
制得,发生反应: ;取8.5g硝酸钠固体置于装置,加热一段时间,收集到VmL氧气后,停止加热,待固体冷却后称得剩余7.22g,将剩余固体溶于水配制成100mL稀溶液,加入足量铜片,并滴入稀硫酸,使其充分反应(气体只有NO)(已知:
;取8.5g硝酸钠固体置于装置,加热一段时间,收集到VmL氧气后,停止加热,待固体冷却后称得剩余7.22g,将剩余固体溶于水配制成100mL稀溶液,加入足量铜片,并滴入稀硫酸,使其充分反应(气体只有NO)(已知: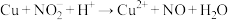 ,未配平),求:
,未配平),求:
(1)V=___________ ;
(2)溶解铜的质量是:___________ g(写出简单计算过程 )
 制得,发生反应:
制得,发生反应: ;取8.5g硝酸钠固体置于装置,加热一段时间,收集到VmL氧气后,停止加热,待固体冷却后称得剩余7.22g,将剩余固体溶于水配制成100mL稀溶液,加入足量铜片,并滴入稀硫酸,使其充分反应(气体只有NO)(已知:
;取8.5g硝酸钠固体置于装置,加热一段时间,收集到VmL氧气后,停止加热,待固体冷却后称得剩余7.22g,将剩余固体溶于水配制成100mL稀溶液,加入足量铜片,并滴入稀硫酸,使其充分反应(气体只有NO)(已知: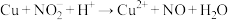 ,未配平),求:
,未配平),求:(1)V=
(2)溶解铜的质量是:
您最近一年使用:0次
4 . 氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素 的碱性溶液制氢气的装置示意图
的碱性溶液制氢气的装置示意图 电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极
电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极 。
。
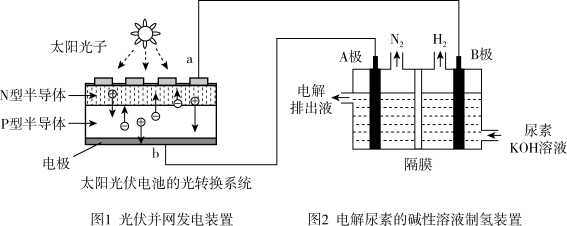
(1)图1中N型半导体为______  填“正极”或“负极”
填“正极”或“负极”
(2)该系统工作时,A极的电极反应式为______
(3)若A极产生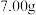
 ,则此时B极产生
,则此时B极产生______ L  标况下
标况下 。
。
 的碱性溶液制氢气的装置示意图
的碱性溶液制氢气的装置示意图 电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极
电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极 。
。
(1)图1中N型半导体为
 填“正极”或“负极”
填“正极”或“负极”
(2)该系统工作时,A极的电极反应式为
(3)若A极产生
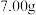
 ,则此时B极产生
,则此时B极产生 标况下
标况下 。
。
您最近一年使用:0次
5 . 化学工业为疫情防控提供了强有力的物质支撑。氯的许多化合物既是重要化工原料,又是高效、广谱的灭菌消毒剂。回答下列问题:
(1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许______ 离子通过,氯气的逸出口是_______ (填标号)。

(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ[δ(X)= ,X为HClO或ClO−]与pH的关系如图(b)所示。HClO的电离常数Ka值为
,X为HClO或ClO−]与pH的关系如图(b)所示。HClO的电离常数Ka值为______ 。
(3)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为______ 。
(4)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为_____ mol;产生“气泡”的化学方程式为____________ 。
(5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是______ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000 kg该溶液需消耗氯气的质量为____ kg(保留整数)。
(1)氯气是制备系列含氯化合物的主要原料,可采用如图(a)所示的装置来制取。装置中的离子膜只允许

(2)次氯酸为一元弱酸,具有漂白和杀菌作用,其电离平衡体系中各成分的组成分数δ[δ(X)=
 ,X为HClO或ClO−]与pH的关系如图(b)所示。HClO的电离常数Ka值为
,X为HClO或ClO−]与pH的关系如图(b)所示。HClO的电离常数Ka值为(3)Cl2O为淡棕黄色气体,是次氯酸的酸酐,可由新制的HgO和Cl2反应来制备,该反应为歧化反应(氧化剂和还原剂为同一种物质的反应)。上述制备Cl2O的化学方程式为
(4)ClO2常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。一种有效成分为NaClO2、NaHSO4、NaHCO3的“二氧化氯泡腾片”,能快速溶于水,溢出大量气泡,得到ClO2溶液。上述过程中,生成ClO2的反应属于歧化反应,每生成1 mol ClO2消耗NaClO2的量为
(5)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
2020-07-08更新
|
12835次组卷
|
13卷引用:专题13 元素及其化合物知识的综合应用-2020年高考真题和模拟题化学分项汇编
(已下线)专题13 元素及其化合物知识的综合应用-2020年高考真题和模拟题化学分项汇编(已下线)专题08 常见无机物及其应用——备战2021年高考化学纠错笔记(已下线)押全国卷理综第27题 工业流程-备战2021年高考化学临考题号押题(课标全国卷)(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押全国卷理综第27题 工业流程-备战2022年高考化学临考题号押题(全国卷)(已下线)题型43 次氯酸、氯的含氧酸盐的性质和应用(已下线)专题17 原理综合题2020年全国统一考试化学试题(新课标Ⅱ)四川省成都市双流棠湖中学2021届高三上学期开学考试理综化学试题青海省湟川中学2020-2021学年高二下学期第一次月考化学试题山东省枣庄市第三中学2022届高三第一次月考化学试题2020年全国卷Ⅱ化学真题变式题(已下线)第05练 以简单工业流程突破金属及其化合物-2022年【暑假分层作业】高二化学(2023届一轮复习通用)



