名校
解题方法
1 . 碘酸钙为白色固体,微溶于水,是一种无机精细与专用化学品。一种制备并测定六水合碘酸钙含量的实验设计如下。
步骤Ⅰ:碘酸氢钾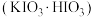 的制备
的制备
在三颈烧瓶中加入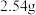 碘、
碘、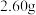 氯酸钾和
氯酸钾和 水,滴加
水,滴加 的盐酸至
的盐酸至 ,控制温度
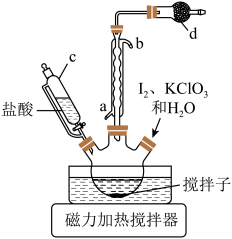
,控制温度 左右,装置如图。
左右,装置如图。
步骤Ⅱ:碘酸钙晶体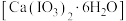 的制备
的制备
将步骤Ⅰ反应后的溶液转入烧杯中,加入 溶液调节
溶液调节 ;继续滴加
;继续滴加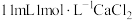 溶液,充分反应后用冰水冷却,抽滤、用少量冰水洗涤、再用少量无水乙醇洗涤,干燥,得粗产品碘酸钙晶体
溶液,充分反应后用冰水冷却,抽滤、用少量冰水洗涤、再用少量无水乙醇洗涤,干燥,得粗产品碘酸钙晶体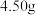 。
。
步骤Ⅲ:产品中碘酸钙晶体含量测定
①准确称取 粗产品,置于烧杯中,加入
粗产品,置于烧杯中,加入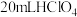 溶解样品,转移到
溶解样品,转移到 容量瓶中定容。量取
容量瓶中定容。量取 溶液于碘量瓶中,加入稍过量的
溶液于碘量瓶中,加入稍过量的 ,然后用
,然后用 标准溶液滴定至浅黄色,加入2滴淀粉溶液,继续滴定至终点,平行测定三次后取平均值,用去
标准溶液滴定至浅黄色,加入2滴淀粉溶液,继续滴定至终点,平行测定三次后取平均值,用去 标准溶液。
标准溶液。
②空白实验:不取产品,其余试剂用量和步骤相同,消耗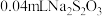 标准溶液。
标准溶液。
已知: ,
, ,
,
请回答下列问题:
(1)仪器 的名称为
的名称为___________ ,步骤Ⅰ中有黄绿色气体产生,则制备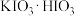 反应的化学方程式为
反应的化学方程式为___________ , 的作用是
的作用是___________ 。
(2)步骤Ⅰ中温度不宜过高的原因是___________ ,判断反应结束的实验现象是___________ 。
(3)步骤Ⅱ中用少量无水乙醇洗涤的目的是___________ 。
(4)步骤Ⅲ中空白实验的主要目的是___________ 。
(5)下列关于滴定分析的操作,不正确的是___________ 。
A.用量筒量取 待测液转移至碘量瓶中
待测液转移至碘量瓶中
B.滴定过程中用少量蒸馏水将锥形并瓦内壁附着的溶液冲下
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.平行滴定时,须重新装液并调节液面至“0”刻度或“零刻度以下
(6)碘酸钙晶体中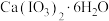 (相对分子质量为498)的纯度为
(相对分子质量为498)的纯度为___________ (计算结果保留两位小数)。
步骤Ⅰ:碘酸氢钾
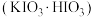 的制备
的制备在三颈烧瓶中加入
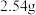 碘、
碘、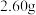 氯酸钾和
氯酸钾和 水,滴加
水,滴加 的盐酸至
的盐酸至 ,控制温度
,控制温度 左右,装置如图。
左右,装置如图。
步骤Ⅱ:碘酸钙晶体
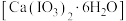 的制备
的制备将步骤Ⅰ反应后的溶液转入烧杯中,加入
 溶液调节
溶液调节 ;继续滴加
;继续滴加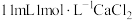 溶液,充分反应后用冰水冷却,抽滤、用少量冰水洗涤、再用少量无水乙醇洗涤,干燥,得粗产品碘酸钙晶体
溶液,充分反应后用冰水冷却,抽滤、用少量冰水洗涤、再用少量无水乙醇洗涤,干燥,得粗产品碘酸钙晶体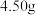 。
。步骤Ⅲ:产品中碘酸钙晶体含量测定
①准确称取
 粗产品,置于烧杯中,加入
粗产品,置于烧杯中,加入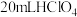 溶解样品,转移到
溶解样品,转移到 容量瓶中定容。量取
容量瓶中定容。量取 溶液于碘量瓶中,加入稍过量的
溶液于碘量瓶中,加入稍过量的 ,然后用
,然后用 标准溶液滴定至浅黄色,加入2滴淀粉溶液,继续滴定至终点,平行测定三次后取平均值,用去
标准溶液滴定至浅黄色,加入2滴淀粉溶液,继续滴定至终点,平行测定三次后取平均值,用去 标准溶液。
标准溶液。②空白实验:不取产品,其余试剂用量和步骤相同,消耗
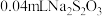 标准溶液。
标准溶液。已知:
 ,
, ,
,
请回答下列问题:
(1)仪器
 的名称为
的名称为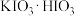 反应的化学方程式为
反应的化学方程式为 的作用是
的作用是(2)步骤Ⅰ中温度不宜过高的原因是
(3)步骤Ⅱ中用少量无水乙醇洗涤的目的是
(4)步骤Ⅲ中空白实验的主要目的是
(5)下列关于滴定分析的操作,不正确的是
A.用量筒量取
 待测液转移至碘量瓶中
待测液转移至碘量瓶中B.滴定过程中用少量蒸馏水将锥形并瓦内壁附着的溶液冲下
C.滴定时应一直观察滴定管中溶液体积的变化
D.读数时应将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
E.平行滴定时,须重新装液并调节液面至“0”刻度或“零刻度以下
(6)碘酸钙晶体中
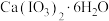 (相对分子质量为498)的纯度为
(相对分子质量为498)的纯度为
您最近一年使用:0次
名校
解题方法
2 . 甘氨酸亚铁[(H2NCH2COO)2Fe]是新一代畜禽饲料补铁添加剂。某实验小组以碳酸亚铁和甘氨酸反应制备甘氨酸亚铁的装置如下(夹持和加热仪器略去):
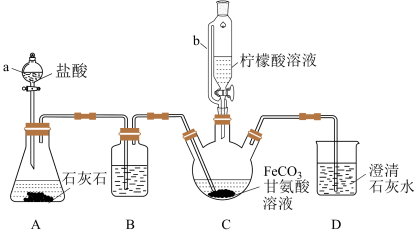
已知:①反应原理为2H2NCH2COOH+FeCO3 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。
②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为_______ 。
(2)装置A制备CO2的用途是_______ 。
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为_______ 。
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是_______ 。
②柠檬酸溶液除了起酸性作用外,还有的作用是_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是_______ %。

已知:①反应原理为2H2NCH2COOH+FeCO3
 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为
(2)装置A制备CO2的用途是
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是
②柠檬酸溶液除了起酸性作用外,还有的作用是
(5)过程II中加入无水乙醇的目的是
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是
您最近一年使用:0次
名校
解题方法
3 . 乙酰苯胺俗称退热冰,是常用的化工原料和重要的化学试剂。某实验小组拟用一定量的乙酸和苯胺制备一定量的乙酰苯胺,具体实验步骤如下:
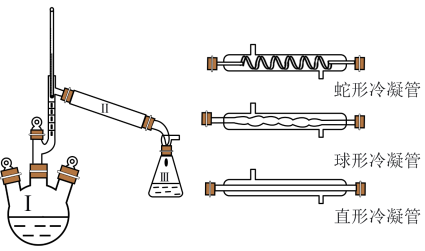
步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
回答下列问题
(1)Ⅱ处空白位置应选择的仪器为___________ (填“蛇形冷凝管”“球形冷凝管”或“直形冷凝管”);反应开始后发现忘加沸石,正确的操作为___________ 。
(2)步骤1中,发生反应的化学方程式是___________ ;温度计控温在105℃的原因是___________ 。
(3)步骤2中,用冷水进行洗涤的原因是___________ 。
(4)步骤3中,趁热抽滤的目的是___________ 。
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为___________ (结果保留2位有效数字)。

步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g/mL) | 溶解性 | |
| 乙酸 | 60 | 16.6 | 117.9 | 1.05 | 能溶于水、乙醇、乙醚 |
| 苯胺 | 93 | -6 | 184 | 1.022 | 微溶于水,易溶于乙醇、乙醚 |
| 乙酰苯胺 | 135 | 114 | 304 | 1.12 | 微溶于冷水,能溶于热水 |
(1)Ⅱ处空白位置应选择的仪器为
(2)步骤1中,发生反应的化学方程式是
(3)步骤2中,用冷水进行洗涤的原因是
(4)步骤3中,趁热抽滤的目的是
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
4 . 氮化硼(BN)是白色难溶于水的粉末状固体,高温下易被氧化。实验室以硼粉(黑色)为原料,用下图装置模拟制备氮化硼。
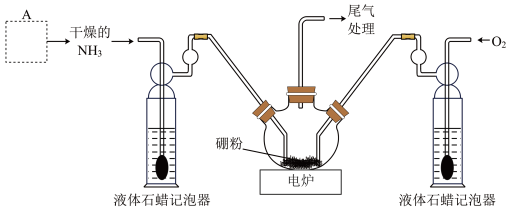
(1)写出制备BN的化学方程式___________ 。
(2)下列装置可填入A框中的是___________ (填标号)。
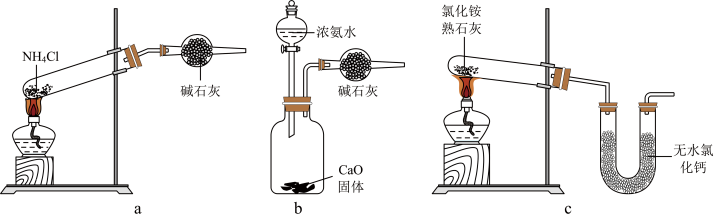
(3)下列装置可用做尾气处理的是___________ (填标号)。
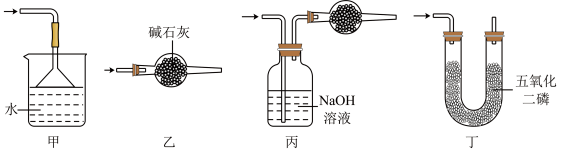
(4)实验所得的氮化硼样品可用“铵盐蒸馏法”测定纯度,具体步骤如下:
①称取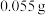 氮化硼样品,加入浓硫酸和催化剂,微热,令样品中N元素全部转为铵盐;
氮化硼样品,加入浓硫酸和催化剂,微热,令样品中N元素全部转为铵盐;
②向铵盐中加入足量 溶液并加热,蒸出的氨全部被
溶液并加热,蒸出的氨全部被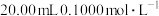 的稀硫酸溶液完全吸收;
的稀硫酸溶液完全吸收;
③向稀硫酸中加入指示剂,用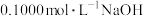 溶液滴定剩余硫酸,消耗
溶液滴定剩余硫酸,消耗 溶液平均体积为
溶液平均体积为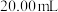 。
。
氮化硼样品的纯度为___________ %(保留1位小数)。

(1)写出制备BN的化学方程式
(2)下列装置可填入A框中的是

(3)下列装置可用做尾气处理的是

(4)实验所得的氮化硼样品可用“铵盐蒸馏法”测定纯度,具体步骤如下:
①称取
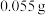 氮化硼样品,加入浓硫酸和催化剂,微热,令样品中N元素全部转为铵盐;
氮化硼样品,加入浓硫酸和催化剂,微热,令样品中N元素全部转为铵盐;②向铵盐中加入足量
 溶液并加热,蒸出的氨全部被
溶液并加热,蒸出的氨全部被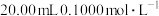 的稀硫酸溶液完全吸收;
的稀硫酸溶液完全吸收;③向稀硫酸中加入指示剂,用
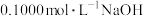 溶液滴定剩余硫酸,消耗
溶液滴定剩余硫酸,消耗 溶液平均体积为
溶液平均体积为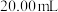 。
。氮化硼样品的纯度为
您最近一年使用:0次
5 . 碳酸锰( )用途广泛,可用作脱硫的催化剂,涂料和饲料添加剂等。某化学小组在实验室模拟用软锰矿粉(主要成分为
)用途广泛,可用作脱硫的催化剂,涂料和饲料添加剂等。某化学小组在实验室模拟用软锰矿粉(主要成分为 )制备
)制备 ,过程如下(部分操作和条件略)。已知:
,过程如下(部分操作和条件略)。已知: 不溶于水和乙醇,在干燥空气中稳定,潮湿时易被氧化;
不溶于水和乙醇,在干燥空气中稳定,潮湿时易被氧化;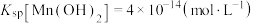 。回答下列问题:
。回答下列问题:
(1)制备 溶液:m g软锰矿粉经除杂后制得
溶液:m g软锰矿粉经除杂后制得 浊液,向
浊液,向 浊液中通入
浊液中通入 ,制得
,制得 溶液,实验装置如下图所示(夹持和加热装置略)。
溶液,实验装置如下图所示(夹持和加热装置略)。
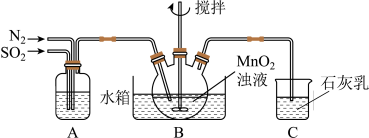
通过装置A可观察通入 与
与 的快慢,则A中加入的最佳试剂是
的快慢,则A中加入的最佳试剂是_______ ;为使 尽可能转化完全,在停止实验前应进行的操作是
尽可能转化完全,在停止实验前应进行的操作是_______ ; 转化为
转化为 的离子方程式为
的离子方程式为_______ 。实验中若将 换成空气,将导致
换成空气,将导致 浓度明显大于
浓度明显大于 浓度,原因是
浓度,原因是_______ 。
(2)制备 固体:在搅拌下向
固体:在搅拌下向 溶液中缓慢滴加
溶液中缓慢滴加 溶液,过滤,分别用蒸馏水和乙醇洗涤,低于100℃干燥,得到
溶液,过滤,分别用蒸馏水和乙醇洗涤,低于100℃干燥,得到 固体。若用同浓度的
固体。若用同浓度的 溶液代替
溶液代替 溶液,将导致制得的
溶液,将导致制得的 产品中混有
产品中混有_______ (填化学式);用乙醇洗涤的目的是_______ 。
(3)测定软锰矿中锰元素的含量:向产品中加入稍过量的磷酸和硝酸,加热使 完全转化为
完全转化为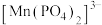 (其中
(其中 完全转化为
完全转化为 ),除去多余的硝酸,加入稍过量的硫酸铵除去
),除去多余的硝酸,加入稍过量的硫酸铵除去 ,加入稀硫酸酸化,再用
,加入稀硫酸酸化,再用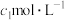 硫酸亚铁铵标准溶液滴定,发生反应
硫酸亚铁铵标准溶液滴定,发生反应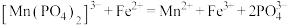 ,消耗标准液的体积平均为
,消耗标准液的体积平均为 mL;用
mL;用 mL
mL 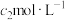 酸性
酸性 溶液恰好除去过量的
溶液恰好除去过量的 。软锰矿中锰元素的质量分数为
。软锰矿中锰元素的质量分数为_______ (用m,c,V的式子表示);用硫酸亚铁铵标准溶液滴定时,下列操作会使锰元素的质量分数偏大的是_______ (填标号)。
A.滴定管水洗后直接装入标准液 B.滴定终点时俯视滴定管读数
C.滴定管在滴定前有气泡,滴定后无气泡 D.锥形瓶未干燥即盛放待测液
 )用途广泛,可用作脱硫的催化剂,涂料和饲料添加剂等。某化学小组在实验室模拟用软锰矿粉(主要成分为
)用途广泛,可用作脱硫的催化剂,涂料和饲料添加剂等。某化学小组在实验室模拟用软锰矿粉(主要成分为 )制备
)制备 ,过程如下(部分操作和条件略)。已知:
,过程如下(部分操作和条件略)。已知: 不溶于水和乙醇,在干燥空气中稳定,潮湿时易被氧化;
不溶于水和乙醇,在干燥空气中稳定,潮湿时易被氧化;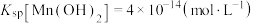 。回答下列问题:
。回答下列问题:(1)制备
 溶液:m g软锰矿粉经除杂后制得
溶液:m g软锰矿粉经除杂后制得 浊液,向
浊液,向 浊液中通入
浊液中通入 ,制得
,制得 溶液,实验装置如下图所示(夹持和加热装置略)。
溶液,实验装置如下图所示(夹持和加热装置略)。
通过装置A可观察通入
 与
与 的快慢,则A中加入的最佳试剂是
的快慢,则A中加入的最佳试剂是 尽可能转化完全,在停止实验前应进行的操作是
尽可能转化完全,在停止实验前应进行的操作是 转化为
转化为 的离子方程式为
的离子方程式为 换成空气,将导致
换成空气,将导致 浓度明显大于
浓度明显大于 浓度,原因是
浓度,原因是(2)制备
 固体:在搅拌下向
固体:在搅拌下向 溶液中缓慢滴加
溶液中缓慢滴加 溶液,过滤,分别用蒸馏水和乙醇洗涤,低于100℃干燥,得到
溶液,过滤,分别用蒸馏水和乙醇洗涤,低于100℃干燥,得到 固体。若用同浓度的
固体。若用同浓度的 溶液代替
溶液代替 溶液,将导致制得的
溶液,将导致制得的 产品中混有
产品中混有(3)测定软锰矿中锰元素的含量:向产品中加入稍过量的磷酸和硝酸,加热使
 完全转化为
完全转化为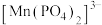 (其中
(其中 完全转化为
完全转化为 ),除去多余的硝酸,加入稍过量的硫酸铵除去
),除去多余的硝酸,加入稍过量的硫酸铵除去 ,加入稀硫酸酸化,再用
,加入稀硫酸酸化,再用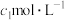 硫酸亚铁铵标准溶液滴定,发生反应
硫酸亚铁铵标准溶液滴定,发生反应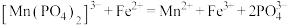 ,消耗标准液的体积平均为
,消耗标准液的体积平均为 mL;用
mL;用 mL
mL 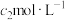 酸性
酸性 溶液恰好除去过量的
溶液恰好除去过量的 。软锰矿中锰元素的质量分数为
。软锰矿中锰元素的质量分数为A.滴定管水洗后直接装入标准液 B.滴定终点时俯视滴定管读数
C.滴定管在滴定前有气泡,滴定后无气泡 D.锥形瓶未干燥即盛放待测液
您最近一年使用:0次
6 . 实验室在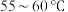 的条件下将
的条件下将 苯(密度为
苯(密度为 )与
)与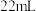 浓硫酸和
浓硫酸和 浓硝酸的混合液共热来制备硝基苯(难溶于水的油状液体),制备原理和装置如下(加热和夹持装置省略):
浓硝酸的混合液共热来制备硝基苯(难溶于水的油状液体),制备原理和装置如下(加热和夹持装置省略):
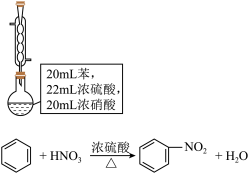
(1)实验所用苯的质量为_________ 。
(2)若该实验制备得到纯硝基苯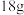 ,计算该实验中硝基苯的产率为
,计算该实验中硝基苯的产率为________ (保留小数点后两位)。
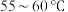 的条件下将
的条件下将 苯(密度为
苯(密度为 )与
)与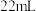 浓硫酸和
浓硫酸和 浓硝酸的混合液共热来制备硝基苯(难溶于水的油状液体),制备原理和装置如下(加热和夹持装置省略):
浓硝酸的混合液共热来制备硝基苯(难溶于水的油状液体),制备原理和装置如下(加热和夹持装置省略):
(1)实验所用苯的质量为
(2)若该实验制备得到纯硝基苯
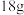 ,计算该实验中硝基苯的产率为
,计算该实验中硝基苯的产率为
您最近一年使用:0次
名校
解题方法
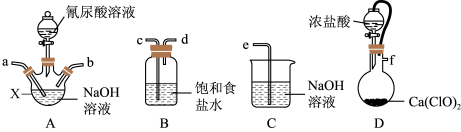
7 . 反应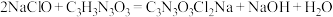 可制备广谱消毒剂
可制备广谱消毒剂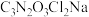 ,装置如图所示(夹持装置已略去)。下列说法错误的是
,装置如图所示(夹持装置已略去)。下列说法错误的是
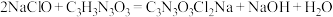 可制备广谱消毒剂
可制备广谱消毒剂 ,装置如图所示(夹持装置已略去)。下列说法错误的是
,装置如图所示(夹持装置已略去)。下列说法错误的是
| A.按气流从左至右,装置中导管连接顺序为f→c→d→a→b→e |
| B.升高温度不利于装置A中产品的生成 |
C.当加入4mol NaOH时,最多消耗氰尿酸( )1mol )1mol |
| D.装置D中橡皮管可平衡气压,便于浓盐酸顺利流下 |
您最近一年使用:0次
2023-02-06更新
|
541次组卷
|
9卷引用:考点09 氯及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)
(已下线)考点09 氯及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第1讲 氯及其化合物湖南省永州市2022届高三高考第三次适应性考试化学试题湖南省岳阳市一中2021-2022学年高三下学期第三次模拟考试试题湖南省株洲市第二中学2022-2023学年高一上学期第三次月考化学试题湖南省长沙市雅礼中学2022-2023学年高三下学期月考卷(六)化学试题 湖南省常德市第一中学2023届高三第五次月考化学试题湖南省娄底市新化县第一中学2023届高三第七次月考化学试题湖北省襄阳市第一中学2022-2023学年高一下学期4月月考化学试题
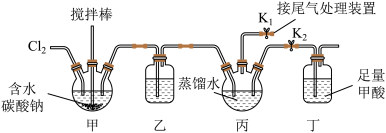
8 . 用如图装置制备次氯酸并验证其氧化性。 可以与含水碳酸钠反应得到
可以与含水碳酸钠反应得到 气体和
气体和 。下列说法错误的是
。下列说法错误的是
 可以与含水碳酸钠反应得到
可以与含水碳酸钠反应得到 气体和
气体和 。下列说法错误的是
。下列说法错误的是
A.装置甲中每生成16.8g碳酸氢钠同时生成标准状况下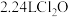 |
| B.装置乙中盛装的是浓硫酸 |
C.将装置丙中次氯酸溶液转移到装置丁中的具体操作是打开 关闭 关闭 |
| D.装置丁中溶液酸性显著增强可证明次氯酸的氧化性 |
您最近一年使用:0次
解题方法
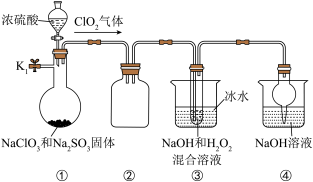
9 . NaClO2是一种高效的杀菌消毒剂,也常用来漂白织物。制备NaClO2的装置如图所示:
回答下列问题:
(1)仪器组装完毕后必须进行的实验操作是_______ 。
(2)装置②的作用是_______ 。
(3)关闭K1,从分液漏斗中加入一定量浓硫酸,装置③中生成NaClO2的化学方程式为_______ 。
(4)实验完成后,为防止装置中残留的有毒气体污染空气,可以进行的操作是:打开止水夹K1,_______ 。
(5)从装置③的溶液中获得NaClO2晶体的主要操作有减压蒸发浓缩、_______ 、过滤洗涤、干燥等。
(6)晶体以NaClO2•3H2O的形式存在,已知: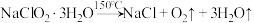 。为测定所得固体中NaClO2•3H2O的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为ag,灼烧恒重后,得到固体bg。则晶体中NaClO2•3H2O的质量分数是
。为测定所得固体中NaClO2•3H2O的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为ag,灼烧恒重后,得到固体bg。则晶体中NaClO2•3H2O的质量分数是_______ 。若发生副反应 ,则实验测得的值会
,则实验测得的值会_______ (填“偏大”“偏小”或“不变”)。

回答下列问题:
(1)仪器组装完毕后必须进行的实验操作是
(2)装置②的作用是
(3)关闭K1,从分液漏斗中加入一定量浓硫酸,装置③中生成NaClO2的化学方程式为
(4)实验完成后,为防止装置中残留的有毒气体污染空气,可以进行的操作是:打开止水夹K1,
(5)从装置③的溶液中获得NaClO2晶体的主要操作有减压蒸发浓缩、
(6)晶体以NaClO2•3H2O的形式存在,已知:
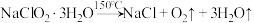 。为测定所得固体中NaClO2•3H2O的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为ag,灼烧恒重后,得到固体bg。则晶体中NaClO2•3H2O的质量分数是
。为测定所得固体中NaClO2•3H2O的质量分数,在收集到足量的晶体后,进行如下实验:取样品质量为ag,灼烧恒重后,得到固体bg。则晶体中NaClO2•3H2O的质量分数是 ,则实验测得的值会
,则实验测得的值会
您最近一年使用:0次
10 . 捕集 的技术对解决全球温室效应意义重大。回答下列问题。
的技术对解决全球温室效应意义重大。回答下列问题。
(1)国际空间站处理 的一个重要方法是将
的一个重要方法是将 还原,所涉及的反应方程式为:
还原,所涉及的反应方程式为:
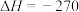
 几种化学键的键能如表所示:
几种化学键的键能如表所示:
则
______ 。
(2)将 还原为
还原为 ,是实现
,是实现 资源化利用的有效途径之一。装置如图所示:
资源化利用的有效途径之一。装置如图所示:
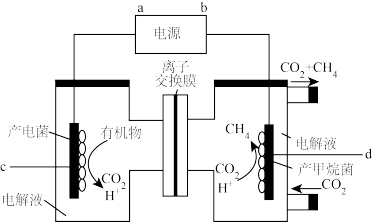
① 的移动方向为
的移动方向为______ (填“自左至右”或“自右至左”);d电极的电极反应式为____________ 。
②若电源为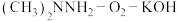 清洁燃料电池,当消耗0.1mol燃料
清洁燃料电池,当消耗0.1mol燃料 时,离子交换膜中通过
时,离子交换膜中通过______ mol ,该清洁燃料电池中的正极反应式为
,该清洁燃料电池中的正极反应式为____________ 。
(3)CaO可在较高温度下捕集 。
。 热分解可制备CaO,
热分解可制备CaO, 加热升温过程中固体的质量变化如图。
加热升温过程中固体的质量变化如图。
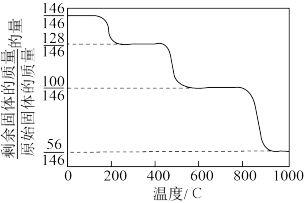
则400~600℃时分解得到的气体产物是______ (填化学式),写出800∼1000℃范围内分解反应的化学方程式:__________________________________________ 。
 的技术对解决全球温室效应意义重大。回答下列问题。
的技术对解决全球温室效应意义重大。回答下列问题。(1)国际空间站处理
 的一个重要方法是将
的一个重要方法是将 还原,所涉及的反应方程式为:
还原,所涉及的反应方程式为:
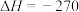
 几种化学键的键能如表所示:
几种化学键的键能如表所示:化学键 |
|
|
|
|
键能/kJ⋅mol | 413 | 436 | a | 745 |

(2)将
 还原为
还原为 ,是实现
,是实现 资源化利用的有效途径之一。装置如图所示:
资源化利用的有效途径之一。装置如图所示:
①
 的移动方向为
的移动方向为②若电源为
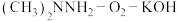 清洁燃料电池,当消耗0.1mol燃料
清洁燃料电池,当消耗0.1mol燃料 时,离子交换膜中通过
时,离子交换膜中通过 ,该清洁燃料电池中的正极反应式为
,该清洁燃料电池中的正极反应式为(3)CaO可在较高温度下捕集
 。
。 热分解可制备CaO,
热分解可制备CaO, 加热升温过程中固体的质量变化如图。
加热升温过程中固体的质量变化如图。
则400~600℃时分解得到的气体产物是
您最近一年使用:0次








