1 .  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.标准状况下, 完全反应,转移电子数目一定为 完全反应,转移电子数目一定为 |
B.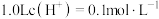 的 的 溶液中 溶液中 的数目为 的数目为 |
C.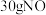 与 与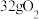 混合后所含原子总数小于 混合后所含原子总数小于 |
D.若核反应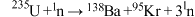 ( (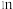 为中子)体系内中子增加 为中子)体系内中子增加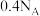 ,则消耗 ,则消耗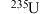 质量为 质量为 |
您最近半年使用:0次
解题方法
2 . 如图是某学校实验室从化学试剂商店买回来的氢氧化钠试剂标签上的部分内容。某同学从该试剂瓶中取出24.0 g固体,配成1 L溶液,请计算:
(1)所得氢氧化钠溶液的物质的量浓度为___________ 。
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为___________ 。(写出解答步骤)
| 氢氧化钠 化学纯(CP) 500 g 品名:氢氧化钠 化学式:NaOH 相对分子质量:40 |
(2)从所得氢氧化钠溶液中取出200 mL于一烧杯中,投入2.7 g的金属铝,产生的气体在标准状况下的体积为
您最近半年使用:0次
3 . 氯及其化合物的价类二维图如图,回答下列问题: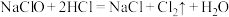 。写出反应①离子方程式
。写出反应①离子方程式___________ ;反应②中HCl体现的性质是___________ 。
(2)溶质质量分数为36.5%、密度为1.2g/cm3的浓盐酸中,盐酸的物质的量浓度为___________ mol/L,取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是___________ 。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)若用(2)中浓盐酸配制500 mL0.3mol/L稀盐酸。该学生需要用量筒量取___________ mL上述浓盐酸进行配制。完成此实验需用到的玻璃仪器除了量筒、烧杯、玻璃棒、胶头滴管外,还需要___________ 。
(4)现将200 mL0.3 mol/L盐酸与300 mL0.4 mol/LCuCl2溶液混合,溶液体积变化忽略不计,所得溶液中Cl-的物质的量浓度是___________ mol/L。
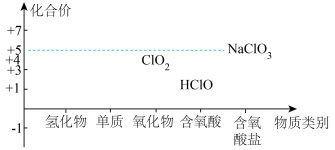
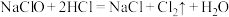 。写出反应①离子方程式
。写出反应①离子方程式(2)溶质质量分数为36.5%、密度为1.2g/cm3的浓盐酸中,盐酸的物质的量浓度为
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)若用(2)中浓盐酸配制500 mL0.3mol/L稀盐酸。该学生需要用量筒量取
(4)现将200 mL0.3 mol/L盐酸与300 mL0.4 mol/LCuCl2溶液混合,溶液体积变化忽略不计,所得溶液中Cl-的物质的量浓度是
您最近半年使用:0次
名校
4 . 将amol钠和amol铝一同投入mg足量水中,所得溶液密度为dg·mL-1,该溶液中溶质的质量分数和物质的量浓度为分别
| A.8200a/(46+m)% | B.11800a/(46+m)% |
| C.1000ad/(46+m)mol/L | D.1000ad/(46+2m)mol/L |
您最近半年使用:0次
名校
5 . 某 混合液中,
混合液中, 和
和 的物质的量浓度分别为
的物质的量浓度分别为 和
和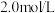 。向该混合液中加入
。向该混合液中加入 铜粉,加热,待充分反应后,所得溶液中
铜粉,加热,待充分反应后,所得溶液中 的物质的量浓度为(忽略反应前后溶液体积变化)
的物质的量浓度为(忽略反应前后溶液体积变化)
 混合液中,
混合液中, 和
和 的物质的量浓度分别为
的物质的量浓度分别为 和
和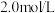 。向该混合液中加入
。向该混合液中加入 铜粉,加热,待充分反应后,所得溶液中
铜粉,加热,待充分反应后,所得溶液中 的物质的量浓度为(忽略反应前后溶液体积变化)
的物质的量浓度为(忽略反应前后溶液体积变化)A. | B. | C. | D. |
您最近半年使用:0次
6 .  为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.100g46%的乙醇溶液中含有O-H键的数目为 |
B.标准状况下,11.2LHF中电子的数目为 |
C.pH=1的 溶液中 溶液中 的数目为 的数目为 |
D.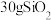 中含有的Si-O键数目为 中含有的Si-O键数目为 |
您最近半年使用:0次
名校
7 . 标况下,将某气体X充满一个干燥烧瓶,将烧瓶倒立于水槽中,瓶内液面上升(假设烧瓶内液体未扩散水槽)最后烧瓶中溶质的物质的量浓度最小的是
| A.X为NH3 | B.X为NO2 |
| C.X为NO2和O2(体积比为4:1) | D.X为NO和O2(体积比为4:3) |
您最近半年使用:0次
2024-04-15更新
|
84次组卷
|
2卷引用:福建省福州市闽侯县第一中学2023-2024学年高一下学期3月月考化学试题
8 . 一种电化学还原制氨气的反应为: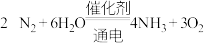 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
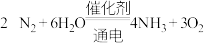 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.标准状况下,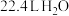 含有的分子数为 含有的分子数为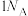 |
B.标准状况下,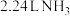 含有质子的数目为 含有质子的数目为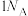 |
C. 氨水中,含有的 氨水中,含有的 分子数等于 分子数等于 |
D.每消耗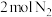 ,理论上电子转移的数目为 ,理论上电子转移的数目为 |
您最近半年使用:0次
名校
9 . 设 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是
 表示阿伏加德罗常数的值,下列叙述正确的是
表示阿伏加德罗常数的值,下列叙述正确的是A. 熔融态时含有 熔融态时含有 个离子 个离子 |
B. 和 和 混合气体中氧原子总数为 混合气体中氧原子总数为 |
C.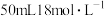 硫酸与足量铜共热,转移的电子数为 硫酸与足量铜共热,转移的电子数为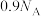 |
D. 的 的 水溶液中含有的氧原子数为 水溶液中含有的氧原子数为 |
您最近半年使用:0次
名校
10 . 将32g铜与140mL一定浓度的硝酸反应,铜完全溶解产生的NO和 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:
(1)NO的体积为___________ L, 的体积为
的体积为___________ L。
(2)参加反应的硝酸的物质的量是___________ mol。
(3)待产生的气体全部释放后,向溶液加入V mL a mol/L的NaOH溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为___________ mol/L。(结果不需化简)
(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为 ,至少需要30%的双氧水
,至少需要30%的双氧水_________ g。
 混合气体在标准状况下的体积为11.2L。请回答:
混合气体在标准状况下的体积为11.2L。请回答:(1)NO的体积为
 的体积为
的体积为(2)参加反应的硝酸的物质的量是
(3)待产生的气体全部释放后,向溶液加入V mL a mol/L的NaOH溶液,恰好使溶液中的
 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为(4)欲使铜与硝酸反应生成的气体在NaOH溶液中全部转化为
 ,至少需要30%的双氧水
,至少需要30%的双氧水
您最近半年使用:0次



