名校
解题方法
1 . Ι.完成下列反应的离子反应方程式
(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式:___________ ;常用澄清石灰水检验CO2气体的离子方程式是___________________________ 。
(2)表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是_______________ ;反应片刻后,可观察到有气体产生,其离子方程式是________________________ 。
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为___________________ 。
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为__________ 。
(4)碳酸钙与醋酸反应____________________
(5) NaHCO3 溶液和 NaOH混合________________
书写离子方程式时,哪些物质不能写成离子_____________________
II.配平下列反应
① KMnO4+ K2SO3+ H2O=____ MnO2+____ K2SO4+ KOH_______________ 。
② K2Cr2O7+ KI+ H2SO4= K2SO4+ Cr2(SO4)3+ I2+ H2O______________ 。
氧化还原方程式的配平依据是____________________
(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式:
(2)表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是
(3)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为
②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为
(4)碳酸钙与醋酸反应
(5) NaHCO3 溶液和 NaOH混合
书写离子方程式时,哪些物质不能写成离子
II.配平下列反应
① KMnO4+ K2SO3+ H2O=____ MnO2+____ K2SO4+ KOH
② K2Cr2O7+ KI+ H2SO4= K2SO4+ Cr2(SO4)3+ I2+ H2O
氧化还原方程式的配平依据是
您最近一年使用:0次
2 . 现有下列10种物质:①铝 ②硫酸溶液 ③CO2 ④H2SO4 ⑤Ba(OH)2 ⑥胆矾 ⑦盐酸 ⑧NaHSO4 ⑨碳酸钙 ⑩乙醇
(1)上述物质中属于电解质的有_______ ,非电解质__________ ,能导电的有_____ (填序号)。
电解质与非电解质都属于______________ ,电解质包括哪些物质类别________________________________________________
(2)⑧在水中的电离方程式为___________________________________________ 。
(3)向⑧溶液中逐滴滴加⑤溶液至恰好中和,发生反应的离子方程式为_______ ;
(4)⑨和⑦混合,反应的离子方程式为_____________________________________ 。
(1)上述物质中属于电解质的有
电解质与非电解质都属于
(2)⑧在水中的电离方程式为
(3)向⑧溶液中逐滴滴加⑤溶液至恰好中和,发生反应的离子方程式为
(4)⑨和⑦混合,反应的离子方程式为
您最近一年使用:0次
名校
解题方法
3 . 下列离子方程式正确的是
A. 溶于足量的NaOH溶液: 溶于足量的NaOH溶液: |
B. 与 与 反应: 反应: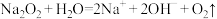 |
C.氯气与水的反应: |
D.盐酸中滴加氨水: |
您最近一年使用:0次
2021-01-18更新
|
275次组卷
|
3卷引用:天津市部分区2019-2020学年高一上学期期末考试化学试题
20-21高一上·浙江绍兴·阶段练习
名校
解题方法
4 . 能正确表示下列变化的离子方程式是
| A.磁性氧化铁溶于足量稀盐酸:Fe3O4+8H+=2Fe2++Fe3++4H2O |
B.Na2O2溶于水产生O2:2 +2H2O=4OH-+O2↑ +2H2O=4OH-+O2↑ |
C.NH4HCO3溶液和过量Ca(OH)2溶液混合:Ca2++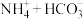 +2OH-=CaCO3↓+H2O+NH3·H2O +2OH-=CaCO3↓+H2O+NH3·H2O |
| D.氯化铝溶液中加入足量氨水Al3++3OH-=Al(OH)3↓ |
您最近一年使用:0次
名校
解题方法
5 . 下列反应的离子方程式书写正确的是
A.Fe与 溶液反应: 溶液反应: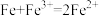 |
B.稀盐酸与KOH溶液反应: |
C. 与稀盐酸反应: 与稀盐酸反应: |
D.FeO与稀硫酸反应: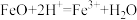 |
您最近一年使用:0次
2021-01-12更新
|
556次组卷
|
9卷引用:北京市西城区2019-2020学年高一上学期期末考试化学试题
北京市西城区2019-2020学年高一上学期期末考试化学试题北京市育才学校2020-2021高一上学期期中考试化学试题天津市和平区2021-2022学年高一上学期线上期末质量检测化学试题天津市武清区黄花店中学2023-2024学年高一上学期第二次形成性练习化学试题专题3 第二单元 第3课时 离子反应-高中化学苏教2019版必修第一册北京临川育人学校2021-2022学年高二上学期开学考试化学试题安徽省桐城中学2021-2022学年高二上学期综合测试化学试题甘肃省天水市秦安县第一中学2022-2023学年高一上学期10月期中考试化学试题北京市第十五中学2022-2023学年高一上学期12月月考化学试题
名校
解题方法
6 . 下列反应的离子方程式书写正确的是
A.用KIO3氧化酸性溶液中的KI:5I- + +3H2O═3I2+6OH- +3H2O═3I2+6OH- |
B.向NH4HCO3溶液中加过量的NaOH溶液并加热: +OH- +OH- NH3↑+H2O NH3↑+H2O |
C.将过量SO2通入冷氨水中:SO2+NH3·H2O═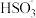 + + |
D.用稀硝酸洗涤试管内壁的银镜:Ag+2H++ ═Ag++NO↑+H2O ═Ag++NO↑+H2O |
您最近一年使用:0次
2021-01-08更新
|
438次组卷
|
6卷引用:2015届山东省青岛市高三上学期期末考试化学试卷
名校
7 . 某学习小组通过实验研究Na2O2与水的反应。
(1)甲同学认为ⅱ中溶液褪色是溶液a中存在较多的H2O2,H2O2与酚酞发生了反应,并实验证实了H2O2的存在;取少量溶液a,加入试剂____ (填化学式),有气体产生。
(2)乙同学查阅资料获悉:用KMnO4可以氧化H2O2并测定其含量。取20.00mL溶液,用稀H2SO4酸化,用0.002mol/LKMnO4溶液滴定,产生气体,溶液褪色,至终点时共消耗10.00mLKMnO4溶液。
①实验中,滴定时KMnO4溶液应装在____ (酸或碱)式滴定管中。
②配平并用用单线桥标出该反应电子转移的方向和数目:___
MnO +H2O2+H+=Mn2++O2↑+H2O
+H2O2+H+=Mn2++O2↑+H2O
③溶液a中c(H2O2)=____ mol/L。
| 操作 | 现象 |
| 向盛有4.0gNa2O2的烧杯中加入50mL蒸馏水 | 剧列反应,产生能使带火星木条复燃的气体,得到的无色溶液a |
| 向溶液a中滴入两滴酚酞 | ⅰ.溶液变红 ⅱ.10分钟后溶液颜色明显变浅,稍后,溶液变为无色 |
(1)甲同学认为ⅱ中溶液褪色是溶液a中存在较多的H2O2,H2O2与酚酞发生了反应,并实验证实了H2O2的存在;取少量溶液a,加入试剂
(2)乙同学查阅资料获悉:用KMnO4可以氧化H2O2并测定其含量。取20.00mL溶液,用稀H2SO4酸化,用0.002mol/LKMnO4溶液滴定,产生气体,溶液褪色,至终点时共消耗10.00mLKMnO4溶液。
①实验中,滴定时KMnO4溶液应装在
②配平并用用单线桥标出该反应电子转移的方向和数目:
MnO
 +H2O2+H+=Mn2++O2↑+H2O
+H2O2+H+=Mn2++O2↑+H2O③溶液a中c(H2O2)=
您最近一年使用:0次
名校
8 . (1)某反应体系中有H2O、ClO-、 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式___ ,消耗1 mol还原剂,转移电子数为___ 。

(2)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1∶16,则x的值为___ 。
(3)足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.12 LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是_____ mL。
(4)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
①H3PO2是一元中强酸,写出其电离方程式:___ 。
②H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银,利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,写出化学镀银反应的化学方程式___ 。
 、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
、OH-、N2、Cl-等微粒,其中N2、ClO-的物质的量随时间变化的曲线如图所示,写出该反应的离子方程式
(2)Na2Sx在碱性溶液中可被NaClO氧化为Na2SO4,而NaClO被还原为NaCl,若反应中Na2Sx与NaClO的物质的量之比为1∶16,则x的值为
(3)足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.12 LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5 mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
(4)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列问题:
①H3PO2是一元中强酸,写出其电离方程式:
②H3PO2及NaH2PO2均可将溶液中的银离子还原为银单质,从而可用于化学镀银,利用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,写出化学镀银反应的化学方程式
您最近一年使用:0次
名校
解题方法
9 . 下列离子方程式正确的是
①纯碱溶液中滴加少量盐酸:CO +H+=HCO
+H+=HCO
②NH4HCO3溶液与过量NaOH溶液反应:NH +OH-=NH3↑+H2O
+OH-=NH3↑+H2O
③FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
④NaHSO4与等物质的量的Ba(OH)2溶液反成:H++SO +Ba2++OH-=BaSO4↓+H2O
+Ba2++OH-=BaSO4↓+H2O
⑤小苏打溶液中加入少量的石灰水:Ca2++2OH-+2HCO =CaCO3↓+CO
=CaCO3↓+CO +2H2O
+2H2O
⑥Fe(OH)3与氢碘酸溶液混合:Fe(OH)3+3H+=Fe3++3H2O
①纯碱溶液中滴加少量盐酸:CO
 +H+=HCO
+H+=HCO
②NH4HCO3溶液与过量NaOH溶液反应:NH
 +OH-=NH3↑+H2O
+OH-=NH3↑+H2O③FeBr2溶液中通入过量Cl2:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl-
④NaHSO4与等物质的量的Ba(OH)2溶液反成:H++SO
 +Ba2++OH-=BaSO4↓+H2O
+Ba2++OH-=BaSO4↓+H2O⑤小苏打溶液中加入少量的石灰水:Ca2++2OH-+2HCO
 =CaCO3↓+CO
=CaCO3↓+CO +2H2O
+2H2O⑥Fe(OH)3与氢碘酸溶液混合:Fe(OH)3+3H+=Fe3++3H2O
| A.①④⑤ | B.②③⑤ | C.③④⑥ | D.①⑤⑥ |
您最近一年使用:0次
2021-01-08更新
|
293次组卷
|
2卷引用:天津市静海区第一中学2021届高三12月考化学试题
名校
解题方法
10 . 下列反应的离子方程式书写正确的是
| A.稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
B.稀硫酸与氢氧化钡溶液混合: +2H++2OH−+Ba2+=BaSO4↓+2H2O +2H++2OH−+Ba2+=BaSO4↓+2H2O |
| C.稀硝酸滴在大理石上:CaCO3+2H+=Ca2++H2CO3 |
| D.铜与硝酸银溶液反应Cu+Ag+=Cu2++Ag |
您最近一年使用:0次



