21-22高三上·江苏南通·期末
名校
解题方法
1 . 用化学方法降解水中有机物已成为污水处理领域的重要研究方向。
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。
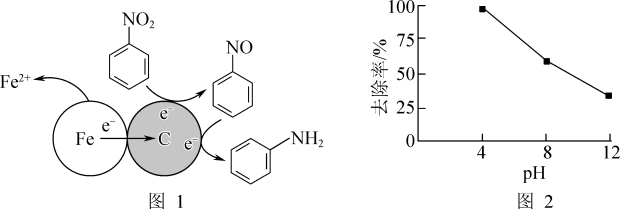
①该物质转化示意图可以描述为_______ 。
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是_______ 。
(2)向含Fe2+和苯胺(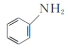 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:_______ 。
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:_______ 。
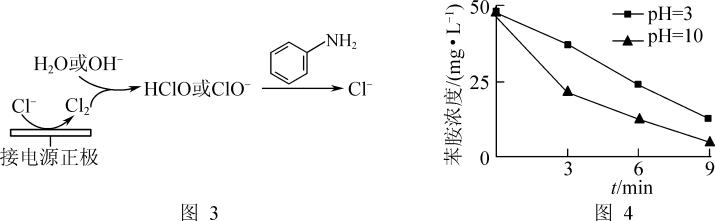
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是_______ 。[已知氧化性:HClO(H+)>ClO-(OH-)]
(1)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图1所示。

①该物质转化示意图可以描述为
②其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图2所示。pH越大,硝基苯的去除率越低的原因是
(2)向含Fe2+和苯胺(
 )的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O
)的酸性溶液中加入双氧水,会发生如下反应:Fe2++H++H2O2=Fe3++HO·+H2O①HO·(羟基自由基)具有强氧化性,能将溶液中的苯胺氧化成CO2和N2。写出该反应的离子方程式:
②H2O2也具有氧化性,设计验证苯胺是被HO·氧化而不是被H2O2氧化的实验方案:
(3)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图3所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图4所示。反应相同时间,初始溶液pH=3时苯胺浓度大于pH=10时的原因是

您最近一年使用:0次
名校
解题方法
2 . 从矿物学资料查得,一定条件下自然界中存在反应 。(其中
。(其中 中Fe为+2价S为-1价)下列说法正确的是
中Fe为+2价S为-1价)下列说法正确的是
 。(其中
。(其中 中Fe为+2价S为-1价)下列说法正确的是
中Fe为+2价S为-1价)下列说法正确的是A. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
B.参与反应的 与转移电子数之比为1∶2 与转移电子数之比为1∶2 |
C. 只作还原剂 只作还原剂 |
D.产物中的 有一部分是氧化产物 有一部分是氧化产物 |
您最近一年使用:0次
2022-01-13更新
|
2084次组卷
|
4卷引用:辽宁省建平县实验中学2023-2024学年高一上学期11月期中化学试题
3 . As(0)、As(Ⅲ)和As(V)分别表示砷单质、三价砷和五价砷的化合物。硫酸厂产生的酸性废水中含有超标的H3AsO3,需处理达标后才能排放。目前含砷废水的处理常用石灰中和-PFS、氧化吸附、纳米级零价铁等方法。
(1)石灰中和-PFS法,处理过程如下:
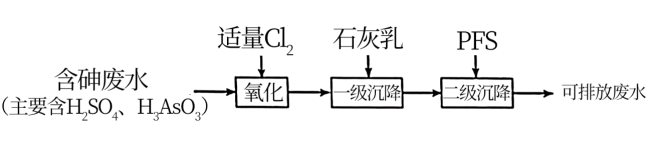
含砷废水经氧化后,加入石灰乳,在相同时间内,废水中沉降的固体、砷的去除率与溶液pH的关系如图1所示。H3AsO3水溶液中含砷微粒的物质的量分布分数与pH的关系如图2所示。已知此温度下,Ca(H2AsO4)2溶于水,Ksp(FeAsO4)=5.7×10-21,Ksp[Ca3(AsO4)2] =6.8×10-19,Ksp(CaHAsO4)=8.4×10-4,。
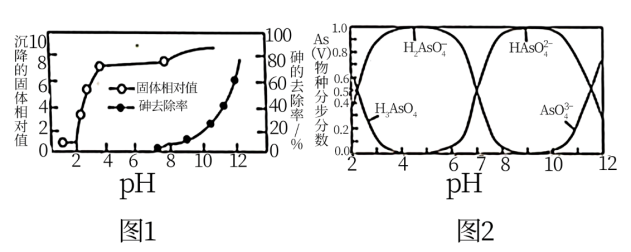
①一级沉降时,当pH=2,废水中开始产生沉淀,该沉淀主要成分的化学式为___________ 。pH调节到8时,开始产生Ca3(AsO4)2沉淀,原因是___________ 。
②二级沉降中,保持溶液pH在8-10之间。加入PFS(聚合硫酸铁,[(Fe2(OH)2n(SO4)3-n]m)形成的Fe(OH)3胶体粒子与含砷微粒反应可提高砷的去除率,其主要反应的离子方程式为___________ 。
(2)氧化吸附法:新生态MnO2悬浊液具有较强的氧化性,能将As(Ⅲ)氧化为As(V),也具有较强的吸附性,能吸附水体中的H+而带正电荷。所带正电荷越多,吸附含砷微粒的能力越强。pH不同时,新生态MnO2悬浊液对砷去除率如图所示。
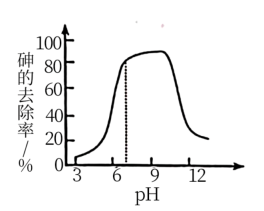
①加入新生态MnO2悬浊液使废水中H3AsO3转化为H3AsO4反应的离子方程式为___________ 。
②pH从3增大到7的过程中,随着pH增大,砷的去除率上升。其原因是___________ 。
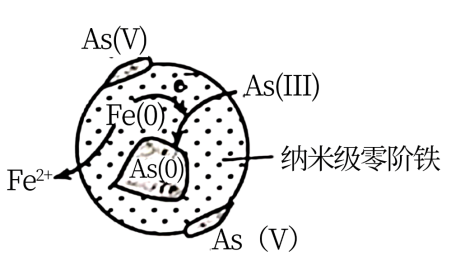
(3)纳米级零价铁法:纳米级零价铁具有强吸附性和还原性,可直接处理有氧条件下含As(Ⅰ)较多的废水。处理后在纳米级零价铁表面有大量的As(0),外围有大量的As(V)。产生As(0)的原理如图所示。请描述产生As(0)、As(V)的过程:___________ 。
(1)石灰中和-PFS法,处理过程如下:

含砷废水经氧化后,加入石灰乳,在相同时间内,废水中沉降的固体、砷的去除率与溶液pH的关系如图1所示。H3AsO3水溶液中含砷微粒的物质的量分布分数与pH的关系如图2所示。已知此温度下,Ca(H2AsO4)2溶于水,Ksp(FeAsO4)=5.7×10-21,Ksp[Ca3(AsO4)2] =6.8×10-19,Ksp(CaHAsO4)=8.4×10-4,。

①一级沉降时,当pH=2,废水中开始产生沉淀,该沉淀主要成分的化学式为
②二级沉降中,保持溶液pH在8-10之间。加入PFS(聚合硫酸铁,[(Fe2(OH)2n(SO4)3-n]m)形成的Fe(OH)3胶体粒子与含砷微粒反应可提高砷的去除率,其主要反应的离子方程式为
(2)氧化吸附法:新生态MnO2悬浊液具有较强的氧化性,能将As(Ⅲ)氧化为As(V),也具有较强的吸附性,能吸附水体中的H+而带正电荷。所带正电荷越多,吸附含砷微粒的能力越强。pH不同时,新生态MnO2悬浊液对砷去除率如图所示。

①加入新生态MnO2悬浊液使废水中H3AsO3转化为H3AsO4反应的离子方程式为
②pH从3增大到7的过程中,随着pH增大,砷的去除率上升。其原因是
(3)纳米级零价铁法:纳米级零价铁具有强吸附性和还原性,可直接处理有氧条件下含As(Ⅰ)较多的废水。处理后在纳米级零价铁表面有大量的As(0),外围有大量的As(V)。产生As(0)的原理如图所示。请描述产生As(0)、As(V)的过程:

您最近一年使用:0次
名校
解题方法
4 . 取一定质量的NaBr、NaI的混合物平均分成五等分,分别加水配成溶液并编号为甲、乙、丙、丁、戊,再分别向各溶液中通入一定体积的氯气,将反应后所得溶液蒸干灼烧得固体,通入氯气的体积与最终所得固体质量记录如下:
下列实验结论正确的是
| 编号 | 甲 | 乙 | 丙 | 丁 | 戊 |
| 固体组成 | NaCl | ||||
| Cl2的体积/mL | V | 2V | 3V | 4V | 5V |
| 固体质量/g | 54.62 | 43.64 | 35.48 | 30.14 | 29.25 |
| A.甲溶液中发生的反应是Cl2+2Br-=2Cl-+Br2 |
| B.乙中固体组成为NaBr、NaCl |
| C.标准状况下Cl2的体积V为2688mL |
| D.原混合物中NaBr的物质的量为1mol |
您最近一年使用:0次
2020-11-19更新
|
1663次组卷
|
5卷引用:江西省赣州市全南中学2023-2024学年高三上学期11月期中考试化学试题
江西省赣州市全南中学2023-2024学年高三上学期11月期中考试化学试题广东省深圳外国语学校2021届高三第二次月考化学试题(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密07 非金属及其化合物(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)
名校
5 . 足量的铜与一定量的浓硝酸充分反应,得到4.48L(标准状况)NO2与NO的混合气体,这些气体与一定体积的O2混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入100mL4mol·L-1NaOH溶液,Cu2+恰好沉淀完全。下列说法正确的是
| A.此反应过程中转移了0.5mol的电子 |
| B.消耗氧气的体积为1.12L(标准状况) |
| C.参加反应的HNO3是0.45mol |
| D.混合气体中含2.24L(标准状况)NO |
您最近一年使用:0次
2020-07-22更新
|
3034次组卷
|
11卷引用:云南省曲靖市第一中学2022-2023学年高一下学期期末考试化学试题
云南省曲靖市第一中学2022-2023学年高一下学期期末考试化学试题安徽省铜陵市第一中学2022-2023 学年高一下学期期中教学质量检测化学试题云南省开远市第一中学校2022-2023学年高一下学期期末考试化学试题辽宁省大连市旅顺口区2019-2020学年高一下学期期末考试化学试题辽宁省大连市2019-2020学年高一下学期期末考试化学试题重庆市缙云教育联盟2020-2021学年高一9月月考化学试题山西省实验中学2020-2021学年高一下学期第一次月考化学试题辽宁省大连市一0三中学2020-2021学年高一4月月考化学试题辽宁省部分中学2019-2020高一下学期期末考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高一下学期4月月考化学试题重庆市万州第二高级中学2023-2024学年高一下学期3月月考试题 化学试题
名校
6 . 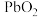 是褐色固体,受热分解为Pb的
是褐色固体,受热分解为Pb的 和
和 价的混合氧化物,
价的混合氧化物, 价的Pb能氧化浓盐酸生成
价的Pb能氧化浓盐酸生成 ,
, 价的Pb还原成
价的Pb还原成 价的Pb;现将
价的Pb;现将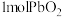 加热分解得到
加热分解得到 ,向剩余固体中加入足量的浓盐酸得到
,向剩余固体中加入足量的浓盐酸得到 ,
, 和
和 的物质的量之比为
的物质的量之比为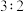 ,则剩余固体的组成及物质的量比是
,则剩余固体的组成及物质的量比是
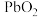 是褐色固体,受热分解为Pb的
是褐色固体,受热分解为Pb的 和
和 价的混合氧化物,
价的混合氧化物, 价的Pb能氧化浓盐酸生成
价的Pb能氧化浓盐酸生成 ,
, 价的Pb还原成
价的Pb还原成 价的Pb;现将
价的Pb;现将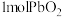 加热分解得到
加热分解得到 ,向剩余固体中加入足量的浓盐酸得到
,向剩余固体中加入足量的浓盐酸得到 ,
, 和
和 的物质的量之比为
的物质的量之比为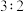 ,则剩余固体的组成及物质的量比是
,则剩余固体的组成及物质的量比是A. 混合的 混合的 、 、 | B.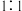 混合的 混合的 、PbO 、PbO |
C.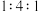 混合的 混合的 、 、 、PbO 、PbO | D.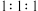 混合的 混合的 、 、 、PbO 、PbO |
您最近一年使用:0次
2020-02-06更新
|
1480次组卷
|
5卷引用:湖北省武汉市华中师范大学第一附属中学2022-2023学年高一下学期4月期中考试化学试题
名校
解题方法
7 . 有关 反应的叙述正确的为
反应的叙述正确的为
 反应的叙述正确的为
反应的叙述正确的为| A.还原剂与氧化剂物质的量之比为5:3 |
| B.生成lmolO2,反应共转移4mol电子 |
C.若有5mol水做还原剂时,被BrF3还原的BrF3为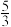 mol mol |
| D.若有5mol水参与反应时,被水还原的BrF3为2mol |
您最近一年使用:0次
2019-11-24更新
|
2665次组卷
|
7卷引用:辽宁省沈阳市第一二〇中学2022-2023学年高一下学期期初质量监测化学试题
名校
8 . 汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则下列判断不正确的是
| A.生成44.8L N2(标准状况) |
| B.有0.25 mol KNO3被还原 |
| C.转移电子的物质的量为1.75mol |
| D.被氧化的N原子的物质的量为3.75mol |
您最近一年使用:0次
2019-07-05更新
|
9182次组卷
|
8卷引用:湖南省邵阳市第二中学2023-2024学年高一上学期基础知识竞赛化学试题
真题
名校
9 . 聚合硫酸铁[Fe(OH)SO4]n能用作净水剂(絮凝剂),可由绿矾(FeSO4·7H2O)和KClO3在水溶液中反应得到。下列说法不正确 的是
| A.KClO3作氧化剂,每生成1 mol [Fe(OH)SO4]n消耗6/n mol KClO3 |
| B.生成聚合硫酸铁后,水溶液的pH增大 |
| C.聚合硫酸铁可在水中形成氢氧化铁胶体而净水 |
| D.在相同条件下,Fe3+比[Fe(OH)]2+的水解能力更强 |
您最近一年使用:0次
2019-04-12更新
|
5924次组卷
|
36卷引用:第三章 金属及其化合物 第13讲 铁及其重要化合物
第三章 金属及其化合物 第13讲 铁及其重要化合物湖南省株洲市第四中学2023届高三第六次月考化学试题(已下线)题型27 铁及其化合物的性质、用途及相关计算重庆市万州第二高级中学2022-2023学年高三下学期5月月考化学试题(已下线)2019年高考浙江卷化学试题变式题(单选题21-25)北京市第八十中学2024届高三上学期10月月考化学试题化学江苏省扬州市宝应区2023-2024学年曹甸高级中学高三上学期9月化学试卷2019年4月浙江省普通高校招生选考科目考试化学试题福建省华安一中2018-2019学年高二下学期期末考试化学试题湖南省长沙市第一中学2020届高三第一次月考化学试题江西省宜春市奉新县第一中学2020届高三上学期第二次月考化学试题黑龙江省牡丹江市第一高级中学2020届高三10月月考化学试题河北省邯郸市2019-2020学年高三上学期期中考试化学试题2020届高考化学小题狂练(全国通用版)专练5 氧化还原反应辽宁省抚顺市第一中学2020届高三上学期期中考试化学试题江西省吉安市五校2019-2020学年高二上学期第二次联考化学试题2020届高三化学化学二轮复习——高考常考题:氧化还原反应的实际应用【精编选择25题】专题1.3 氧化还原反应(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专题六 元素化合物的性质、应用及转化(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训(已下线)小题必刷08 氧化还原反应的规律及应用——2021年高考化学一轮复习小题必刷(通用版)广东省佛山市第一中学2020-2021学年高二上学期期中考试化学(选考)试题安徽省池州市第一中学2020-2021学年高二12月月考化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练上海交通大学附属中学2021届高三下学期3月月考化学试题(已下线)课时17 铁及其化合物-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点15 铁及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)3.3.1 盐类的水解-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)专题05.元素及其化合物-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)考向26 盐类的水解-备战2022年高考化学一轮复习考点微专题(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)湖南省长沙市雅礼中学2022-2023学年高三上学期第五次月考化学试题新疆喀什地区伽师县2022-2023学年高三上学期11月期中考试化学试题
名校
10 . 向含a mol NaClO的溶液通入b mol SO2充分反应(不考虑二氧化硫与水之间的反应以及次氯酸的分解)。下列说法不正确的是
A.当0<b<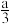 时:SO2+H2O+3ClO-= 时:SO2+H2O+3ClO-= +2HClO+Cl- +2HClO+Cl- |
B.当b=a时:SO2+H2O+ClO-= +2H++Cl- +2H++Cl- |
C.当 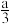 <b<a时;反应后溶液中H+的物质的量:0<n(H+)<2bmol <b<a时;反应后溶液中H+的物质的量:0<n(H+)<2bmol |
D.当0<b<a时;反应后溶液中Cl-、ClO-和 物质的量之比为:(a-b):b:b 物质的量之比为:(a-b):b:b |
您最近一年使用:0次
2017-05-27更新
|
700次组卷
|
4卷引用:安徽省亳州市蒙城县五校联考2023-2024学年高三上学期11月期中考试化学试题



