名校
解题方法
1 . 氮、磷及其化合物在科研及生产中均有着重要的应用。
(1)三氟化氮( )气体是一种新型电子材料。其中N元素的化合价为
)气体是一种新型电子材料。其中N元素的化合价为______ ,它在潮湿的空气中与水蒸气能发生反应生成HF、NO和HNO。反应过程中,被氧化与被还原的元素的质量之比为______ 。
(2)联氨( )是一种常用的强还原剂。可用以下方法制得(装置如右图):NaClO碱性溶液与尿素[化学式为
)是一种常用的强还原剂。可用以下方法制得(装置如右图):NaClO碱性溶液与尿素[化学式为 ,沸点196.6℃]水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。滴液漏斗内的试剂是
,沸点196.6℃]水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。滴液漏斗内的试剂是______ ;制备联氨的离子方程式为______ 。 与澄清石灰水混合,溶液体积为2L,半分钟后的
与澄清石灰水混合,溶液体积为2L,半分钟后的 的物质的量减少了0.2mol,
的物质的量减少了0.2mol,
______ 。
(4)已知: 分子中的键能为a kJ/mol;
分子中的键能为a kJ/mol; 分子中
分子中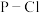 键能为b kJ/mol;1mol
键能为b kJ/mol;1mol 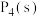 转化为气态P原子吸收能量c kJ。写出
转化为气态P原子吸收能量c kJ。写出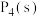 与
与 反应生成
反应生成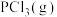 的热化学方程式:
的热化学方程式:______ 。
(1)三氟化氮(
 )气体是一种新型电子材料。其中N元素的化合价为
)气体是一种新型电子材料。其中N元素的化合价为(2)联氨(
 )是一种常用的强还原剂。可用以下方法制得(装置如右图):NaClO碱性溶液与尿素[化学式为
)是一种常用的强还原剂。可用以下方法制得(装置如右图):NaClO碱性溶液与尿素[化学式为 ,沸点196.6℃]水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。滴液漏斗内的试剂是
,沸点196.6℃]水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。滴液漏斗内的试剂是
 与澄清石灰水混合,溶液体积为2L,半分钟后的
与澄清石灰水混合,溶液体积为2L,半分钟后的 的物质的量减少了0.2mol,
的物质的量减少了0.2mol,
(4)已知:
 分子中的键能为a kJ/mol;
分子中的键能为a kJ/mol; 分子中
分子中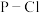 键能为b kJ/mol;1mol
键能为b kJ/mol;1mol 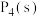 转化为气态P原子吸收能量c kJ。写出
转化为气态P原子吸收能量c kJ。写出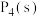 与
与 反应生成
反应生成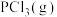 的热化学方程式:
的热化学方程式:
您最近一年使用:0次
名校
2 . 结晶水合物A是一种中药的主要成分,具有养血安神,平肝镇惊,解毒消肿的功效。某实验小组取9.6gA按如下流程进行相关实验。 0.1
0.1
 溶液时恰好反应;溶液E呈红色。
溶液时恰好反应;溶液E呈红色。
请回答下列问题:
(1)B的名称为_______ ,A的化学式为_______ 。
(2)请写出向溶液C中加入 溶液时发生的反应的离子方程式
溶液时发生的反应的离子方程式_______ 。
(3)已知 是拟卤素,性质与卤素相似。向E中滴加硫酸铜溶液,E中红色褪去并产生
是拟卤素,性质与卤素相似。向E中滴加硫酸铜溶液,E中红色褪去并产生 白色沉淀,请写出该过程的化学方程式:
白色沉淀,请写出该过程的化学方程式:_______ 。
(4)向E中通入 ,一段时间后也可观察到红色褪去。甲同学认为是
,一段时间后也可观察到红色褪去。甲同学认为是 被氧化,乙同学认为是
被氧化,乙同学认为是 被氧化。请设计能说明上述两种假设是否正确的实验流程及对应的现象与结论:
被氧化。请设计能说明上述两种假设是否正确的实验流程及对应的现象与结论:_______ 。

 0.1
0.1
 溶液时恰好反应;溶液E呈红色。
溶液时恰好反应;溶液E呈红色。请回答下列问题:
(1)B的名称为
(2)请写出向溶液C中加入
 溶液时发生的反应的离子方程式
溶液时发生的反应的离子方程式(3)已知
 是拟卤素,性质与卤素相似。向E中滴加硫酸铜溶液,E中红色褪去并产生
是拟卤素,性质与卤素相似。向E中滴加硫酸铜溶液,E中红色褪去并产生 白色沉淀,请写出该过程的化学方程式:
白色沉淀,请写出该过程的化学方程式:(4)向E中通入
 ,一段时间后也可观察到红色褪去。甲同学认为是
,一段时间后也可观察到红色褪去。甲同学认为是 被氧化,乙同学认为是
被氧化,乙同学认为是 被氧化。请设计能说明上述两种假设是否正确的实验流程及对应的现象与结论:
被氧化。请设计能说明上述两种假设是否正确的实验流程及对应的现象与结论:
您最近一年使用:0次
名校
解题方法
3 . 某化学兴趣小组利用图1装置(加热和夹持装置已省略)制备氨气并进行喷泉实验.
i.氨气的制备:打开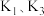 ,关闭
,关闭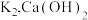 和
和 固体在甲处试管内反应生成
固体在甲处试管内反应生成 .
.
ⅱ.氨气的喷泉实验:当丁中溶液变蓝后,停止制备 ,关闭
,关闭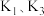 ,打开
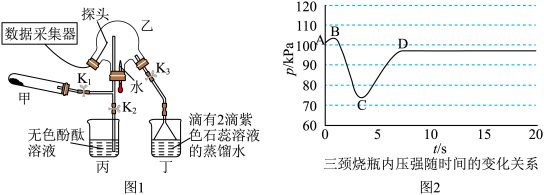
,打开 ,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.
,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.
请回答下列问题:___________________ ;丁处倒置漏斗的作用是______________ ;氨水中含有的分子有 、
、______________ .
(2)C→D过程中,三颈烧瓶中的现象为_____________ ; 能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为
能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为_____________ .
(3)该兴趣小组利用如图3所示装置进行另外一种喷泉实验.__________________________ .
②烧杯中发生反应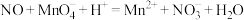 (未配平),该反应的氧化剂为
(未配平),该反应的氧化剂为__________ (填化学式),氧化产物和还原产物的物质的量之比为__________ (填最简整数比).
i.氨气的制备:打开
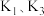 ,关闭
,关闭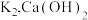 和
和 固体在甲处试管内反应生成
固体在甲处试管内反应生成 .
.ⅱ.氨气的喷泉实验:当丁中溶液变蓝后,停止制备
 ,关闭
,关闭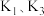 ,打开
,打开 ,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.
,挤压胶头滴管,三颈烧瓶内气体压强随时间的变化关系如图2所示.请回答下列问题:
 、
、(2)C→D过程中,三颈烧瓶中的现象为
 能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为
能灼伤皮肤、眼睛、呼吸器官的黏膜等,若实验室用稀硫酸吸收氨气,则反应的离子方程式为(3)该兴趣小组利用如图3所示装置进行另外一种喷泉实验.
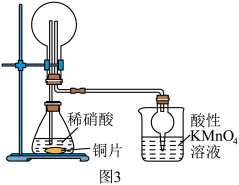
②烧杯中发生反应
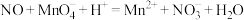 (未配平),该反应的氧化剂为
(未配平),该反应的氧化剂为
您最近一年使用:0次
2024-06-06更新
|
110次组卷
|
3卷引用:甘肃省白银市2023-2024学年高一下学期期中考试化学试题
名校
4 . 氮化镁( )是一种易水解的浅黄色粉末,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物和特殊的陶瓷材料。某化学研究小组拟于实验室利用
)是一种易水解的浅黄色粉末,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物和特殊的陶瓷材料。某化学研究小组拟于实验室利用 与
与 的反应制备氮化镁,并设计了如下装置。
的反应制备氮化镁,并设计了如下装置。
(1)仪器a的名称为_______ 。
(2) 可通过饱和
可通过饱和 溶液与固体
溶液与固体 共热制得,则A处应选用装置
共热制得,则A处应选用装置_______ (填“①”或“②”或“③”),该反应的化学方程式为_______ 。_______ 。
(4)下列说法正确的是_______。
(5)取18g镁粉进行实验,将反应后的固体产物与水充分反应,经过滤、洗涤、干燥得到38.4g固体,则镁粉与氮气反应时 的转化率为
的转化率为_______ 。
 )是一种易水解的浅黄色粉末,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物和特殊的陶瓷材料。某化学研究小组拟于实验室利用
)是一种易水解的浅黄色粉末,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物和特殊的陶瓷材料。某化学研究小组拟于实验室利用 与
与 的反应制备氮化镁,并设计了如下装置。
的反应制备氮化镁,并设计了如下装置。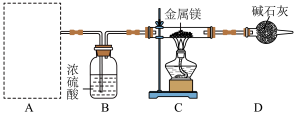
(1)仪器a的名称为
(2)
 可通过饱和
可通过饱和 溶液与固体
溶液与固体 共热制得,则A处应选用装置
共热制得,则A处应选用装置
(4)下列说法正确的是_______。
| A.导管b的作用为平衡气压,使液体顺利滴下 |
| B.实验时应先点燃C处酒精灯预热后,再开始装置A的反应 |
C.装置D中碱石灰可以换成无水 |
D.可用稀盐酸检验反应后的固体产物中是否存在尚未反应完的 |
(5)取18g镁粉进行实验,将反应后的固体产物与水充分反应,经过滤、洗涤、干燥得到38.4g固体,则镁粉与氮气反应时
 的转化率为
的转化率为
您最近一年使用:0次
名校
5 . 研究表明,我国酸雨区域占国土面积的40%以上,我国农业每年因遭受酸雨而造成经济损失高达15亿多元,酸雨的防治迫在眉睫。
(1) 是形成酸雨的主要物质之一,模仿示例图“
是形成酸雨的主要物质之一,模仿示例图“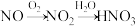 ”,画出由
”,画出由 形成硫酸型酸雨的可能的过程
形成硫酸型酸雨的可能的过程___________ 。
(2)某地降雨经检验,除 和
和 外,还含有
外,还含有 、
、 、
、 、
、 它们的浓度如下:
它们的浓度如下:
则该降雨的pH为___________ ,该降雨___________ (选填“是”或“不是”)酸雨。
(3)常温下,下列三种溶液:
①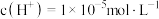 ②
②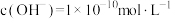 ③
③
按溶液酸性由强到弱的顺序排列为___________ 。
(4)为了减少酸雨产生的途径,你认为可采取的措施为___________。
(1)
 是形成酸雨的主要物质之一,模仿示例图“
是形成酸雨的主要物质之一,模仿示例图“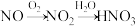 ”,画出由
”,画出由 形成硫酸型酸雨的可能的过程
形成硫酸型酸雨的可能的过程(2)某地降雨经检验,除
 和
和 外,还含有
外,还含有 、
、 、
、 、
、 它们的浓度如下:
它们的浓度如下:| 微粒 |  |  |  |  |  |  |
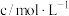 | ? |  |  |  | 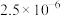 | 很小,可忽略 |
(3)常温下,下列三种溶液:
①
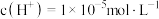 ②
②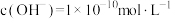 ③
③
按溶液酸性由强到弱的顺序排列为
(4)为了减少酸雨产生的途径,你认为可采取的措施为___________。
| A.把工厂烟囱造高 | B.在汽车排气管上安装汽车尾气催化转化器 |
| C.化石燃料脱硫 | D.在已酸化的土壤中加石灰 |
您最近一年使用:0次
名校
解题方法
6 . 硫化细菌是好氧菌,而反硫化细菌是厌氧菌,两类细菌参与了土壤中硫循环。___________ 剂(填“氧化”或“还原”)。
(2)“硫化细菌浸矿法”可将矿石中的CuS转化为可溶性铜盐,离子方程式是___________ 。
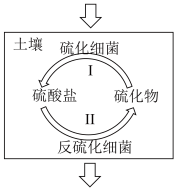
(2)“硫化细菌浸矿法”可将矿石中的CuS转化为可溶性铜盐,离子方程式是
您最近一年使用:0次
名校
7 . 对反应机理的研究有助于对反应的理解。X同学对水溶液中 歧化反应进行了探究,进行了如下实验:分别将9mL
歧化反应进行了探究,进行了如下实验:分别将9mL  饱和溶液加入2mL下列试剂中,密闭放置观察现象。
饱和溶液加入2mL下列试剂中,密闭放置观察现象。
已知:A、B实验结束后,KI溶液的浓度不变。
(1)由以上实验可知,KI可以作为水溶液中 歧化反应的
歧化反应的______ ,可能的反应过程如下。将ⅰ补充完整:
反应ⅰ.______ 。
反应ⅱ.
(2)①B是A的对比实验,则
______ 。
②比较A、B、C,可得出的结论是______ 。
(3)该同学还做了补充实验D:将9mL 饱和溶液加入2mL 0.2
饱和溶液加入2mL 0.2 KI和0.0002mol
KI和0.0002mol  的混合溶液中。现象为:溶液由棕褐色很快褪色,变为黄色,出现浑浊较A快。实验表明,
的混合溶液中。现象为:溶液由棕褐色很快褪色,变为黄色,出现浑浊较A快。实验表明, 的歧化反应速率D>A。原因是ⅰ的反应速率
的歧化反应速率D>A。原因是ⅰ的反应速率______ (选填“<”或“>”)ⅱ反应的速率,且ⅱ反应的发生有利于提高ⅰ反应的反应速率,因为______ 。
 歧化反应进行了探究,进行了如下实验:分别将9mL
歧化反应进行了探究,进行了如下实验:分别将9mL  饱和溶液加入2mL下列试剂中,密闭放置观察现象。
饱和溶液加入2mL下列试剂中,密闭放置观察现象。序号 | A | B | C |
试剂组成 | 0.4 | a 0.2 | 0.2 |
实验现象 | 溶液变黄,一段时间后出现浑浊 | 溶液变黄,出现浑浊较A快 | 无明显现象 |
(1)由以上实验可知,KI可以作为水溶液中
 歧化反应的
歧化反应的反应ⅰ.
反应ⅱ.

(2)①B是A的对比实验,则

②比较A、B、C,可得出的结论是
(3)该同学还做了补充实验D:将9mL
 饱和溶液加入2mL 0.2
饱和溶液加入2mL 0.2 KI和0.0002mol
KI和0.0002mol  的混合溶液中。现象为:溶液由棕褐色很快褪色,变为黄色,出现浑浊较A快。实验表明,
的混合溶液中。现象为:溶液由棕褐色很快褪色,变为黄色,出现浑浊较A快。实验表明, 的歧化反应速率D>A。原因是ⅰ的反应速率
的歧化反应速率D>A。原因是ⅰ的反应速率
您最近一年使用:0次
名校
8 .  是一种具有臭鸡蛋气味的有毒气体,用硫酸铁溶液可脱除空气中的
是一种具有臭鸡蛋气味的有毒气体,用硫酸铁溶液可脱除空气中的 并实现自身再生,原理如图所示,下列说法错误的是
并实现自身再生,原理如图所示,下列说法错误的是
 是一种具有臭鸡蛋气味的有毒气体,用硫酸铁溶液可脱除空气中的
是一种具有臭鸡蛋气味的有毒气体,用硫酸铁溶液可脱除空气中的 并实现自身再生,原理如图所示,下列说法错误的是
并实现自身再生,原理如图所示,下列说法错误的是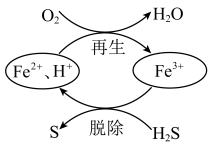
| A.图中的“脱除”“再生”两个过程均为氧化还原反应 |
| B.“脱除”过程中,可观察到溶液中产生黄色浑浊 |
C.脱除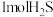 ,至少需要 ,至少需要 (标准状况)氧气 (标准状况)氧气 |
D.“再生”过程中,氧化剂和还原剂的物质的量之比为 |
您最近一年使用:0次
9 . 某化工厂制取硝酸铜有以下两种途径:
A.铜与稀硝酸反应,反应的化学方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
B.铜与浓硝酸反应,反应的化学方程式:Cu+4HNO3(浓)=Cu(NO3)2+2X↑+2H2O
(1)试确定X的化学式_______ ,硝酸铜中氮元素化合价为_______ 。
(2)对比A、B两个反应可得到的结论是_______ 。
(3)一氧化氮,二氧化氮是大气污染物,在生产中要尽可能减少排放,判断:若要制得等质量的硝酸铜,以上的_______ 途径较好?说明理由_______ ,_______ 。(两条)
(4)根据所学知识,设计制取硝酸铜的最佳途径(用化学方程式表示)。______________ 。
A.铜与稀硝酸反应,反应的化学方程式:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
B.铜与浓硝酸反应,反应的化学方程式:Cu+4HNO3(浓)=Cu(NO3)2+2X↑+2H2O
(1)试确定X的化学式
(2)对比A、B两个反应可得到的结论是
(3)一氧化氮,二氧化氮是大气污染物,在生产中要尽可能减少排放,判断:若要制得等质量的硝酸铜,以上的
(4)根据所学知识,设计制取硝酸铜的最佳途径(用化学方程式表示)。
您最近一年使用:0次
解题方法
10 . 探究是创新的源泉,某化学兴趣小组进行了制备氯气并探究卤素性质的实验。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是_______ (填字母代号),该反应体现了浓盐酸的酸性和_______ (填“氧化性”或“还原性”)。
①甲中反应的离子方程式为_______ ,向反应后的橙黄色溶液中滴加 KI-淀粉溶液,溶液变为蓝色,通过上述实验_______ (填“能”或“不能”)得出氧化性:Cl2>Br2>I2。
②乙装置中 NaOH 溶液的作用为_______ ,其主要反应的化学方程式为_______ 。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是
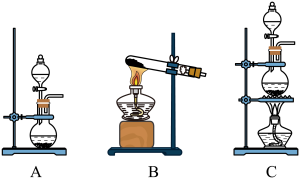
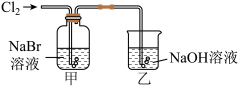
①甲中反应的离子方程式为
②乙装置中 NaOH 溶液的作用为
您最近一年使用:0次




