名校
解题方法
1 .  通入
通入 的水溶液中发生氧化还原反应,生成硫酸和不溶于水的
的水溶液中发生氧化还原反应,生成硫酸和不溶于水的 能与浓硫酸反应生成
能与浓硫酸反应生成 和
和 ,则浓硫酸、
,则浓硫酸、 和
和 三者中,氧化性最弱的为
三者中,氧化性最弱的为___________ 。
A. B.
B. C.浓硫酸
C.浓硫酸
 通入
通入 的水溶液中发生氧化还原反应,生成硫酸和不溶于水的
的水溶液中发生氧化还原反应,生成硫酸和不溶于水的 能与浓硫酸反应生成
能与浓硫酸反应生成 和
和 ,则浓硫酸、
,则浓硫酸、 和
和 三者中,氧化性最弱的为
三者中,氧化性最弱的为A.
 B.
B. C.浓硫酸
C.浓硫酸
您最近一年使用:0次
名校
解题方法
2 . 某研究小组利用 的还原性提纯
的还原性提纯 并制取
并制取 的方案如下:
的方案如下:
 的还原性提纯
的还原性提纯 并制取
并制取 的方案如下:
的方案如下:
A.“沉淀”步骤中不可使用 溶液代替硫酸 溶液代替硫酸 |
B.滤渣中只有 |
C.“转化”步骤中发生反应的离子方程式为 |
D.将转化后的溶液蒸发浓缩、降温结晶得到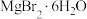 晶体 晶体 |
您最近一年使用:0次
解题方法
3 . 我国在新能源汽车领域世界领先,新能源汽车动力电池的制备和回收利用技术至关重要。回答下列问题:
I.磷酸铁锂电池放电时电池反应为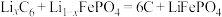 。
。
(1)磷酸铁锂电池正极的电极反应式为_____ 。
(2)将 、磷酸铁与足量炭黑混合高温灼烧可制备
、磷酸铁与足量炭黑混合高温灼烧可制备 ,同时生成一种有毒的气体。写出该反应的化学方程式:
,同时生成一种有毒的气体。写出该反应的化学方程式:_____ 。
Ⅱ.回收含的废旧电池制备 的流程如图所示(已知
的流程如图所示(已知 加热时可溶于盐酸):
加热时可溶于盐酸):_____ ,若要提高 的浸出速率和浸出率,可采取的措施是
的浸出速率和浸出率,可采取的措施是_____ (任写两点)。
(4)写出 与
与 在盐酸中发生反应的离子方程式:
在盐酸中发生反应的离子方程式:_____ 。
(5)欲证明 已沉淀完全,应采用的实验操作是
已沉淀完全,应采用的实验操作是_____ 。
(6)“操作a”所需玻璃仪器有_____ 。
I.磷酸铁锂电池放电时电池反应为
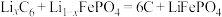 。
。(1)磷酸铁锂电池正极的电极反应式为
(2)将
 、磷酸铁与足量炭黑混合高温灼烧可制备
、磷酸铁与足量炭黑混合高温灼烧可制备 ,同时生成一种有毒的气体。写出该反应的化学方程式:
,同时生成一种有毒的气体。写出该反应的化学方程式:Ⅱ.回收含的废旧电池制备
 的流程如图所示(已知
的流程如图所示(已知 加热时可溶于盐酸):
加热时可溶于盐酸):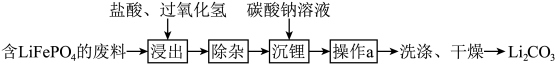
 的浸出速率和浸出率,可采取的措施是
的浸出速率和浸出率,可采取的措施是(4)写出
 与
与 在盐酸中发生反应的离子方程式:
在盐酸中发生反应的离子方程式:(5)欲证明
 已沉淀完全,应采用的实验操作是
已沉淀完全,应采用的实验操作是(6)“操作a”所需玻璃仪器有
您最近一年使用:0次
4 . 农谚说雷雨发庄稼,其中氮元素的转化过程如下:
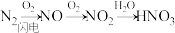
回答下列问题:
(1)常温下,NO是_______ (填“无色”或“红棕色”)气体。
(2) 的水溶液具有
的水溶液具有_______ (填“碱”或“酸”)性。
(3)稀硝酸可与铜反应,配平其化学方程式:
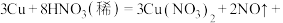
_______ 
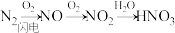
回答下列问题:
(1)常温下,NO是
(2)
 的水溶液具有
的水溶液具有(3)稀硝酸可与铜反应,配平其化学方程式:
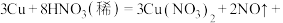

您最近一年使用:0次
解题方法
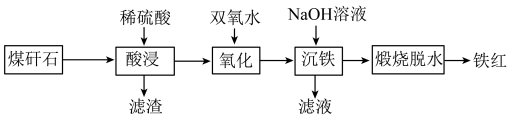
5 . 由煤矸石(主要成分为SiO2及铁铝的氧化物,还含有少量CaO)制备铁红的工艺流程如图。___________ (任写两条)。
(2)滤渣的主要成分是___________ 。
(3)“氧化”过程中发生反应的离子方程式为___________ 。
(4)“沉铁”过程中加入过量NaOH溶液,发生反应的离子方程式为Fe3++3OH-=Fe(OH)3↓和___________ 。
(5)关于“煅烧脱水”制得的铁红,下列说法正确的是___________。
(2)滤渣的主要成分是
(3)“氧化”过程中发生反应的离子方程式为
(4)“沉铁”过程中加入过量NaOH溶液,发生反应的离子方程式为Fe3++3OH-=Fe(OH)3↓和
(5)关于“煅烧脱水”制得的铁红,下列说法正确的是___________。
A.铁红的化学式为 | B.铁红是具有磁性的晶体 |
| C.铁红属于碱性氧化物 | D.铁红常用作油漆、涂料的红色颜料 |
您最近一年使用:0次
6 . 一定实验条件下, 能将
能将 氧化成
氧化成 。下列物质中,能替代
。下列物质中,能替代 进行此实验的是
进行此实验的是
 能将
能将 氧化成
氧化成 。下列物质中,能替代
。下列物质中,能替代 进行此实验的是
进行此实验的是A. | B. | C. | D. |
您最近一年使用:0次
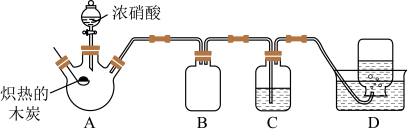
7 . 某化学小组采用如图所示装置对浓硝酸与木炭的反应进行探究(已知:
 )。
)。
(1)实验开始前,首先进行的操作是____________ 。
(2)装有浓硝酸的仪器的名称为____________ 。
(3)写出炽热的木炭与浓硝酸反应的化学方程式:________________ 。
(4)装置B的作用是________________ 。
(5)装置D中集气瓶收集到了无色气体,部分同学认为该气体是NO,还有部分同学认为是 。写出一种检验该气体的方法:
。写出一种检验该气体的方法:__________________ 。
(6)在催化剂作用下加热, 可用于处理
可用于处理 ,所得产物为
,所得产物为 和
和 ,则
,则 与
与 反应时,反应中的氧化剂是
反应时,反应中的氧化剂是___________ ,还原产物和氧化产物的质量之比为___________ 。每生成1.96g  ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为___________ 。如果用氨来处理NO,有关反应的化学方程式为_____________ 。

 )。
)。
(1)实验开始前,首先进行的操作是
(2)装有浓硝酸的仪器的名称为
(3)写出炽热的木炭与浓硝酸反应的化学方程式:
(4)装置B的作用是
(5)装置D中集气瓶收集到了无色气体,部分同学认为该气体是NO,还有部分同学认为是
 。写出一种检验该气体的方法:
。写出一种检验该气体的方法:(6)在催化剂作用下加热,
 可用于处理
可用于处理 ,所得产物为
,所得产物为 和
和 ,则
,则 与
与 反应时,反应中的氧化剂是
反应时,反应中的氧化剂是 ,反应中转移电子的物质的量为
,反应中转移电子的物质的量为
您最近一年使用:0次
8 . 重晶石( )与焦炭在一定条件下发生反应:
)与焦炭在一定条件下发生反应: 。下列说法不正确的是
。下列说法不正确的是
 )与焦炭在一定条件下发生反应:
)与焦炭在一定条件下发生反应: 。下列说法不正确的是
。下列说法不正确的是A. 发生还原反应 发生还原反应 |
| B.C把电子转移给了CO |
C.还原剂为C,氧化剂为 |
| D.C的还原性比BaS的还原性强 |
您最近一年使用:0次
解题方法
9 . 多功能净水剂高铁酸钠( )主要用于饮用水处理,
)主要用于饮用水处理, 进入水中能杀灭水中细菌,同时会生成
进入水中能杀灭水中细菌,同时会生成 胶体,
胶体, 胶体通过吸附水中悬浮物达到净水的功能。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可表示为:
胶体通过吸附水中悬浮物达到净水的功能。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可表示为:
 。回答下列问题:
。回答下列问题:
(1) 中Fe元素的化合价
中Fe元素的化合价___________
(2)由上述化学原理可知 的氧化性比NaClO的氧化性
的氧化性比NaClO的氧化性___________ (填“强”或“弱”);
(3)将上述化学反应方程式改写为离子反应方程式___________ ;
(4) 沉淀没有净水作用,而
沉淀没有净水作用,而 胶体则可以净水,形成这样差异的本质原因是
胶体则可以净水,形成这样差异的本质原因是___________ ;
(5) 具有杀菌消毒是利用其
具有杀菌消毒是利用其___________ 的性质;
(6)请用单线桥法标出上述反应的电子转移方向和数目___________ ;
(7)制备8.3g 需要消耗
需要消耗___________ gNaOH。
 )主要用于饮用水处理,
)主要用于饮用水处理, 进入水中能杀灭水中细菌,同时会生成
进入水中能杀灭水中细菌,同时会生成 胶体,
胶体, 胶体通过吸附水中悬浮物达到净水的功能。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可表示为:
胶体通过吸附水中悬浮物达到净水的功能。工业上制备高铁酸钠有多种方法,其中一种方法的化学原理可表示为:
 。回答下列问题:
。回答下列问题:(1)
 中Fe元素的化合价
中Fe元素的化合价(2)由上述化学原理可知
 的氧化性比NaClO的氧化性
的氧化性比NaClO的氧化性(3)将上述化学反应方程式改写为离子反应方程式
(4)
 沉淀没有净水作用,而
沉淀没有净水作用,而 胶体则可以净水,形成这样差异的本质原因是
胶体则可以净水,形成这样差异的本质原因是(5)
 具有杀菌消毒是利用其
具有杀菌消毒是利用其(6)请用单线桥法标出上述反应的电子转移方向和数目
(7)制备8.3g
 需要消耗
需要消耗
您最近一年使用:0次
名校
10 .  是一种重要的化工原料,可用于制化肥、农药,炸药、染料等.工业制硝酸的流程如图所示.下列说法错误的是
是一种重要的化工原料,可用于制化肥、农药,炸药、染料等.工业制硝酸的流程如图所示.下列说法错误的是
 是一种重要的化工原料,可用于制化肥、农药,炸药、染料等.工业制硝酸的流程如图所示.下列说法错误的是
是一种重要的化工原料,可用于制化肥、农药,炸药、染料等.工业制硝酸的流程如图所示.下列说法错误的是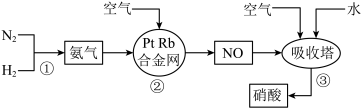
| A.反应①②③均属于氧化还原反应 |
B.若有 完全转化为 完全转化为 ,理论上共需要消耗 ,理论上共需要消耗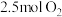 |
C.吸收塔内反应的化学方程式为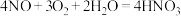 |
D.浓硝酸在光照下会逐渐变黄,原因是浓硝酸光照时分解生成了 |
您最近一年使用:0次
2024-06-07更新
|
146次组卷
|
2卷引用:甘肃省白银市2023-2024学年高一下学期期中考试化学试题



