解题方法
1 . 根据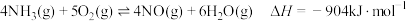 ,下列说法
,下列说法不正确 的是
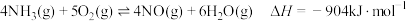 ,下列说法
,下列说法A.反应的 |
B.有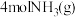 和 和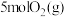 在反应器中充分反应,能放出 在反应器中充分反应,能放出 热量 热量 |
C.断裂1mol 键的同时,断裂 键的同时,断裂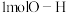 键,说明该反应达到平衡状态 键,说明该反应达到平衡状态 |
D.每消耗 转移电子的数目约为 转移电子的数目约为 |
您最近一年使用:0次
解题方法
2 . 在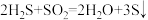 中,氧化剂与还原剂的物质的量之比为
中,氧化剂与还原剂的物质的量之比为
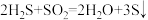 中,氧化剂与还原剂的物质的量之比为
中,氧化剂与还原剂的物质的量之比为| A.2∶1 | B.1∶2 | C.1∶1 | D.16∶17 |
您最近一年使用:0次
解题方法
3 . 用盐酸洗钢材会产生“酸洗废液”(主要成分为FeCl2)。工业上用“酸洗废液”经高温氧化制取高纯氧化铁,同时产生的氯化氢气体可回收使用,发生的反应为aFeCl2 +bO2 + cH2O dFe2O3+8HCl(未配平)。下列说法正确的是
dFe2O3+8HCl(未配平)。下列说法正确的是
 dFe2O3+8HCl(未配平)。下列说法正确的是
dFe2O3+8HCl(未配平)。下列说法正确的是| A.a+b+d=7 |
| B.该反应中,每消耗3.2gO2,同时生成32 g Fe2O3 |
| C.该反应中,HCl既是氧化产物也是还原产物 |
| D.将生成的气体通入碳酸氢钙溶液中,会有碳酸钙沉淀生成 |
您最近一年使用:0次
4 . 复印机工作时易产生臭氧,臭氧具有强氧化性,可使润湿的淀粉-KI试纸变蓝。反应为O3+2KI+H2O=2KOH+I2+O2,关于此反应的说法正确的是
| A.每生成1molO2,转移电子数的物质的量为4mol |
| B.O3是氧化剂,H2O与KI是还原剂 |
| C.氧化性强弱顺序:O3>I2 |
| D.氧化产物与还原产物的个数之比是1:2 |
您最近一年使用:0次
解题方法
5 . 钠元素广泛存在于自然界,下列关于钠及其化合物的叙述正确的是
| A.金属钠着火时,可用泡沫灭火器灭火 |
| B.等质量的钠与氧气反应分别生成氧化钠和过氧化钠,转移的电子后者更多 |
| C.Na2O2固体中阴阳离子个数比为1:2,可以作供氧剂 |
| D.进行焰色试验时如无铂丝和铁丝,可以用玻璃棒代替 |
您最近一年使用:0次
解题方法
6 . 氨是一种重要的化工原料,主要用于化肥工业,也广泛用于硝酸、纯碱、制药等工业;合成氨反应N2(g)+3H2(g) 2NH3(g) ΔH=-92.4 kJ/mol。下列有关合成氨反应的说法正确的是
2NH3(g) ΔH=-92.4 kJ/mol。下列有关合成氨反应的说法正确的是
 2NH3(g) ΔH=-92.4 kJ/mol。下列有关合成氨反应的说法正确的是
2NH3(g) ΔH=-92.4 kJ/mol。下列有关合成氨反应的说法正确的是| A.高温条件下该反应可以自发 |
| B.反应的ΔH=E(N-N)+3E(H-H)-6E(N-H) (E表示键能) |
| C.反应中每消耗1 mol H2转移电子的数目约等于2×6.02×1023 |
| D.该反应采用高温高压条件是为了增大H2的平衡转化率 |
您最近一年使用:0次
7 . 将宏观物质、微观粒子和化学符号建立联系是化学学科特有的研究方式。生产水煤气的微观过程如图所示,下列说法错误的是


A. 能被氢氧化钠溶液吸收 能被氢氧化钠溶液吸收 | B. 是该反应的还原剂 是该反应的还原剂 |
C.生成1个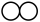 的同时会转移2个电子 的同时会转移2个电子 | D.该反应属于置换反应 |
您最近一年使用:0次
名校
8 . 高铁酸钾是一种新型水处理剂,使用说明书如下。
回答下列问题:
(1) 中铁元素的化合价为
中铁元素的化合价为___________ 。
(2)制备 需要在
需要在___________ (填“酸性”“碱性”或“中性”)环境中进行。
(3)下列关于 的说法中,错误的是
的说法中,错误的是___________ (填字母)。
a.是具有强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4) 与水反应生成
与水反应生成 胶体、
胶体、 和
和 反应的化学方程式为
反应的化学方程式为___________ ;该反应消耗 转移的电子数为
转移的电子数为___________  (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(5)消毒净化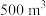 水,至少需要
水,至少需要 的质量为
的质量为___________  。
。
(6)产生 胶体时,该分散系区别于其他分散系的本质特征是
胶体时,该分散系区别于其他分散系的本质特征是___________ 。
| 高铁酸钾使用说明书 【化学式】  【性状】暗紫色具有金属光泽的粉末,无臭无味 【产品特点】干燥品在室温下稳定,在强碱溶液中稳定,随着  减小,稳定性下降。 减小,稳定性下降。 能与水反应放出氧气并通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 能与水反应放出氧气并通过强烈的氧化作用可迅速杀灭细菌,有消毒作用,同时不会产生有害物质。 与水反应还能产生具有强吸附性的 与水反应还能产生具有强吸附性的 胶体,可除去水中细微的悬浮物,有净水作用。 胶体,可除去水中细微的悬浮物,有净水作用。【用途】主要用于饮用水消毒净化、城市生活污水和工业污水处理 【用量】消毒净化1L水投放 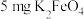 即可达到卫生标准 即可达到卫生标准 |
(1)
 中铁元素的化合价为
中铁元素的化合价为(2)制备
 需要在
需要在(3)下列关于
 的说法中,错误的是
的说法中,错误的是a.是具有强氧化性的盐 b.固体保存需要防潮
c.其消毒和净化水的原理相同 d.其净水优点有:作用快、安全性好、无异味
(4)
 与水反应生成
与水反应生成 胶体、
胶体、 和
和 反应的化学方程式为
反应的化学方程式为 转移的电子数为
转移的电子数为 (
( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。(5)消毒净化
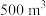 水,至少需要
水,至少需要 的质量为
的质量为 。
。(6)产生
 胶体时,该分散系区别于其他分散系的本质特征是
胶体时,该分散系区别于其他分散系的本质特征是
您最近一年使用:0次
解题方法
9 . 红热的铁粉与水蒸气发生的反应为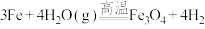 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
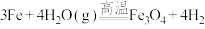 ,设
,设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.通常状况下,1.8g水分子中,所含的电子总数为 |
B.该反应中,每消耗1.68gFe,同时转移的电子数为 |
C.标准状况下,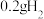 分子中,所含的质子数为 分子中,所含的质子数为 |
D.等物质的量的 和 和 中,所含的氢原子总数均为: 中,所含的氢原子总数均为: |
您最近一年使用:0次
10 . 氧化还原反应在工农业生产、日常生活中具有广泛用途,贯穿古今。
(1)工业盐的主要成分是 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有_______ (填“氧化”或“还原”,下同)。工业盐中毒后,可服用维生素C来缓解中毒状况,这说明维生素C具有________ 性。
(2) 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下: 。
。
①配平上述氧化还原反应方程式___________ 。
②该反应中,氧化剂是___________ (填化学式),被氧化的元素是___________ (填元素名称)。
(3)二氧化氯是一种高效消毒剂。工业上制备 的反应为:
的反应为: 。
。
①该反应中的还原产物是___________ (写化学式),反应中每生成1mol 分子,被氧化的HCl的物质的量为
分子,被氧化的HCl的物质的量为___________ ,转移电子的数目为___________ 。
②用“单线桥”标出反应中电子转移的方向与数目___________ 。
③ 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),要将其转化为
),要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是___________ (填字母)。
a. b.
b. c.
c. d.
d.
(4)双氯水是公认的绿色氧化剂。已知氯化性强弱顺序为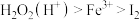 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为___________ 。
(1)工业盐的主要成分是
 ,以前有许多起因误食
,以前有许多起因误食 而中毒的事件,其原因是
而中毒的事件,其原因是 把人体内的
把人体内的 转化为
转化为 而失去与
而失去与 结合的能力,这说明
结合的能力,这说明 具有
具有(2)
 常用于焊接,在焊接铜器时可用
常用于焊接,在焊接铜器时可用 除去铜器表面的氧化铜,便于焊接,其反应如下:
除去铜器表面的氧化铜,便于焊接,其反应如下: 。
。①配平上述氧化还原反应方程式
②该反应中,氧化剂是
(3)二氧化氯是一种高效消毒剂。工业上制备
 的反应为:
的反应为: 。
。①该反应中的还原产物是
 分子,被氧化的HCl的物质的量为
分子,被氧化的HCl的物质的量为②用“单线桥”标出反应中电子转移的方向与数目
③
 在杀菌消毒的过程中会生成副产物亚氯酸盐(
在杀菌消毒的过程中会生成副产物亚氯酸盐( ),要将其转化为
),要将其转化为 除去,下列试剂能实现其转化过程的是
除去,下列试剂能实现其转化过程的是a.
 b.
b. c.
c. d.
d.
(4)双氯水是公认的绿色氧化剂。已知氯化性强弱顺序为
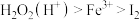 ,向
,向 溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
溶液中加入足量硫酸酸化的双氧水,发生反应的离子方程式为
您最近一年使用:0次



