2013·山东滨州·一模
解题方法
1 . (1)某学习小组利用下图装置制取氯气并探究其性质。
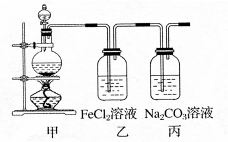
①甲装置中反应的化学方程式是_____________________________________ ;
②证明乙装置中FeCl2溶液与Cl2发生了反应的实验方法是(只注明试剂、现象)__________________________________________________________ ;
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中反应的化学方程式是____________________________________ 。
(2)有一瓶长期放置的漂白粉,请利用以下仪器和试剂,完成该漂白粉成份的探究。
试管、胶头滴管、带导管的单孔塞、蒸馏水、1mol·L-1盐酸、品红溶液、新制澄清石灰水。
【提出假设】假设一:该漂白粉未变质,含CaCl2、Ca(ClO)2;
假设二:该漂白粉全部变质,含________________ ;
假设三:该漂白粉部分变质,含CaCl2、Ca(ClO)2、CaCO3 。
【进行实验】在答题卡上完成下表(不必检验Ca2+、Cl-):

①甲装置中反应的化学方程式是
②证明乙装置中FeCl2溶液与Cl2发生了反应的实验方法是(只注明试剂、现象)
③丙装置中通入少量Cl2,可制得某种生活中常用的漂白、消毒的物质。已知碳酸的酸性强于次氯酸,则丙中反应的化学方程式是
(2)有一瓶长期放置的漂白粉,请利用以下仪器和试剂,完成该漂白粉成份的探究。
试管、胶头滴管、带导管的单孔塞、蒸馏水、1mol·L-1盐酸、品红溶液、新制澄清石灰水。
【提出假设】假设一:该漂白粉未变质,含CaCl2、Ca(ClO)2;
假设二:该漂白粉全部变质,含
假设三:该漂白粉部分变质,含CaCl2、Ca(ClO)2、CaCO3 。
【进行实验】在答题卡上完成下表(不必检验Ca2+、Cl-):
| 实验步骤 | 预期现象和结论 | |
| ① | 用A试管取少量澄清石灰水备用,用B试管取少量样品,再向B试管 | 若无气体放出且澄清石灰水未见浑浊,则假设一成立; |
| ② | ||
您最近一年使用:0次
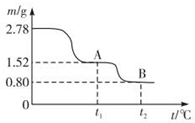
2 . 在中国古代,炼丹家以绿矾(FeSO4•7H2O为原料,放在炼丹炉中煅烧可制得绿矾油.绿矾油是一种无色粘稠液体,可用于除掉兵器上的铁锈.如图是2.78g绿矾隔绝空气受热分解时,所得固体产物的质量随温度变化的曲线.将加热产生的所有气体通入足量的BaCl2溶液.得自色沉淀1.16g.
(1)绿矾油主要成份的化学式为_________ .t1~t2.发生反应的化学方程式为_________________ .
(2)若将2.88g草酸亚铁(FeC2O4)隔绝空气加热至100℃,得到1.44g黑色细粉,则可推知该黑色细粉为_________ .
(3)以下是FeSO4•7H2O的实验室制备流理图.
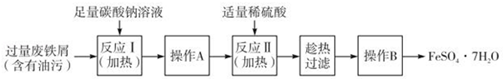
根据题意完成下列填空:
①反应II需要100mL1. 5mol•L﹣1的稀H2SO4溶解洁净的铁屑,用质量分数为98%、密度为1.84g•cm﹣3的浓H2SO4配制.所用的仪器有量筒、烧杯、玻璃捧、胶头滴管及____________ .
②操作A的名称为_____________ .
③测定FeSO4•7H2O产品中Fe2+含量的常用方法是KMnO4溶液滴定法.已知称取6.0g FeSO4•7H2O产品,配制成溶液,用硫酸酸化的0.2000mol•L﹣1KMnO4溶液滴定,消耗KMnO4溶液的体积为20.00mL.发生反应的离子方程式为_______________ ,计算上述样品中FeSO4•7H2O的质量分数为_________ (保留两位有效数字).
(1)绿矾油主要成份的化学式为
(2)若将2.88g草酸亚铁(FeC2O4)隔绝空气加热至100℃,得到1.44g黑色细粉,则可推知该黑色细粉为
(3)以下是FeSO4•7H2O的实验室制备流理图.

根据题意完成下列填空:

①反应II需要100mL1. 5mol•L﹣1的稀H2SO4溶解洁净的铁屑,用质量分数为98%、密度为1.84g•cm﹣3的浓H2SO4配制.所用的仪器有量筒、烧杯、玻璃捧、胶头滴管及
②操作A的名称为
③测定FeSO4•7H2O产品中Fe2+含量的常用方法是KMnO4溶液滴定法.已知称取6.0g FeSO4•7H2O产品,配制成溶液,用硫酸酸化的0.2000mol•L﹣1KMnO4溶液滴定,消耗KMnO4溶液的体积为20.00mL.发生反应的离子方程式为
您最近一年使用:0次
3 . 硫代硫酸钠(Na2S2O3)为白色结晶粉末,易溶于水,在中性或碱性条件下稳定,在酸性条件下发生反应(S2O32-+2H+=S↓+SO2+H2O),是一种重要的化工原料。请回答下列问题:
(1)Na2S2O3溶液可用作照相底片(AgBr)中的定影剂,其原理是将未感光的AgBr转化为可溶于水的稳定络合物Na3[Ag(S2O3)2]。写出该络合反应的离子方程式___ 。
(2)工业上利用硫化碱残渣(主要成分Na2S,Na2CO3)与硫黄废气(主要成分SO2)反应,经吸硫、蒸发、结晶,制得硫代硫酸钠。已知该反应中C(碳)原子化合价不变,则氧化剂和还原剂物质的量之比为___ 。
(3)Na2S2O3长期暴露在空气中易被氧化生成Na2SO4,设计实验方案检验Na2S2O3是否变质(已知BaS2O3微溶于水)___ 。
(4)现有含Na2S2O3·5H2O的样品,用以下方法计算Na2S2O3·5H2O的质量分数。
a.取样品7.0g溶于蒸馏水中,并定容至500mL容量瓶中待用。
b.取0.01mol.L-1的K2Cr2O7标准溶液20.00mL于锥形瓶中,加过量KI溶液并酸化,加2滴淀粉指示剂,用a中未知浓度的Na2S2O3待测液滴定至终点,共用去25.00mL。(已知2S2O32-+I2=S4O62-+2I-),在酸性环境中Cr2O72-被还原为绿色的Cr3+)。
回答下列问题:
①滴定终点的现象是___ 。
②样品中Na2S2O3·5H2O的质量分数为___ (保留2位有效数字)。
(1)Na2S2O3溶液可用作照相底片(AgBr)中的定影剂,其原理是将未感光的AgBr转化为可溶于水的稳定络合物Na3[Ag(S2O3)2]。写出该络合反应的离子方程式
(2)工业上利用硫化碱残渣(主要成分Na2S,Na2CO3)与硫黄废气(主要成分SO2)反应,经吸硫、蒸发、结晶,制得硫代硫酸钠。已知该反应中C(碳)原子化合价不变,则氧化剂和还原剂物质的量之比为
(3)Na2S2O3长期暴露在空气中易被氧化生成Na2SO4,设计实验方案检验Na2S2O3是否变质(已知BaS2O3微溶于水)
(4)现有含Na2S2O3·5H2O的样品,用以下方法计算Na2S2O3·5H2O的质量分数。
a.取样品7.0g溶于蒸馏水中,并定容至500mL容量瓶中待用。
b.取0.01mol.L-1的K2Cr2O7标准溶液20.00mL于锥形瓶中,加过量KI溶液并酸化,加2滴淀粉指示剂,用a中未知浓度的Na2S2O3待测液滴定至终点,共用去25.00mL。(已知2S2O32-+I2=S4O62-+2I-),在酸性环境中Cr2O72-被还原为绿色的Cr3+)。
回答下列问题:
①滴定终点的现象是
②样品中Na2S2O3·5H2O的质量分数为
您最近一年使用:0次
名校
4 . I.二氧化氯(C1O2)气体是一种常用的高效自来水消毒剂。
(1)KC1O3和浓盐酸在一定温度下反应会生成C1O2和C12,反应方程式为_____ 。
(2)C1O2和Cl2在消毒时自身均被还原为C1-,则常温常压下,等体积的ClO2的消毒能力是Cl2的_____ 倍。
(3)自来水厂用C1O2处理后的水中,要求C1O2的浓度在0.1~0.8mg·L-1之间,用碘量法可以检测水中CIO2的浓度(不同pH环境中粒子种类如图所示),步骤如下:

I.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝;
Ⅱ.加入一定量的Na2S2O3溶液:(已知: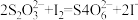 )
)
Ⅲ.加硫酸调节水样pH至1~3。
请回答:
①操作I中反应的离子方程式是_____ 。
②若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10-3mo·L-1的Na2S2O3溶液10mL,则水样中C1O2的浓度是_____ mg·L-1。
Ⅱ.
(4)过二硫酸(结构如图)是一种白色晶体,其酸及盐均为强氧化剂。
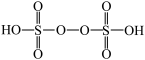
在Ag+及加热的条件下,S2O 可将溶液中的Mn2+氧化为MnO
可将溶液中的Mn2+氧化为MnO ,该反应的离子方程式为
,该反应的离子方程式为_____ 。
(5)连二亚硫酸钠(N2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为_____ 。
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为1:2时,产物为_____ (填化学式)。
(1)KC1O3和浓盐酸在一定温度下反应会生成C1O2和C12,反应方程式为
(2)C1O2和Cl2在消毒时自身均被还原为C1-,则常温常压下,等体积的ClO2的消毒能力是Cl2的
(3)自来水厂用C1O2处理后的水中,要求C1O2的浓度在0.1~0.8mg·L-1之间,用碘量法可以检测水中CIO2的浓度(不同pH环境中粒子种类如图所示),步骤如下:

I.取一定体积的水样,加入一定量的碘化钾,再将反应后溶液调至中性,并加入淀粉溶液,溶液变蓝;
Ⅱ.加入一定量的Na2S2O3溶液:(已知:
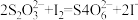 )
)Ⅲ.加硫酸调节水样pH至1~3。
请回答:
①操作I中反应的离子方程式是
②若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10-3mo·L-1的Na2S2O3溶液10mL,则水样中C1O2的浓度是
Ⅱ.
(4)过二硫酸(结构如图)是一种白色晶体,其酸及盐均为强氧化剂。

在Ag+及加热的条件下,S2O
 可将溶液中的Mn2+氧化为MnO
可将溶液中的Mn2+氧化为MnO ,该反应的离子方程式为
,该反应的离子方程式为(5)连二亚硫酸钠(N2S2O4)又称保险粉,是最适合木浆造纸的漂白剂,其水溶液性质不稳定,有极强的还原性。
①Na2S2O4中S元素的化合价为
②Na2S2O4暴露于空气中易吸收氧气和水蒸气而变质,发生反应时,当氧化剂和还原剂的物质的量之比为1:2时,产物为
您最近一年使用:0次
11-12高三上·上海松江·期中
5 . 将1.68克铁粉投入100mL稀硝酸中,两物质恰好完全反应,硝酸的还原产物全部是NO。向反应后的溶液中加入一定量的NaOH溶液,恰好使铁元素完全转化为沉淀,过滤,将滤渣洗涤、干燥、灼烧、称重,得固体a克,把滤液蒸干、灼烧、称重,得固体b克。根据题意完成下面小题:
(1)此硝酸的物质的量浓度范围是_____________________ ;
(2)a克固体的成份是_____________ ,质量为_______________ 克;
b克固体的成份是_____________ ,质量范围为_____________________ 克。
(3)假如反应中放出NO的体积(标况下)为582.4 mL,若向铁与硝酸反应后的溶液中继续加入铁屑,该溶液还能溶解的铁的质量为_____________ 。
(4)已知:25℃时NaOH的溶解度为118克/100克水。25℃时,把15克NaOH固体溶解在一定量水中,配成20克溶液,其密度为1.44g/mL。用该溶液去沉淀铁与硝酸反应后的溶液中的全部铁元素,至少需要取该NaOH溶液______ mL。
(1)此硝酸的物质的量浓度范围是
(2)a克固体的成份是
b克固体的成份是
(3)假如反应中放出NO的体积(标况下)为582.4 mL,若向铁与硝酸反应后的溶液中继续加入铁屑,该溶液还能溶解的铁的质量为
(4)已知:25℃时NaOH的溶解度为118克/100克水。25℃时,把15克NaOH固体溶解在一定量水中,配成20克溶液,其密度为1.44g/mL。用该溶液去沉淀铁与硝酸反应后的溶液中的全部铁元素,至少需要取该NaOH溶液
您最近一年使用:0次
19-20高一下·天津红桥·期末
解题方法
6 . 现有A、B、C三种物质,均含同一种元素,一定条件下其转化关系如图(部分产物已略去):

请回答:
(1)若A是黄绿色气体单质,C是漂白粉中的有效成分。
①组成A的元素在周期表中的位置是____ 。
②写出工业上用A与D反应制取漂白粉的化学反应方程式____ 。
③A与D的反应中转移1 mol电子时,消耗A的体积为____ (标准状况)。
(2)若A是可以使品红溶液褪色,加热后又恢复原色的气体,D是短周期中原子半径最大的主族元素形成的氢氧化物。
①下列关于A的说法不正确 的是____ (填字母)。
a.能使澄清石灰水变浑浊 b.使品红褪色与氯水漂白原理相同
c.只有还原性没有氧化性 d.是造成大气污染物之一
②C的溶液在空气中放置易变质,写出C溶液在空气中变质的化学方程式____ 。

请回答:
(1)若A是黄绿色气体单质,C是漂白粉中的有效成分。
①组成A的元素在周期表中的位置是
②写出工业上用A与D反应制取漂白粉的化学反应方程式
③A与D的反应中转移1 mol电子时,消耗A的体积为
(2)若A是可以使品红溶液褪色,加热后又恢复原色的气体,D是短周期中原子半径最大的主族元素形成的氢氧化物。
①下列关于A的说法
a.能使澄清石灰水变浑浊 b.使品红褪色与氯水漂白原理相同
c.只有还原性没有氧化性 d.是造成大气污染物之一
②C的溶液在空气中放置易变质,写出C溶液在空气中变质的化学方程式
您最近一年使用:0次
解题方法
7 . 三氯化铬( )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为:
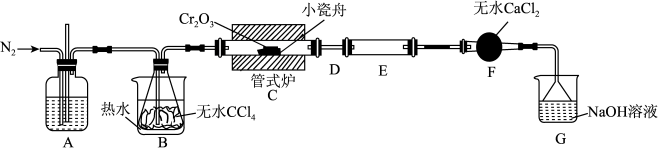
的反应为: ,其实验装置如下图所示:
,其实验装置如下图所示:
已知:① (俗称光气)有毒,遇水发生水解:
(俗称光气)有毒,遇水发生水解: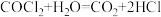 ;
;
②碱性条件下, 可将
可将 氧化为
氧化为 (黄色);酸性条件下,
(黄色);酸性条件下, 将
将 (橙色)还原为
(橙色)还原为 (绿色)。
(绿色)。
(1)A装置用于干燥 和观察其流速,A中的试剂是
和观察其流速,A中的试剂是_______ ;无水 的作用是
的作用是_______ ;反应结束后要继续通入一段时间氮气,主要目的是_______ 。
(2)装置E用来收集产物。实验过程中若D处因发生凝华出现堵塞,A装置中可观察到的现象是_______ ;可通过_______ (填操作)使实验继续进行。
(3)尾气与装置G中过量的 溶液发生反应的离子方程式是
溶液发生反应的离子方程式是_______ 。
(4)测定产品中 ,质量分数的实验步骤如下:
,质量分数的实验步骤如下:
Ⅰ.取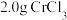 产品,在强碱性条件下,加入过量
产品,在强碱性条件下,加入过量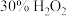 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,再继续加热一段时间。
,再继续加热一段时间。
Ⅱ.冷却后加适量的蒸馏水,再滴入适量的稀硫酸和浓磷酸(浓磷酸作用是防止指示剂提前变色),使 转化为
转化为 。
。
Ⅲ.在溶液中加入适量浓 混合均匀,滴入3滴试亚铁灵做指示剂,用新配制的
混合均匀,滴入3滴试亚铁灵做指示剂,用新配制的 标准溶液滴定,溶液由黄色经蓝绿色至红褐色即为终点,消耗
标准溶液滴定,溶液由黄色经蓝绿色至红褐色即为终点,消耗 标准溶液
标准溶液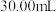 (滴定中
(滴定中 被
被 还原为
还原为 )。
)。
①计算产品中 质量分数为
质量分数为_______ 。
②下列操作将导致产品中 质量分数测定值偏低的是
质量分数测定值偏低的是_______ (填字母标号)。
A.步骤Ⅰ中未继续加热一段时间
B.步骤Ⅱ用盐酸替代硫酸
C.步骤Ⅲ中 溶液部分变质
溶液部分变质
D.步骤Ⅲ中读数时,滴定前俯视,滴定后平视
 )是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取
)是常用的媒染剂和催化剂,易潮解,易升华,高温下易被氧气氧化。实验室制取 的反应为:
的反应为: ,其实验装置如下图所示:
,其实验装置如下图所示:
已知:①
 (俗称光气)有毒,遇水发生水解:
(俗称光气)有毒,遇水发生水解: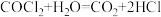 ;
;②碱性条件下,
 可将
可将 氧化为
氧化为 (黄色);酸性条件下,
(黄色);酸性条件下, 将
将 (橙色)还原为
(橙色)还原为 (绿色)。
(绿色)。(1)A装置用于干燥
 和观察其流速,A中的试剂是
和观察其流速,A中的试剂是 的作用是
的作用是(2)装置E用来收集产物。实验过程中若D处因发生凝华出现堵塞,A装置中可观察到的现象是
(3)尾气与装置G中过量的
 溶液发生反应的离子方程式是
溶液发生反应的离子方程式是(4)测定产品中
 ,质量分数的实验步骤如下:
,质量分数的实验步骤如下:Ⅰ.取
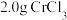 产品,在强碱性条件下,加入过量
产品,在强碱性条件下,加入过量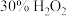 溶液,小火加热使
溶液,小火加热使 完全转化为
完全转化为 ,再继续加热一段时间。
,再继续加热一段时间。Ⅱ.冷却后加适量的蒸馏水,再滴入适量的稀硫酸和浓磷酸(浓磷酸作用是防止指示剂提前变色),使
 转化为
转化为 。
。Ⅲ.在溶液中加入适量浓
 混合均匀,滴入3滴试亚铁灵做指示剂,用新配制的
混合均匀,滴入3滴试亚铁灵做指示剂,用新配制的 标准溶液滴定,溶液由黄色经蓝绿色至红褐色即为终点,消耗
标准溶液滴定,溶液由黄色经蓝绿色至红褐色即为终点,消耗 标准溶液
标准溶液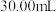 (滴定中
(滴定中 被
被 还原为
还原为 )。
)。①计算产品中
 质量分数为
质量分数为②下列操作将导致产品中
 质量分数测定值偏低的是
质量分数测定值偏低的是A.步骤Ⅰ中未继续加热一段时间
B.步骤Ⅱ用盐酸替代硫酸
C.步骤Ⅲ中
 溶液部分变质
溶液部分变质D.步骤Ⅲ中读数时,滴定前俯视,滴定后平视
您最近一年使用:0次
2022-03-29更新
|
663次组卷
|
3卷引用:山东省聊城市2021-2022学年下学期高三一模化学试题
名校
8 . 二氧化铈(CeO2)是重要的稀土氧化物。以氟碳铈矿(主要含CeFCO3)为原料制备CeO2的一种工艺流程如下:

已知:①CeO2具有较强的氧化性,难溶于一般的酸或碱。
②F-能和很多金属离子形成较为稳定的配合物,如Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF ;它的这种性质有利于酸浸步骤,却不利于后续的沉淀步骤。
;它的这种性质有利于酸浸步骤,却不利于后续的沉淀步骤。
③Ce4+ 能被萃取剂 TBP 萃取,而Ce3+ 不能。回答下列问题:
(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是___________ 。
(2)氧化焙烧后的固体产物中含有 CeO2和 CeF4物质的量之比为 3:1,“酸浸”时发生反应的离子方程式为___________ 。传统工艺中用盐酸替代硫酸,其缺点为___________ 。
(3)TBP是一种有机萃取剂,“萃取”时存在反应CeF3++TBP CeTBP4++F-,氟洗液中添加 Al3+的作用是
CeTBP4++F-,氟洗液中添加 Al3+的作用是___________ 。
(4)“反萃取”步骤中发生反应的离子方程式为___________ 。
(5)CeO2是汽车尾气净化催化剂的关键成分,在尾气消除过程中发生着 CeO2与 CeO2(1-x) (0≤x≤0.25)的相互转化。写出CeO2消除CO尾气的化学方程式:___________ 。
(6)CeO2(1-x)中的 Ce为+3、+4 价,测定x的值可判断它们的比例。现取CeO2(1-x)固体0.8280 g,加入足量硫酸和0.0110 mol FeSO4·7H2O充分溶解,使Ce4+全部被还原成Ce3+,再用0.1000 mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00 mL标准溶液。(已知氧化性:Ce4+>KMnO4)
①x的值为___________ 。
②若加入的 FeSO4·7H2O部分变质,会导致测定的 x 值___________ (填“偏高”“偏低”或“不变”)。

已知:①CeO2具有较强的氧化性,难溶于一般的酸或碱。
②F-能和很多金属离子形成较为稳定的配合物,如Ce4+能与F-结合成CeF3+,Al3+也能与F-结合成AlF
 ;它的这种性质有利于酸浸步骤,却不利于后续的沉淀步骤。
;它的这种性质有利于酸浸步骤,却不利于后续的沉淀步骤。③Ce4+ 能被萃取剂 TBP 萃取,而Ce3+ 不能。回答下列问题:
(1)“氧化焙烧”前需将矿石粉碎成细颗粒,其目的是
(2)氧化焙烧后的固体产物中含有 CeO2和 CeF4物质的量之比为 3:1,“酸浸”时发生反应的离子方程式为
(3)TBP是一种有机萃取剂,“萃取”时存在反应CeF3++TBP
 CeTBP4++F-,氟洗液中添加 Al3+的作用是
CeTBP4++F-,氟洗液中添加 Al3+的作用是(4)“反萃取”步骤中发生反应的离子方程式为
(5)CeO2是汽车尾气净化催化剂的关键成分,在尾气消除过程中发生着 CeO2与 CeO2(1-x) (0≤x≤0.25)的相互转化。写出CeO2消除CO尾气的化学方程式:
(6)CeO2(1-x)中的 Ce为+3、+4 价,测定x的值可判断它们的比例。现取CeO2(1-x)固体0.8280 g,加入足量硫酸和0.0110 mol FeSO4·7H2O充分溶解,使Ce4+全部被还原成Ce3+,再用0.1000 mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00 mL标准溶液。(已知氧化性:Ce4+>KMnO4)
①x的值为
②若加入的 FeSO4·7H2O部分变质,会导致测定的 x 值
您最近一年使用:0次
9 . 2Na2S2O3+I2=2NaI+Na2S4O6是定量分析中的常用反应。下列关于说法不正确 的是
| A.反应中,I2表现了氧化性 |
| B.反应中,每生成1 mol Na2S4O6,有4 mol e-发生转移 |
| C.Na2S2O3是含有共价键的离子化合物 |
| D.Na2S2O3在空气中放置会变质,产物可能有Na2SO4 |
您最近一年使用:0次
2021-01-22更新
|
984次组卷
|
9卷引用:北京市海淀区2021届高三上学期期末考试化学试题
北京市海淀区2021届高三上学期期末考试化学试题(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)2021年天津高考化学试题变式题1-12北京市中国人民大学附属中学2022届高三下学期第三次适应性练习化学试题山东省潍坊五县市2022-2023学年高三上学期10月质量检测联考化学试题山东省济宁市育才中学2022-2023学年高三10月线上阶段性检测化学试题北京市中国人民大学附属中学2022-2023学年高三上学期统练6化学试题北京工业大学附属中学2022-2023学年高三上学期开学测试化学试题
17-18高三上·北京·期中
名校
解题方法
10 . 亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如下:
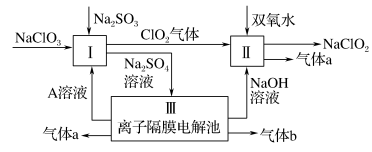
(1)Ⅰ中发生反应的还原剂是____ (填化学式)。
(2)Ⅱ中反应的离子方程式是____ 。
(3)Ⅲ中离子隔膜电解池的装置如下:
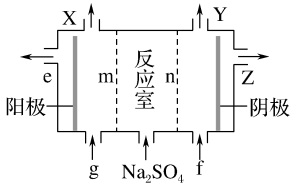
①A的化学式是________ ,A在____ 口产生。
②m为____ (填“阴”或“阳”)离子交换膜。
③结合化学用语和文字说明解释NaOH产生的原因:________
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O
①该反应中氧化剂和还原剂的物质的量之比是____ 。
②研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是____ 。
(5)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量前者____ (填“>”“<”或“=”)后者。

(1)Ⅰ中发生反应的还原剂是
(2)Ⅱ中反应的离子方程式是
(3)Ⅲ中离子隔膜电解池的装置如下:

①A的化学式是
②m为
③结合化学用语和文字说明解释NaOH产生的原因:
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备:5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O
①该反应中氧化剂和还原剂的物质的量之比是
②研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是
(5)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量前者
您最近一年使用:0次



