名校
解题方法
1 . 某处工厂排出的烟道气中含氮氧化物(主要为NO、 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式______________ ;若反应后尾气无残留,则参加反应的 、NO物质的量比值为
、NO物质的量比值为_____ (填字母)。
a.≥1 b.≤1 c.任意值
(2)可使用适量酸性 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是_______________ 。
(4)有氧条件下,NO在催化剂作用下可被 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是___________ 。
(5)羟基自由基( )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程:______________ 。 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加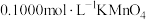 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗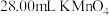 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数__________ 。(写出计算过程)
 )、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图:
)、粉尘和少量水蒸气.课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图: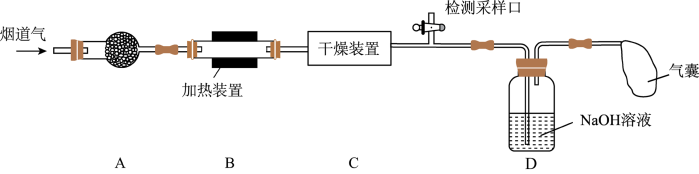
 混合气体按一定比例被
混合气体按一定比例被 溶液完全吸收生成
溶液完全吸收生成 和
和 ,写出该反应的化学方程式
,写出该反应的化学方程式 、NO物质的量比值为
、NO物质的量比值为a.≥1 b.≤1 c.任意值
(2)可使用适量酸性
 溶液,将溶液中的
溶液,将溶液中的 全部氧化为
全部氧化为 ,发生反应的离子方程式是
,发生反应的离子方程式是(3)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性
 溶液来处理。
溶液来处理。 氧化NO生成
氧化NO生成 和
和 ,发生反应的离子方程式是
,发生反应的离子方程式是(4)有氧条件下,NO在催化剂作用下可被
 还原为
还原为 。在钒基催化剂
。在钒基催化剂 作用下的脱硝反应机理如图所示:
作用下的脱硝反应机理如图所示: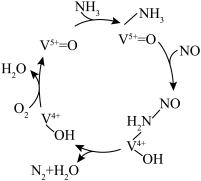
 在有氧条件下的总化学方程式是
在有氧条件下的总化学方程式是(5)羟基自由基(
 )也可以用于脱硫脱硝。如图表示光催化氧化技术可生成
)也可以用于脱硫脱硝。如图表示光催化氧化技术可生成 ﹔光照时,价带失去电子产生有强氧化性的空穴,价带上
﹔光照时,价带失去电子产生有强氧化性的空穴,价带上 直接转化为
直接转化为 ;描述产生
;描述产生 的另一种过程:
的另一种过程: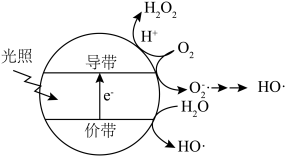
 等杂质,可以采用
等杂质,可以采用 测定含量。称取
测定含量。称取 该亚硝酸钠产品溶于水配制成
该亚硝酸钠产品溶于水配制成 的样品溶液。取
的样品溶液。取 该样品溶液于锥形瓶中,用稀
该样品溶液于锥形瓶中,用稀 酸化后,再向锥形瓶中滴加
酸化后,再向锥形瓶中滴加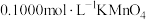 溶液,至恰好完全反应时,消耗
溶液,至恰好完全反应时,消耗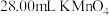 溶液。计算该产品中
溶液。计算该产品中 的质量分数
的质量分数
您最近一年使用:0次
2024-05-03更新
|
219次组卷
|
3卷引用:河南省焦作市博爱县第一中学2023-2024学年高一下学期4月期中考试化学试题
名校
2 . 为测定Cu和Cu2O混合粉末中Cu的含量。某同学将44.8g Cu和Cu2O混合粉末加入500mL 4.5mol/L的稀硝酸中,得到6.72LNO(标准状况下),忽略溶液体积的变化。下列说法正确的是
| A.反应后有固体剩余 | B.混合粉末中Cu的质量分数约为37% |
| C.反应后的溶液中c(Cu2+)=1.2mol/L | D.在反应后的溶液中加入足量铁粉,可置换出41.6g Cu |
您最近一年使用:0次
名校
3 . 以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O3既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
以下是一种废钒催化剂回收工艺路线:
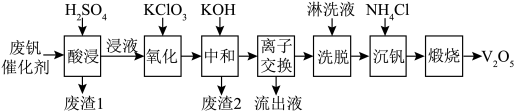
回答下列问题:
(1)“酸浸”时V2O5转化为 , 反应的离子方程式为
, 反应的离子方程式为___________ ,同时V2O4转化为 。“废渣1”的主要成分是
。“废渣1”的主要成分是______ 。
(2)“氧化”中使 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为______ 。
(3)“中和”后的溶液中,钒主要以 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
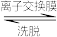
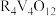 +
+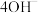 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈_____ 性(填“敢”或“碱”)。
(4)检验“流出液”中含量最多的阳离子,其实验操作称为___ 。
(5)“煅烧”中发生反应的化学方程式 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式_________ 。
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.20~2.90 | 2.8~3.32 | 22~28 | 60~65 | 1~2 | <1 |

回答下列问题:
(1)“酸浸”时V2O5转化为
 , 反应的离子方程式为
, 反应的离子方程式为 。“废渣1”的主要成分是
。“废渣1”的主要成分是(2)“氧化”中使
 变为
变为 , 则“氧化”环节中还原剂与氧化剂的物质的量之比为
, 则“氧化”环节中还原剂与氧化剂的物质的量之比为(3)“中和”后的溶液中,钒主要以
 形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
形式存在。“离子交换”和“洗脱”可简单表示为:4ROH+
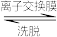
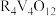 +
+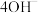 (以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈
(以ROH 为强碱性阴离子交换树脂)-为了提高洗脱效率, 淋洗液应该呈(4)检验“流出液”中含量最多的阳离子,其实验操作称为
(5)“煅烧”中发生反应的化学方程式
 ,写出“沉钒”过程的离子方程式
,写出“沉钒”过程的离子方程式
您最近一年使用:0次
解题方法
4 .  是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成
是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成 晶体以便储运。亚氯酸钠(
晶体以便储运。亚氯酸钠( )是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成
)是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成 。亚氯酸钠晶体的一种生产工艺如下:
。亚氯酸钠晶体的一种生产工艺如下:

已知:① 浓度过高时易发生分解爆炸,一般需稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般需稀释至含量10%以下。
② 受热易分解
受热易分解
(1)向“反应器”中鼓入空气的作用是___________ 。
(2)“吸收塔”的作用是将产生的 转化为
转化为 ,在此过程中加入的
,在此过程中加入的 是作用
是作用_______ (填“氧化剂”或“还原剂”),当有 参与该反应时,反应转移的电子数为
参与该反应时,反应转移的电子数为_________ 。
(3)“吸收塔”中需要控制温度不超过20℃,其原因是___________ 。
(4) 在温度高于60℃时易分解生成
在温度高于60℃时易分解生成 和NaCl,写出该化学方程式
和NaCl,写出该化学方程式________ 。
(5)写出“反应器”步骤中生成 的离子方程式
的离子方程式___________ 。
(6)为测定所得 (摩尔质量
(摩尔质量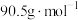 )产品的质量分数,进行如下实验:
)产品的质量分数,进行如下实验:
步骤I:准确称取所得亚氯酸钠样品1.000g于烧杯中,用适量蒸馏水和略过量的KI晶体,再滴加适量的稀硫酸,充分反应。(反应方程式为: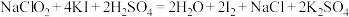 )
)
步骤Ⅱ:将所得溶液转移至250mL容量瓶中,稀释定容得溶液A;准确移取25.00mL溶液A于锥形瓶中,向锥形瓶中滴加两滴淀粉溶液作指示剂,用 的
的 标准溶液与之反应,至恰好完全反应时消耗
标准溶液与之反应,至恰好完全反应时消耗 溶液22.00mL。(反应方程式为:
溶液22.00mL。(反应方程式为: )
)
计算该产品中 的质量分数
的质量分数_______ (保留小数点后两位)。
 是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成
是新一代高效安全的杀菌剂,可用于自来水消毒。由于其浓度过高时易分解,常将其转化成 晶体以便储运。亚氯酸钠(
晶体以便储运。亚氯酸钠( )是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成
)是一种高效氧化剂和漂白剂,主要用于棉纺、纸张漂白、食品消毒、水处理等,消毒时本身被还原成 。亚氯酸钠晶体的一种生产工艺如下:
。亚氯酸钠晶体的一种生产工艺如下:
已知:①
 浓度过高时易发生分解爆炸,一般需稀释至含量10%以下。
浓度过高时易发生分解爆炸,一般需稀释至含量10%以下。②
 受热易分解
受热易分解(1)向“反应器”中鼓入空气的作用是
(2)“吸收塔”的作用是将产生的
 转化为
转化为 ,在此过程中加入的
,在此过程中加入的 是作用
是作用 参与该反应时,反应转移的电子数为
参与该反应时,反应转移的电子数为(3)“吸收塔”中需要控制温度不超过20℃,其原因是
(4)
 在温度高于60℃时易分解生成
在温度高于60℃时易分解生成 和NaCl,写出该化学方程式
和NaCl,写出该化学方程式(5)写出“反应器”步骤中生成
 的离子方程式
的离子方程式(6)为测定所得
 (摩尔质量
(摩尔质量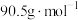 )产品的质量分数,进行如下实验:
)产品的质量分数,进行如下实验:步骤I:准确称取所得亚氯酸钠样品1.000g于烧杯中,用适量蒸馏水和略过量的KI晶体,再滴加适量的稀硫酸,充分反应。(反应方程式为:
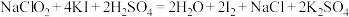 )
)步骤Ⅱ:将所得溶液转移至250mL容量瓶中,稀释定容得溶液A;准确移取25.00mL溶液A于锥形瓶中,向锥形瓶中滴加两滴淀粉溶液作指示剂,用
 的
的 标准溶液与之反应,至恰好完全反应时消耗
标准溶液与之反应,至恰好完全反应时消耗 溶液22.00mL。(反应方程式为:
溶液22.00mL。(反应方程式为: )
)计算该产品中
 的质量分数
的质量分数
您最近一年使用:0次
名校
5 . 海洋是一个巨大的化学资源宝库,其中钠元素和氯元素是海洋中含量较高的元素。生活中也有很多含钠、含氯的化合物。请结合所学化学知识,回答下列问题。
(1)过氧化钠可以在潜水艇和消防员的呼吸面具中作为氧气来源。若只考虑过氧化钠与二氧化碳反应,每消耗1mol过氧化钠固体、反应转移电子数为_____ 。
(2)漂白粉广泛用于环境的消毒、杀菌。漂白粉溶于水后,与空气中的二氧化碳反应,能生成具有强漂白性的物质。请用离子方程式表示该过程:_____ 。
(3)“84消毒液”能有效杀灭病毒,某同学购买了瓶“84消毒液”,其说明中有如下信息:NaClO质量分数为25%、密度为 、1000mL、请稀释后使用。
、1000mL、请稀释后使用。
①该“84消毒液”中NaClO的物质的量浓度为_____  。(保留至小数点后一位)
。(保留至小数点后一位)
②现实验室需要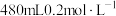 的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液。应用托盘天平称取NaClO固体
的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液。应用托盘天平称取NaClO固体_____ g。配制NaClO溶液时需用的主要仪器有托盘天平、药匙、烧杯、量筒、玻璃棒、_____ 、_____ 。
③实验时遇到下列情况,会导致溶液物质的量浓度偏高的是_____ (填标号)。
A.容量瓶内壁附有水珠而未干燥处理
B.称量使用的砝码已生锈
C.溶解时使用的烧杯及玻璃棒未洗涤
D.溶解后没有冷却便进行定容
E.定容时俯视刻度线
F.摇匀后发现液面低于刻度线后未做处理
(1)过氧化钠可以在潜水艇和消防员的呼吸面具中作为氧气来源。若只考虑过氧化钠与二氧化碳反应,每消耗1mol过氧化钠固体、反应转移电子数为
(2)漂白粉广泛用于环境的消毒、杀菌。漂白粉溶于水后,与空气中的二氧化碳反应,能生成具有强漂白性的物质。请用离子方程式表示该过程:
(3)“84消毒液”能有效杀灭病毒,某同学购买了瓶“84消毒液”,其说明中有如下信息:NaClO质量分数为25%、密度为
 、1000mL、请稀释后使用。
、1000mL、请稀释后使用。①该“84消毒液”中NaClO的物质的量浓度为
 。(保留至小数点后一位)
。(保留至小数点后一位)②现实验室需要
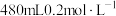 的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液。应用托盘天平称取NaClO固体
的NaClO溶液,某同学用NaClO固体配制该物质的量浓度的溶液。应用托盘天平称取NaClO固体③实验时遇到下列情况,会导致溶液物质的量浓度偏高的是
A.容量瓶内壁附有水珠而未干燥处理
B.称量使用的砝码已生锈
C.溶解时使用的烧杯及玻璃棒未洗涤
D.溶解后没有冷却便进行定容
E.定容时俯视刻度线
F.摇匀后发现液面低于刻度线后未做处理
您最近一年使用:0次
2023-11-09更新
|
217次组卷
|
2卷引用:湖南省长沙市长郡中学2023-2024学年高一上学期期中考试化学试题
名校
6 . 钛是航空、军工、电力等领域的重要原材料。地壳中的含钛矿石之一是金红石( ),其是冶炼钛的重要原料。生产钛的工艺流程如图:
),其是冶炼钛的重要原料。生产钛的工艺流程如图:

已知:①常温下,钛既不与常见非金属单质反应,也不与强酸反应;
②加热时,钛可以和常见的非金属单质反应。
(1)在反应I中:
①下列有关CO的说法正确的是_______ (填标号)。
A.属于酸性氧化物 B.摩尔质量为28 C.为可燃性气体 D.具有还原性
②反应I的化学方程式为_______ ,该反应中氧化剂与还原剂的质量之比为_______ 。
③每转移0.2mol电子,同时生成CO的体积为_______ (标准状况下)。
(2)在反应II中:
①氩气的作用为_______ 。
②该反应的基本反应类型为_______ 。
(3)为了测定反应II制得的金属钛(杂质仅含Mg)中的钛元素含量。常温下,取mg反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为 的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:
的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:
①上述反应的离子方程式为_______ 。
②金属钛的质量分数为_______ (用含m、c、V的代数式表示)。
 ),其是冶炼钛的重要原料。生产钛的工艺流程如图:
),其是冶炼钛的重要原料。生产钛的工艺流程如图:
已知:①常温下,钛既不与常见非金属单质反应,也不与强酸反应;
②加热时,钛可以和常见的非金属单质反应。
(1)在反应I中:
①下列有关CO的说法正确的是
A.属于酸性氧化物 B.摩尔质量为28 C.为可燃性气体 D.具有还原性
②反应I的化学方程式为
③每转移0.2mol电子,同时生成CO的体积为
(2)在反应II中:
①氩气的作用为
②该反应的基本反应类型为
(3)为了测定反应II制得的金属钛(杂质仅含Mg)中的钛元素含量。常温下,取mg反应II制得的金属钛置于烧杯中,往烧杯中逐滴滴入物质的量浓度为
 的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:
的稀硫酸,当不再出现气泡时,共消耗VmL稀硫酸:①上述反应的离子方程式为
②金属钛的质量分数为
您最近一年使用:0次
2023-01-11更新
|
287次组卷
|
7卷引用:辽宁省辽西联合校2023-2024学年高三上学期期中考试化学试题
名校
7 . 2020年初,突如其来的新型冠状肺炎在全世界肆虐,依据研究,含氯消毒剂可以有效消灭新冠病毒,为阻断疫情做出了巨大贡献。二氧化氯(ClO2)就是其中一种高效消毒灭菌剂,但其稳定性较差,可转化为NaClO2保存。分别利用吸收法和电解法两种方法得到较稳定的NaClO2。其工艺流程示意图如图所示:

已知:(Ⅰ)纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(Ⅱ)饱和NaClO2溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时NaClO2分解成NaClO3和NaCl。
(1)步骤1中,生成C1O2的离子方程式是_______ ,通入空气的作用是_________ 。
(2)方法1中,反应的离子方程式是_________________ ,利用方法1制NaClO2时,温度不能超过20 ℃,可能的原因是______ 。
(3)方法2中,将ClO2通入电解槽的阴极室,饱和NaCl溶液加入电解槽的阳极室,电解一段时间后,可得到产品,写出电解时阴极的电极反应式________________ 。
(4)步骤3中从NaClO2溶液中获得NaClO2晶体的操作步骤为:①减压,55 ℃蒸发结晶;②趁热过滤;③__________________ ;④低于60 ℃干燥,得到成品。
(5)为测定制得的晶体中NaClO2的含量,做如下操作:
①称取a g样品于烧杯中,加入适量蒸馏水溶解后加过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应。将所得混合液配成100 mL待测溶液。
②移取25.00 mL待测溶液于锥形瓶中,用b mol·L−1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为c mL(已知:I2+2 =2I−+
=2I−+ )。样品中NaClO2的质量分数为
)。样品中NaClO2的质量分数为_____ 。(用含a、b、c的代数式表示)。在滴定操作正确无误的情况下,测得结果偏高,可能的原因是_______________ (用离子方程式和文字表示)。

已知:(Ⅰ)纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(Ⅱ)饱和NaClO2溶液在温度低于38 ℃时析出的晶体是NaClO2·3H2O,高于38 ℃时析出的晶体是NaClO2,高于60 ℃时NaClO2分解成NaClO3和NaCl。
(1)步骤1中,生成C1O2的离子方程式是
(2)方法1中,反应的离子方程式是
(3)方法2中,将ClO2通入电解槽的阴极室,饱和NaCl溶液加入电解槽的阳极室,电解一段时间后,可得到产品,写出电解时阴极的电极反应式
(4)步骤3中从NaClO2溶液中获得NaClO2晶体的操作步骤为:①减压,55 ℃蒸发结晶;②趁热过滤;③
(5)为测定制得的晶体中NaClO2的含量,做如下操作:
①称取a g样品于烧杯中,加入适量蒸馏水溶解后加过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应。将所得混合液配成100 mL待测溶液。
②移取25.00 mL待测溶液于锥形瓶中,用b mol·L−1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为c mL(已知:I2+2
 =2I−+
=2I−+ )。样品中NaClO2的质量分数为
)。样品中NaClO2的质量分数为
您最近一年使用:0次
2021-11-12更新
|
427次组卷
|
3卷引用:河北省唐山市第一中学2021-2022学年高三上学期期中考试化学试题
名校
解题方法
8 . 氮化钙有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。某化学兴趣小组设计制备氮化钙并测定其纯度的实验如下:
已知:氮化钙(Ca3N2)是一种棕色粉末,遇水会发生水解,生成氢氧化钙并放出氨。
I.氮化钙的制备(如图):

(1)仪器a的名称是_______ 。
(2)装置A中每生成标准状况下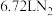 ,转移的电子数为
,转移的电子数为_______ 。
(3)装置C的作用是吸收氧气,则C中发生反应的离子方程式为_______ 。
(4)设计实验证明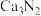 中混有钙单质,写出实验操作及现象:
中混有钙单质,写出实验操作及现象:_______ 。
II.测定氮化钙的纯度:
(5)甲同学称取mg反应后的固体,加入足量的碳酸钠溶液充分反应,过滤、洗涤、干燥得ng沉淀,通过数据m、n即可求得氮化钙的质量分数。
甲同学的方案是否合理?_______ (填“是”或“否”),理由是_______ 。
(6)乙同学的方案如下:
取氮化钙样品24g,按图所示装置进行实验,发现B装置增重5.1g。
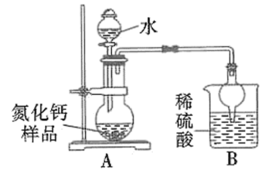
①该样品中氮化钙的质量分数为_______ 。
②导致该样品中氮化钙含量测定结果偏低的可能原因是_______ 。
已知:氮化钙(Ca3N2)是一种棕色粉末,遇水会发生水解,生成氢氧化钙并放出氨。
I.氮化钙的制备(如图):

(1)仪器a的名称是
(2)装置A中每生成标准状况下
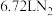 ,转移的电子数为
,转移的电子数为(3)装置C的作用是吸收氧气,则C中发生反应的离子方程式为
(4)设计实验证明
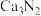 中混有钙单质,写出实验操作及现象:
中混有钙单质,写出实验操作及现象:II.测定氮化钙的纯度:
(5)甲同学称取mg反应后的固体,加入足量的碳酸钠溶液充分反应,过滤、洗涤、干燥得ng沉淀,通过数据m、n即可求得氮化钙的质量分数。
甲同学的方案是否合理?
(6)乙同学的方案如下:
取氮化钙样品24g,按图所示装置进行实验,发现B装置增重5.1g。

①该样品中氮化钙的质量分数为
②导致该样品中氮化钙含量测定结果偏低的可能原因是
您最近一年使用:0次
2021-09-16更新
|
255次组卷
|
3卷引用:广西钦州市第四中学2021-2022学年高三上学期期中考试理综化学试题
名校
解题方法
9 . 废弃物的综合利用有利于节约资源、保护环境。实验室利用废旧电池的铜帽(Cu、Zn总含量约为99%)制备ZnSO4·7H2O和CuSO4·5H2O的部分实验步骤如下:

(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是_____ (任写一种方法)。
(2) 从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为_____ 、_____ 、过滤、冰水洗涤、低温干燥。
(3)在“溶解II”步骤中,发生反应的化学方程式为_____________ 。
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol·L-1Na2S2O3溶液至刚好完全反应,消耗Na2S2O3溶液25.00mL。已知:2Cu2++4I-=2CuI(白色)↓+I2, 2S2O +I2=2I-+S4O
+I2=2I-+S4O 请依据实验数据计算样品中CuSO4·5H2O的质量分数(写出计算过程,结果保留4位有效数字)
请依据实验数据计算样品中CuSO4·5H2O的质量分数(写出计算过程,结果保留4位有效数字)_______ 。

(1)在“溶解I”步骤中,为加快溶解速率,可采取的措施是
(2) 从“滤液I”中提取ZnSO4·7H2O的实验步骤依次为
(3)在“溶解II”步骤中,发生反应的化学方程式为
(4)为测定产品中CuSO4·5H2O的纯度,称取1.270g样品,溶于稀硫酸并稀释至250mL,取出25.00mL溶液于锥形瓶中,加入过量的KI溶液充分反应,再向其中逐滴加入0.02000mol·L-1Na2S2O3溶液至刚好完全反应,消耗Na2S2O3溶液25.00mL。已知:2Cu2++4I-=2CuI(白色)↓+I2, 2S2O
 +I2=2I-+S4O
+I2=2I-+S4O 请依据实验数据计算样品中CuSO4·5H2O的质量分数(写出计算过程,结果保留4位有效数字)
请依据实验数据计算样品中CuSO4·5H2O的质量分数(写出计算过程,结果保留4位有效数字)
您最近一年使用:0次
2020-11-11更新
|
156次组卷
|
2卷引用:江苏省扬州中学2020-2021学年高一上学期期中考试化学试题
10 . 锂离子电池是目前具有最高比能量的二次电池。LiFePO4可极大地改善电池体系的安全性能,且具有资源丰富、循环寿命长、环境友好等特点,是锂离子电池正极材料的理想选择。生产LiFePO4的一种工艺流程如图:

已知:①Ksp[Fe(OH)3]=4.0×10-38,Ksp(FePO4·xH2O)=1.0×10-15。
②葡萄糖分子式为C6H12O6
回答下列问题:
(1)在合成磷酸铁时,步骤Ⅰ中pH的控制是关键。如果pH<1.9,Fe3+沉淀不完全,影响产量;如果pH>3.0,则可能存在的问题是_________ 。
(2)步骤Ⅱ中,洗涤是为了除去FePO4·xH2O表面附着的________ 等离子。
(3)取三组FePO4·xH2O样品,经过高温充分煅烧测其结晶水含量,实验数据如下表:
固体失重质量分数=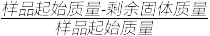 100%
100%
则x=________ (精确至0.1)。
(4)步骤Ⅲ中研磨的作用是__________ 。
(5)在步骤Ⅳ中生成了LiFePO4、CO2和H2O,则氧化剂与还原剂的物质的量之比为________ 。
(6)H3PO4是三元酸,如图是溶液中含磷微粒的物质的量分数(δ)随pH变化示意图。则PO 第一步水解的水解常数K1的数值最接近
第一步水解的水解常数K1的数值最接近________ (填字母)。

A.10-12.4 B.10-1.6 C.10-7.2 D.10-4.2

已知:①Ksp[Fe(OH)3]=4.0×10-38,Ksp(FePO4·xH2O)=1.0×10-15。
②葡萄糖分子式为C6H12O6
回答下列问题:
(1)在合成磷酸铁时,步骤Ⅰ中pH的控制是关键。如果pH<1.9,Fe3+沉淀不完全,影响产量;如果pH>3.0,则可能存在的问题是
(2)步骤Ⅱ中,洗涤是为了除去FePO4·xH2O表面附着的
(3)取三组FePO4·xH2O样品,经过高温充分煅烧测其结晶水含量,实验数据如下表:
| 实验序号 | 1 | 2 | 3 |
| 固体失重质量分数/% | 19.9 | 20.1 | 20.0 |
固体失重质量分数=
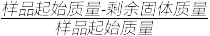 100%
100%则x=
(4)步骤Ⅲ中研磨的作用是
(5)在步骤Ⅳ中生成了LiFePO4、CO2和H2O,则氧化剂与还原剂的物质的量之比为
(6)H3PO4是三元酸,如图是溶液中含磷微粒的物质的量分数(δ)随pH变化示意图。则PO
 第一步水解的水解常数K1的数值最接近
第一步水解的水解常数K1的数值最接近
A.10-12.4 B.10-1.6 C.10-7.2 D.10-4.2
您最近一年使用:0次
2020-11-29更新
|
176次组卷
|
2卷引用:湖北省部分省重点中学2020-2021学年高二上学期期中联考化学试题



