名校
1 . 学以致用是学习化学的动力和源泉,掌握化学知识有助于我们更好地认识世界。回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是______ ,胶体和溶液的本质区别是_______ 。
(2)生铁是______ (填“混合物”或“化合物”)。通常合金的熔点_____ (填“高于”或“低于”)其组成单质的熔点。
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得: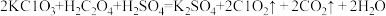 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为______ mol;该反应中的还原剂是______ (填化学式)。
(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=____ 。
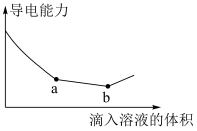
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是______ ,从a点到b点反应的离子方程式是______ ,解释b点之后导电能力上升的原因:______ 。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)生铁是
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得:
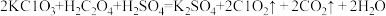 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是
您最近一年使用:0次
2024-01-28更新
|
104次组卷
|
4卷引用:新疆生产建设兵团第三师图木舒克市第二中学2023-2024学年高一下学期开学考试化学试题
名校
解题方法
2 . 硝酸厂烟气中的大量NO经还原法可转化为无害物质。常温下,将NO与 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法错误的是
的混合溶液中,其转化过程如图所示。下列说法错误的是
 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法错误的是
的混合溶液中,其转化过程如图所示。下列说法错误的是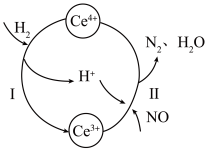
A.该转化过程的实质为NO被 还原 还原 |
| B.反应I中氧化剂与还原剂的物质的量之比为1∶2 |
C.反应II的离子反应方程式为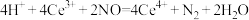 |
D.反应过程中混合溶液内 和 和 的总数不变 的总数不变 |
您最近一年使用:0次
2023-11-29更新
|
671次组卷
|
5卷引用:新疆生产建设兵团第三师图木舒克市第二中学2023-2024学年高一下学期开学考试化学试题
名校
解题方法
3 . 如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为:CH3CH2OH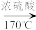 CH2=CH2↑十H2O;回答下列问题:
CH2=CH2↑十H2O;回答下列问题:
(1)图 1 中仪器①、②的名称分别为_______ 、_______ 。
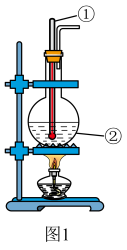
(2)收集乙烯气体最好的收集方法是_______ 。
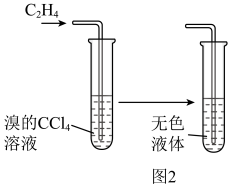
(3)向溴的四氯化碳溶液中通入乙烯(如图 2),溶液的颜色很快褪去,该反应属于_______ (填反应类型) 。
(4)铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
①黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料,其中发生的一个反应为 3FeS2+8O2 6SO2+Fe3O4;若有 3 mol FeS2参加反应,则转移
6SO2+Fe3O4;若有 3 mol FeS2参加反应,则转移_______ mol 电子。
②氯化铁溶液常用作印刷电路铜板的腐蚀剂, 反应的离子方程式为_______ 。从腐蚀废液中回收金属铜还需要的试剂是_______ 。
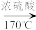 CH2=CH2↑十H2O;回答下列问题:
CH2=CH2↑十H2O;回答下列问题:(1)图 1 中仪器①、②的名称分别为

(2)收集乙烯气体最好的收集方法是
(3)向溴的四氯化碳溶液中通入乙烯(如图 2),溶液的颜色很快褪去,该反应属于

(4)铁单质及其化合物在生活、生产中有广泛应用。请回答下列问题:
①黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料,其中发生的一个反应为 3FeS2+8O2
 6SO2+Fe3O4;若有 3 mol FeS2参加反应,则转移
6SO2+Fe3O4;若有 3 mol FeS2参加反应,则转移②氯化铁溶液常用作印刷电路铜板的腐蚀剂, 反应的离子方程式为
您最近一年使用:0次
名校
解题方法
4 . 将 铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为
铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为 ,放出的气体
,放出的气体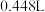 (标准状况)。则下列判断中正确的是
(标准状况)。则下列判断中正确的是
 铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为
铁和氧化铁的混合物加入足量的盐酸中充分反应,固体无剩余。测得参加反应的盐酸的物质的量为 ,放出的气体
,放出的气体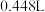 (标准状况)。则下列判断中正确的是
(标准状况)。则下列判断中正确的是A.原混合物中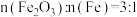 |
B.原混合物中氧化铁的质量为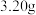 |
C.向所得溶液中滴加 溶液,溶液显红色 溶液,溶液显红色 |
D.向所得溶液中通入 ,可以将 ,可以将 完全转化为 完全转化为 |
您最近一年使用:0次
2023-01-01更新
|
585次组卷
|
5卷引用:新疆乌鲁木齐市第八中学2022-2023学年高一下学期第一次质量检测(开学摸底)化学试题
名校
5 . 潜艇中氧气来源之一的反应是:2Na2O2+2H2O=4NaOH+O2↑。用NA表示阿伏加德罗常数,下列说法正确的是
| A.22.4LO2含2NA个O原子 | B.1.8gH2O含有的质子数为NA |
| C.1molNa2O2含共价键的总数为2NA | D.上述反应,每生成1molO2转移4NA电子 |
您最近一年使用:0次
2022-10-25更新
|
106次组卷
|
2卷引用:新疆第二师八一中学2022-2023学年高三上学期开学考试化学试题
名校
解题方法
6 . 已知:将Cl2通入适量NaOH溶液中,反应会放热,当温度升高后会发生如下反应:3Cl2+6NaOH=5NaCl+NaClO3+3H2O。则Cl2通入NaOH溶液的产物中可能有NaCl、NaClO、NaClO3中的两种或三种,且 的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
 的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是
的值与温度高低有关。当参与反应的n(NaOH)= a mol时,下列说法错误的是| A.与碱的反应中,Cl2既是氧化剂又是还原剂 |
| B.参加反应的Cl2物质的量为0.5a mol |
C.若某温度下,反应后 =6,则溶液中 =6,则溶液中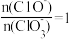 |
D.改变温度,反应中转移电子的物质的量可能为 mol mol |
您最近一年使用:0次
2022-10-24更新
|
2077次组卷
|
12卷引用:新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题
新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试(选考)化学试题江苏省苏州中学2022-2023学年高一下学期开学考试化学试题陕西省安康市2022-2023学年高一下学期开学摸底考试化学试题江苏省无锡市锡山高级中学2021-2022学年高一上学期期中考试化学试题山东省实验中学2022-2023学年高一上学期11月期中考试化学试题甘肃省酒泉市玉门油田第一中学2022-2023学年高一上学期期中考试化学(A卷)试题北京市第八中学2022-2023学年高一上学期12月月考化学试题陕西省榆林中学2022-2023学年高一上学期期末考试化学试题辽宁省沈阳市五校协作体2022-2023学年高一上学期期末考试化学试题 山东省淄博市部分学校联考2022-2023学年高一下学期4月期中考试化学试题(已下线)专题03 氧化还原反应-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
名校
7 . NaNO2是一种食品添加剂,它能致癌。酸性KMnO4溶液与NaNO2反应的化学方程式是:  +
+ +____→Mn2++
+____→Mn2++ +H2O。下列叙述中正确的是
+H2O。下列叙述中正确的是
 +
+ +____→Mn2++
+____→Mn2++ +H2O。下列叙述中正确的是
+H2O。下列叙述中正确的是A.该反应中 被还原 被还原 |
| B.反应过程中溶液的pH减小 |
| C.生成1molNaNO3需消耗0.4molKMnO4 |
| D.横线中的粒子是OH- |
您最近一年使用:0次
2022-07-26更新
|
554次组卷
|
45卷引用:2017届新疆兵团农二师华山中学高三上学前考试化学试卷
2017届新疆兵团农二师华山中学高三上学前考试化学试卷黑龙江省牡丹江市第一高级中学2019-2020学年高二上学期开学检测化学试题云南省漾濞二中2020届高三上学期开学考试化学试题黑龙江省佳木斯市第八中学2022-2023学年高三上学期第一次调研(开学考试)化学试题(已下线)2013届浙江省宁波市效实中学高三上学期期中考试化学试卷(已下线)2014届福建省南侨中学等五校高中毕业班期末摸底考试化学试卷(已下线)2014高考化学名师知识点精编 专题4氧化还原反应练习卷2016届湖南省益阳市箴言中学高三上学期第二次模拟测试化学试卷2016-2017学年河南省南阳一中高一上月考二化学卷2016-2017学年河南省南阳一中高一月考二化学卷天津市和平区2017-2018学年高一上学期期中质量调查化学试题辽宁省盘锦市高级中学2017-2018学年高二下学期期末考试化学试题2018-2019学年人教版高中化学必修一模块综合测评题(A)2018-2019学年苏教版高中化学必修一 模块综合测评(A)河南省安阳市第三十六中学2018-2019学年高二6月月考化学试题(已下线)专题2.3 氧化还原反应(练)-《2020年高考一轮复习讲练测》江西省赣州市寻乌中学2020届高三上学期第一阶段考试化学试题(已下线)专题四 氧化还原反应(提分特训)-2020年高考二轮模块化复习之《化学基本概念》名师讲案与提分特训(已下线)衔接点09 氧化还原反应的表示-2020年【衔接教材·暑假作业】初高中衔接化学(已下线)第09讲 氧化还原反应的计算及方程式的配平(精练)——2021年高考化学一轮复习讲练测高一必修第一册(鲁科2019)考试帮 模块综合测评B卷人教版(2019)高一必修第一册 模块综合测评-B卷贵州省铜仁市思南中学2021届高三上学期第二次月考化学试题江西省上饶市万年中学2020-2021学年高一上学期期中考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练湖南省武冈市第二中学2020-2021学年高一上学期第一次月考化学试题(已下线)衔接点09 氧化还原反应的表示-2021年初升高化学无忧衔接西藏拉萨市拉萨中学2022届高三上学期第一次月考理综化学试题黑龙江省哈尔滨市第六中学2021-2022学年高三上学期期中考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)4.2.2 氧化还原反应方程式的配平(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)黑龙江省哈尔滨市第九中学2021-2022学年高一上学期期中学业阶段性评价考试化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题01 物质及其变化-2023年高考化学一轮复习小题多维练(全国通用)黑龙江省哈尔滨市香坊区第九中学校2021-2022学年高一上学期期中考试化学试题西藏林芝市第二高级中学2022-2023学年高三上学期第二次月考化学试题(已下线)第一章 化学物质及其变化 第5练 氧化还原反应的计算与方程式的配平(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)山东省枣庄市第三中学2022-2023学年高一上学期12月期中考试化学试题宁夏银川市第二中学2023-2024学年高三上学期统练二化学试题黑龙江省龙西北名校联合体2023-2024学年高三上学期期中考试化学试题黑龙江省齐齐哈尔市龙西北高中名校联盟2023-2024学年高三上学期10月联考化学试题江西省南昌市第十九中学2022-2023学年高一上学期12月第二次月考化学试卷
名校
8 . 二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO2的反应原理如下:2NaClO3 + 4HCl=2ClO2↑+ Cl2↑+2H2O + 2NaCl,下列关于该反应的说法中正确的是
| A.每生成0.1mol ClO2转移0.2mol电子 |
| B.氧化性:NaClO3< Cl2 |
| C.浓盐酸在反应中仅体现还原性 |
| D.反应中氧化剂和还原剂的物质的量之比为1:1 |
您最近一年使用:0次
2022-04-13更新
|
55次组卷
|
2卷引用:新疆喀什第二中学2021-2022学年高一下学期开学考试化学试题
名校
解题方法
9 . 对于反应3Cl2+6NaOH=5NaCl+NaClO3+3H2O,以下叙述正确的是
| A.Cl2是氧化剂,NaOH是还原剂 |
| B.每生成1mol的NaClO3转移6mol电子 |
| C.Cl2既是氧化剂又是还原剂 |
| D.被氧化的Cl原子和被还原的Cl原子的物质的量之比为5:1 |
您最近一年使用:0次
2022-03-24更新
|
90次组卷
|
18卷引用:新疆沙湾第一中学2020-2021学年高一下学期入学考试化学试题
新疆沙湾第一中学2020-2021学年高一下学期入学考试化学试题安徽省滁州市定远县育才学校2019-2020学年高二上学期入学考试化学试题四川省自贡市田家炳中学2020-2021学年高一下学期开学考试化学试题(已下线)2014-2015福建省福州文博中学高一上学期期中化学试卷2015-2016学年辽宁省大连二十中学高一上学期期中测试化学试卷2016-2017学年浙江省杭州市五县七校高一上期中化学试卷贵州省兴义中学2017-2018学年高一上学期期中考试化学试题黑龙江省牡丹江市第三高级中学2018-2019学年高一上学期期中考试化学试题内蒙古自治区正镶白旗察汗淖中学2018-2019学年高一上学期期末考试化学试题黑龙江省牡丹江市第三高级中学2019-2020学年高一上学期期中考试化学试题浙江省杭州市西湖高级中学2019-2020学年高一12月月考化学试题2019-2020学年高一上学期期末复习《新题速递·化学》12月(考点01-05)陕西省西安市第八十五中学2019-2020学年高一上学期期末考试化学试题(已下线)【浙江新东方】1(已下线)【浙江新东方】90湖南省长沙市明德中学2020-2021学年高一上学期第三月考化学试题陕西省洋县中学2021-2022学年高一上学期期末考试化学试题广西河池市罗城仫佬族自治县高级中学等2校2022-2023学年高一上学期12月月考化学试题
10 . 饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,其化学方程式为:
还原为N2,其化学方程式为: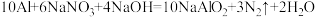 。请回答下列问题:
。请回答下列问题:
(1)上述反应中,被氧化的元素___________ ,还原产物是___________ 。
(2)用“双线桥法”表示反应中电子转移的方向和数目:___________ 。
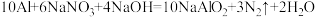
(3)反应中每生成1个N2,转移___________ 个电子。
(4)请配平下列离子方程式___________ 。

(5)已知I-、Fe2+、SO2、Cl-、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为: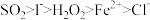 ,则下列反应不能发生的是___________。
,则下列反应不能发生的是___________。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,可以在碱性条件下用铝粉将
的浓度,可以在碱性条件下用铝粉将 还原为N2,其化学方程式为:
还原为N2,其化学方程式为: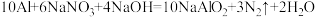 。请回答下列问题:
。请回答下列问题:(1)上述反应中,被氧化的元素
(2)用“双线桥法”表示反应中电子转移的方向和数目:
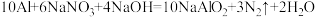
(3)反应中每生成1个N2,转移
(4)请配平下列离子方程式

(5)已知I-、Fe2+、SO2、Cl-、H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为:
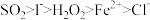 ,则下列反应不能发生的是___________。
,则下列反应不能发生的是___________。A.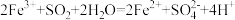 | B.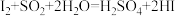 |
C.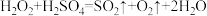 | D.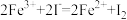 |
您最近一年使用:0次
2022-03-08更新
|
238次组卷
|
4卷引用:新疆乌苏市第一中学2021-2022学年高一下学期开学考试化学(A)试题



