名校
解题方法
1 . 已知反应 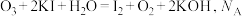 为阿伏加德罗常数的值,若生成
为阿伏加德罗常数的值,若生成  (标况),下列说法错误的是
(标况),下列说法错误的是
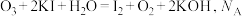 为阿伏加德罗常数的值,若生成
为阿伏加德罗常数的值,若生成  (标况),下列说法错误的是
(标况),下列说法错误的是A.转移的电子数目为  | B. 的 的 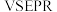 模型为 模型为 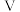 形 形 |
C.参与反应的  含有孤电子对数为 含有孤电子对数为 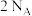 | D.生成的还原产物质量为  |
您最近一年使用:0次
名校
2 . 造纸、印刷等工业废水中含有大量的硫化物(主要成分为 ),可用如图转化方式除去,则下列说法错误的是
),可用如图转化方式除去,则下列说法错误的是
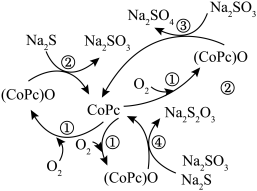
 ),可用如图转化方式除去,则下列说法错误的是
),可用如图转化方式除去,则下列说法错误的是
A. 溶液中存在 溶液中存在 |
B.反应②和③的转移电子数相等时,还原剂之比为 |
C.在废水处理过程中,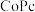 为催化剂, 为催化剂, 为氧化剂 为氧化剂 |
D.反应④中 与 与 等物质的量反应,反应的化学方程式为 等物质的量反应,反应的化学方程式为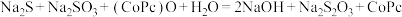 |
您最近一年使用:0次
3 . 汽车剧烈碰撞时,安全气囊中发生反应 。对于该反应,下列判断正确的是
。对于该反应,下列判断正确的是
 。对于该反应,下列判断正确的是
。对于该反应,下列判断正确的是| A.氧化产物与还原产物分子个数之比为15∶1 |
| B.氧化剂和还原剂是同一物质 |
| C.反应过程中转移1mol电子,则产生2.24L气体(标准状况) |
D. 中氮元素的化合价为-1 中氮元素的化合价为-1 |
您最近一年使用:0次
4 . NO 在维持心血管功能方面具有重要作用,实验室通过干法制备NO的原理为:3KNO2+KNO3+Cr2O3═2K2CrO4+4NO↑。 下列说法不正确的是
| A.NO是极性分子 |
B. 的键角小于NO 的键角小于NO |
| C.氧化产物与还原产物的物质的量之比1∶2 |
| D.每消耗 10.1 g KNO3时,被KNO3氧化的Cr2O3为0.1 mol |
您最近一年使用:0次
解题方法
5 . 化学源自生活和生产实践,并随着人类社会的进步而不断发展。根据所学知识,回答下列问题:
(1)分类是认识和研究物质及其变化的一种常用的科学方法,如图所示分类方法是__________ (选填“树状分类法”或“交叉分类法”)。
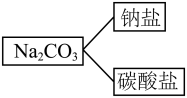
(2)下列物质:①液氯 ②盐酸 ③ ④硝酸钾固体 ⑤熔融
④硝酸钾固体 ⑤熔融 ⑥铜,其中属于电解质的是
⑥铜,其中属于电解质的是__________ (填序号,后同),能导电的是__________ ,④的电离方程式为__________ 。
(3) 所含化学键的类型
所含化学键的类型__________ 。
(4)氢化钠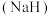 可在野外用作生氢剂,其原理为
可在野外用作生氢剂,其原理为 ,该反应的还原剂是
,该反应的还原剂是__________ (填化学式),生成 转移的电子数目为
转移的电子数目为__________ 。
(5)碳酸钠是一种重要的化工基本原料,俗称__________ ,向碳酸钠溶液中滴加少量稀盐酸,会生成 和
和__________ (填化学式)。除去碳酸钠粉末中混有的少量碳酸氢钠,最好的方法是__________ 。
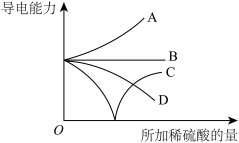
(6)向一定体积的 溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中
溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中__________ (填字母)所示。
(7)把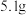 镁铝合金的粉末放入过量的盐酸中,充分反应后得到
镁铝合金的粉末放入过量的盐酸中,充分反应后得到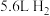 (标准状况),该合金中铝和镁的物质的量之比为
(标准状况),该合金中铝和镁的物质的量之比为__________ 。
(1)分类是认识和研究物质及其变化的一种常用的科学方法,如图所示分类方法是

(2)下列物质:①液氯 ②盐酸 ③
 ④硝酸钾固体 ⑤熔融
④硝酸钾固体 ⑤熔融 ⑥铜,其中属于电解质的是
⑥铜,其中属于电解质的是(3)
 所含化学键的类型
所含化学键的类型(4)氢化钠
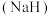 可在野外用作生氢剂,其原理为
可在野外用作生氢剂,其原理为 ,该反应的还原剂是
,该反应的还原剂是 转移的电子数目为
转移的电子数目为(5)碳酸钠是一种重要的化工基本原料,俗称
 和
和(6)向一定体积的
 溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中
溶液中逐滴加入稀硫酸至过量,混合溶液导电能力的变化如图中
(7)把
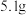 镁铝合金的粉末放入过量的盐酸中,充分反应后得到
镁铝合金的粉末放入过量的盐酸中,充分反应后得到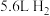 (标准状况),该合金中铝和镁的物质的量之比为
(标准状况),该合金中铝和镁的物质的量之比为
您最近一年使用:0次
6 . 二氧化氯 在工业上可用于淀粉及油脂的漂白及自来水的消毒,制备
在工业上可用于淀粉及油脂的漂白及自来水的消毒,制备 有以下两种方法。
有以下两种方法。
方法1:60℃时,用潮湿的氯酸钠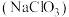 与草酸
与草酸 反应,反应原理为:
反应,反应原理为:
方法2:亚氯酸钠 和稀盐酸反应,反应原理为:
和稀盐酸反应,反应原理为: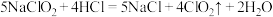
下列说法正确的是
 在工业上可用于淀粉及油脂的漂白及自来水的消毒,制备
在工业上可用于淀粉及油脂的漂白及自来水的消毒,制备 有以下两种方法。
有以下两种方法。方法1:60℃时,用潮湿的氯酸钠
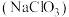 与草酸
与草酸 反应,反应原理为:
反应,反应原理为:
方法2:亚氯酸钠
 和稀盐酸反应,反应原理为:
和稀盐酸反应,反应原理为: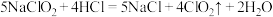
下列说法正确的是
A.方法1中 失去电子 失去电子 |
B.方法1中每生成 气体(换算成标准状况下),转移 气体(换算成标准状况下),转移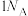 个电子 个电子 |
C.方法2中 是氧化剂, 是氧化剂, 是还原剂 是还原剂 |
D.方法2中氧化产物和还原产物的物质的量之比为 |
您最近一年使用:0次
名校
解题方法
7 . 已知氯气和 溶液在一温度下能发生化学反应,其方程式为:
溶液在一温度下能发生化学反应,其方程式为: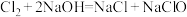
 ,
,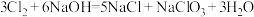 。某温度下,将氯气通入
。某温度下,将氯气通入 溶液中,反应得到
溶液中,反应得到 、
、 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数比为3:1,则氯气与氢氧化钠反应时,被氧化的氯原子和被还原的氯原子的个数比为
的个数比为3:1,则氯气与氢氧化钠反应时,被氧化的氯原子和被还原的氯原子的个数比为
 溶液在一温度下能发生化学反应,其方程式为:
溶液在一温度下能发生化学反应,其方程式为: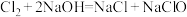
 ,
,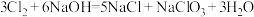 。某温度下,将氯气通入
。某温度下,将氯气通入 溶液中,反应得到
溶液中,反应得到 、
、 和
和 的混合溶液,经测定
的混合溶液,经测定 与
与 的个数比为3:1,则氯气与氢氧化钠反应时,被氧化的氯原子和被还原的氯原子的个数比为
的个数比为3:1,则氯气与氢氧化钠反应时,被氧化的氯原子和被还原的氯原子的个数比为| A.21:5 | B.1:2 | C.3:1 | D.2:1 |
您最近一年使用:0次
2022-12-23更新
|
138次组卷
|
2卷引用:重庆市乌江新高考协作体2023-2024学年高一下学期开学化学试题
名校
8 . 阿伏加德罗常数的值为 ,下列说法正确的是
,下列说法正确的是
 ,下列说法正确的是
,下列说法正确的是A.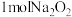 中阴离子个数为 中阴离子个数为 |
B. 铁在足量氧气中完全燃烧,转移的电子数为 铁在足量氧气中完全燃烧,转移的电子数为 |
C.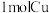 与 与 浓硫酸反应,生成 浓硫酸反应,生成 个 个 分子 分子 |
D.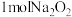 与足量 与足量 充分反应,转移的电子数为 充分反应,转移的电子数为 |
您最近一年使用:0次
2022-09-05更新
|
206次组卷
|
3卷引用:重庆市育才中学校2023届高三上学期开学测试化学试题
名校
解题方法
9 . 已知CaH2中Ca元素为+2价,对于反应CaH2+2H2O=Ca(OH)2+2H2↑,下列说法正确的是
| A.CaH2中H元素为+1价 |
| B.H2O发生氧化反应 |
| C.CaH2中的氢元素既被氧化又被还原 |
| D.H2中被氧化与被还原的原子的质量比为1∶1 |
您最近一年使用:0次
2022-07-08更新
|
2975次组卷
|
13卷引用:重庆两江新区西南大学附属中学校2023-2024学年高一下学期开学检测化学试题
重庆两江新区西南大学附属中学校2023-2024学年高一下学期开学检测化学试题重庆市南开中学2022-2023学年高一上学期12月定时练习化学试题(已下线)衔接点13 氧化还原反应的规律和表示方法-2022年初升高化学无忧衔接?(已下线)第一章《物质及其变化》基础过关单元检测-【帮课堂】2022-2023学年高一化学必修第一册精品讲义(人教版2019)北京市通州区2022-2023学年高一上学期期中考试化学试题河南省宜阳县第一高级中学2022-2023学年高一上学期期中考试化学试题山东省“学情空间”区域教研共同体2022-2023学年高一上学期12月联考(人教版) 化学试题河南省宜阳县第一高级中学2022-2023学年高一上学期期末考试化学试题(已下线)考点巩固卷02 化学物质及其变化(3大考点44题)?-2024年高考化学一轮复习考点通关卷(新高考通用)河北省石家庄市第十五中学2023-2024学年高一上学期第一次月考化学试题湖北省襄阳市第一中学2023-2024学年高一上学期9月月考化学试题广东省汕头市潮阳第一中学2023-2024学年高一上学期10月期中化学试题贵州省安顺市 镇宁布依族苗族自治县第一高级中学(镇宁实验学校)2023-2024学年高一上学期12月月考化学试题
10 . 铁是人体中必需微量元素中含量最多,体内缺失会引起贫血。含FeO 离子的盐具有强氧化性,容易被还原成Fe3+,高铁酸钾是一种新型、高效的消毒剂及绿色净水剂。
离子的盐具有强氧化性,容易被还原成Fe3+,高铁酸钾是一种新型、高效的消毒剂及绿色净水剂。
回答下列有关问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是___________(填字母)。
(2)硫酸铁可用于电化浸出黄铜矿精矿工艺。精矿在阳极浸出的反应比较复杂,其中有一主要反应:CuFeS2+4Fe3+=Cu2++5Fe2++2S。(CuFeS2中S为-2价)则下列说法正确的是___________ (选填序号);
(3)工业上常用KClO和KOH的混合液氧化FeCl3来制备K2FeO4
①实验室配制FeCl3溶液时,为了防止FeCl3水解需要将FeCl3溶于浓盐酸中,再加水稀释。现需配制90mL1mol/L的FeCl3溶液,需要用托盘天平称量___________ 克FeCl3•6H2O晶体。配制该溶液所需玻璃仪器有;烧杯,玻璃棒,量筒,___________ ;如果配制时,俯视定容,则所配溶液的浓度___________ (填偏大、偏小或无影响)
②请写出制备高铁酸钾的离子方程式:___________
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中既能杀菌消毒又能混凝净水,请简述原理___________ 。
 离子的盐具有强氧化性,容易被还原成Fe3+,高铁酸钾是一种新型、高效的消毒剂及绿色净水剂。
离子的盐具有强氧化性,容易被还原成Fe3+,高铁酸钾是一种新型、高效的消毒剂及绿色净水剂。 回答下列有关问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是___________(填字母)。
| A.亚硝酸盐被还原 | B.维生素C是还原剂 |
| C.维生素C将Fe3+还原为Fe2+ | D.亚硝酸盐是还原剂 |
| A.从物质分类的角度看,黄铜矿属于合金 |
| B.反应中,铁元素全部被还原 |
| C.反应中,CuFeS2 既作氧化剂又作还原剂 |
| D.当转移1mol电子时,46g CuFeS2参加反应 |
①实验室配制FeCl3溶液时,为了防止FeCl3水解需要将FeCl3溶于浓盐酸中,再加水稀释。现需配制90mL1mol/L的FeCl3溶液,需要用托盘天平称量
②请写出制备高铁酸钾的离子方程式:
(4)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中既能杀菌消毒又能混凝净水,请简述原理
您最近一年使用:0次



