1 . 高铁酸钠是一种新型绿色消毒剂,湿法制备高铁酸钠的化学原理可用化学方程式表示为: 。
。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。
。 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 在该反应中作氧化剂 在该反应中作氧化剂 |
B.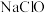 和 和 中均含离子键和极性键 中均含离子键和极性键 |
C. 溶液中含有 溶液中含有 的数目为 的数目为 |
D.当转移 时,生成的 时,生成的 中含有的孤电子对数为 中含有的孤电子对数为 |
您最近一年使用:0次
名校
2 . 红树林沉积物中微生物驱动的硫循环过程原理如图所示,在有氧层中有机物通过微生物有氧呼吸来分解,在无氧层中有机物通过微生物驱动硫酸盐还原来分解,下列说法错误的是
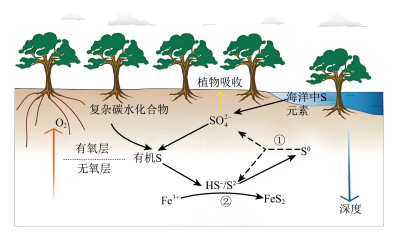
A.随着沉积物深度的增加, 主要做氧化剂将有机物氧化分解 主要做氧化剂将有机物氧化分解 |
B.反应①中氧化剂与还原剂的物质的量之比为 |
C.反应②中 与 与 的反应为 的反应为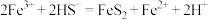 |
D.红树林沉积物中 元素主要以 元素主要以 形式存在 形式存在 |
您最近一年使用:0次
名校
3 . 黑火药配方“一硫二硝三木炭”的爆炸反应为: 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 。设
。设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A.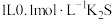 溶液中含 溶液中含 数目小于 数目小于 |
B. 含 含 键数目为 键数目为 |
C.每生成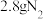 转移电子数目为 转移电子数目为 |
D.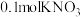 晶体中含 晶体中含 离子数目为 离子数目为 |
您最近一年使用:0次
名校
4 .  可用于玻璃和陶瓷的着色剂。由含钴可矿(
可用于玻璃和陶瓷的着色剂。由含钴可矿( 元素主要以
元素主要以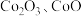 的形式存在,还含有
的形式存在,还含有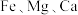 元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图所示:
元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图所示: 常用作食品抗氧化剂。
常用作食品抗氧化剂。
②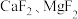 难溶于水。
难溶于水。
③部分金属阳离子形成氢氧化物沉淀的 如表所示:
如表所示:
回答下列问题:
(1)“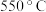 焙烧”的目的是
焙烧”的目的是__________________ 。
(2)“浸取”的过程中, 的主要作用是
的主要作用是__________________ (用离子方程式表示)。若用盐酸代替 和
和 的混合液也能达到目的,从环保角度分析不采用盐酸的原因
的混合液也能达到目的,从环保角度分析不采用盐酸的原因__________________ 。
(3)“滤液1”中加入 溶液,反应过程中氧化剂与还原剂的物质的量之比为
溶液,反应过程中氧化剂与还原剂的物质的量之比为_________ 。
(4)“滤渣2”的主要成分为_________ (填化学式)。
(5)已知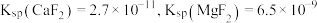 ,当
,当 恰好沉淀完全时(浓度为
恰好沉淀完全时(浓度为 ),溶液中
),溶液中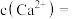
_________ (保留3位有效数字)。
(6)钴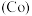 的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含
的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含 的水溶液制备金属钴的装置如图2、3所示。
的水溶液制备金属钴的装置如图2、3所示。 电极应连接乙醇燃料电池的
电极应连接乙醇燃料电池的_________ 极(填“a”或“b”)。
②电解过程中Ⅱ室溶液 变小,则离子交换膜2为
变小,则离子交换膜2为_________ (填“阴”或“阳”)离子交换膜。
 可用于玻璃和陶瓷的着色剂。由含钴可矿(
可用于玻璃和陶瓷的着色剂。由含钴可矿( 元素主要以
元素主要以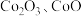 的形式存在,还含有
的形式存在,还含有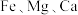 元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图所示:
元素,碳及有机物等)制取氯化钴晶体的一种工艺流程如图所示: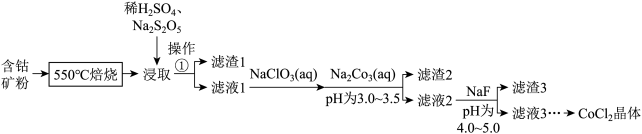
 常用作食品抗氧化剂。
常用作食品抗氧化剂。②
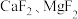 难溶于水。
难溶于水。③部分金属阳离子形成氢氧化物沉淀的
 如表所示:
如表所示:
|
|
|
|
| |
开始沉淀 | 0.3 | 2.7 | 7.2 | 7.6 | 9.6 |
完全沉淀 | 1.1 | 3.2 | 9.2 | 9.6 | 11.1 |
(1)“
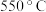 焙烧”的目的是
焙烧”的目的是(2)“浸取”的过程中,
 的主要作用是
的主要作用是 和
和 的混合液也能达到目的,从环保角度分析不采用盐酸的原因
的混合液也能达到目的,从环保角度分析不采用盐酸的原因(3)“滤液1”中加入
 溶液,反应过程中氧化剂与还原剂的物质的量之比为
溶液,反应过程中氧化剂与还原剂的物质的量之比为(4)“滤渣2”的主要成分为
(5)已知
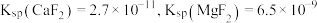 ,当
,当 恰好沉淀完全时(浓度为
恰好沉淀完全时(浓度为 ),溶液中
),溶液中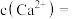
(6)钴
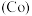 的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含
的合金材料广泛应用于航空航天、机械制造等领域。用乙醇燃料电池作为电源电解含 的水溶液制备金属钴的装置如图2、3所示。
的水溶液制备金属钴的装置如图2、3所示。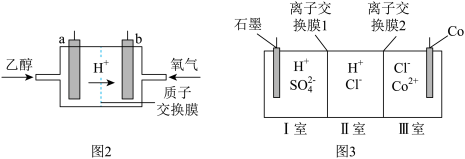
 电极应连接乙醇燃料电池的
电极应连接乙醇燃料电池的②电解过程中Ⅱ室溶液
 变小,则离子交换膜2为
变小,则离子交换膜2为
您最近一年使用:0次
名校
解题方法
5 . 利用甲烷可以除去 ,反应为
,反应为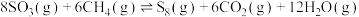 。下列说法正确的是
。下列说法正确的是
 ,反应为
,反应为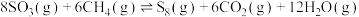 。下列说法正确的是
。下列说法正确的是A.上述反应的 |
B.上述反应的化学平衡常数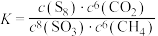 |
C.及时分离出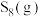 ,正反应速率增大,平衡向正反应方向移动 ,正反应速率增大,平衡向正反应方向移动 |
D.上述反应中生成1mol  ,转移电子的数目约为 ,转移电子的数目约为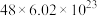 |
您最近一年使用:0次
6 . I.某些常见无机物质存在如图的化学转化关系(部分生成物和反应条件略去),回答下列问题:________ 。
(2)若甲是一种淡黄色固体,丙是一种温室气体,则X的化学式为________ ,当 甲和水生成乙和戊时,反应转移电子的物质的量为
甲和水生成乙和戊时,反应转移电子的物质的量为________ 。
(3)若甲是由两种常见的元素组成的化合物,乙是气体且水溶液呈碱性,X为大气中的一种主要成分,写出丁与水反应的化学方程式________ 。戊是氢氧化物,既能和强酸反应又能和强碱反应,则甲的化学式为________ 。
Ⅱ.固体化合物X由3种元素组成,其转化关系如图,混合气体经过无水 时,固体变蓝,碱性溶液焰色反应为黄色。回答下列问题:
时,固体变蓝,碱性溶液焰色反应为黄色。回答下列问题:____________ 。
(5)X的化学式为________ ,X能和浓盐酸反应生成黄绿色气体,X在反应中作________ (填“氧化剂”或“还原剂”),若反应了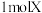 ,该反应转移电子的个数为
,该反应转移电子的个数为________ 。
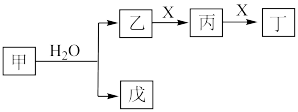
(2)若甲是一种淡黄色固体,丙是一种温室气体,则X的化学式为
 甲和水生成乙和戊时,反应转移电子的物质的量为
甲和水生成乙和戊时,反应转移电子的物质的量为(3)若甲是由两种常见的元素组成的化合物,乙是气体且水溶液呈碱性,X为大气中的一种主要成分,写出丁与水反应的化学方程式
Ⅱ.固体化合物X由3种元素组成,其转化关系如图,混合气体经过无水
 时,固体变蓝,碱性溶液焰色反应为黄色。回答下列问题:
时,固体变蓝,碱性溶液焰色反应为黄色。回答下列问题: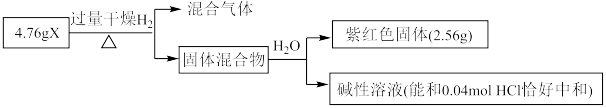
(5)X的化学式为
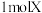 ,该反应转移电子的个数为
,该反应转移电子的个数为
您最近一年使用:0次
7 . 实验室可用干燥的氯气与亚氯酸钠 固体反应来制备
固体反应来制备 ,装置如图所示,已知
,装置如图所示,已知 常温下为黄绿色气体,熔点
常温下为黄绿色气体,熔点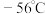 ,沸点
,沸点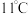 ,极易溶于水且不与水反应,高浓度的
,极易溶于水且不与水反应,高浓度的 受热时易爆炸,下列说法正确的是
受热时易爆炸,下列说法正确的是
 固体反应来制备
固体反应来制备 ,装置如图所示,已知
,装置如图所示,已知 常温下为黄绿色气体,熔点
常温下为黄绿色气体,熔点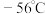 ,沸点
,沸点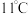 ,极易溶于水且不与水反应,高浓度的
,极易溶于水且不与水反应,高浓度的 受热时易爆炸,下列说法正确的是
受热时易爆炸,下列说法正确的是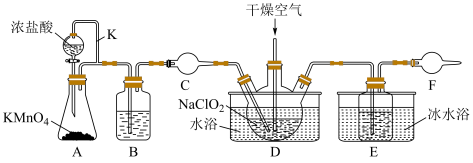
| A.导气管K的作用是平衡气压,保证液体顺利流下 |
| B.C和F中可选用同一种物质 |
C.D中通入一定量的干燥空气,目的主要是将生成的 带入到E中,便于收集. 带入到E中,便于收集. |
D.D中发生的化学反应中氧化剂与还原剂的物质的量之比为 |
您最近一年使用:0次
8 . 利用某钒废渣(主要成分为V2O4以及铁、铝、硅的氧化物)制备V2O5的工艺流程如下: 溶于酸后以
溶于酸后以 的形式存在;
的形式存在; 可将
可将 氧化为
氧化为 ;
;
Ⅱ.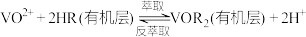 。
。
下列说法正确的是

 溶于酸后以
溶于酸后以 的形式存在;
的形式存在; 可将
可将 氧化为
氧化为 ;
;Ⅱ.
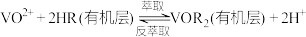 。
。下列说法正确的是
A.滤渣1的主要成分为 |
B. 的作用只是将 的作用只是将 氧化成 氧化成 |
| C.反萃取剂显强酸性 |
| D.“氧化2”中氧化剂与还原剂的物质的量之比为1∶3 |
您最近一年使用:0次
9 . 金属钛(Ti)具有许多优异的性能,是航空、军工、电力等领域的必需材料。以金红石为原料制取金属钛,其中发生的化学反应之一:

(1)作还原剂的物质是_______ ,钛元素的化合价_______ (填“升高”或“降低”)。
(2)若反应中消耗了2molMg,则生成Ti的物质的量为_______ mol,转移电子的物质的量为_______ mol。

(1)作还原剂的物质是
(2)若反应中消耗了2molMg,则生成Ti的物质的量为
您最近一年使用:0次
名校
10 . 二氯化二硫( )是一种常用的橡胶硫化剂,其结构如图所示。
)是一种常用的橡胶硫化剂,其结构如图所示。 极易水解:
极易水解: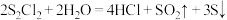 。下列说法错误的是
。下列说法错误的是
 )是一种常用的橡胶硫化剂,其结构如图所示。
)是一种常用的橡胶硫化剂,其结构如图所示。 极易水解:
极易水解: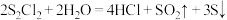 。下列说法错误的是
。下列说法错误的是
A. 中S为+1价 中S为+1价 |
B. 是由非极性键与极性键构成的极性分子 是由非极性键与极性键构成的极性分子 |
C.上述反应中 既作氧化剂又作还原剂 既作氧化剂又作还原剂 |
| D.上述反应中氧化产物与还原产物的质量比为3:1 |
您最近一年使用:0次





