名校
解题方法
1 . 钪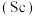 是一种功能强大的稀土金属,广泛用于航天、激光、导弹等尖端科学领域。
是一种功能强大的稀土金属,广泛用于航天、激光、导弹等尖端科学领域。
钛铁矿主要成分为钛酸亚铁 ,还含有少量
,还含有少量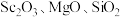 等杂质,从钛铁矿中提取
等杂质,从钛铁矿中提取 的流程如下图:
的流程如下图:
(1)“滤渣”的主要成分是___________ 。
(2)“酸浸”后,钛主要以 的形式存在于溶液中,
的形式存在于溶液中, 在一定条件下可完全水解生成
在一定条件下可完全水解生成 ,写出
,写出 水解的离子方程式:
水解的离子方程式:___________ 。
(3)“萃取”是用酸性磷酸酯萃取剂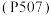 、苯乙酮、磺化煤油配成的混合液作萃取剂,
、苯乙酮、磺化煤油配成的混合液作萃取剂,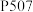 质量分数
质量分数 对萃取率的影响如表所示,料液温度对分离系数的影响如图所示,则萃取时
对萃取率的影响如表所示,料液温度对分离系数的影响如图所示,则萃取时 最佳质量分数及料液温度分别为
最佳质量分数及料液温度分别为___________ 。(已知分离系数指分离后混合体系中某物质的物质的量分数,如 的分离系数
的分离系数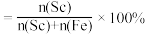 )
)
 ”时,若调
”时,若调 前溶液中
前溶液中 浓度为
浓度为 ,先加氨水调节
,先加氨水调节 ,则
,则 的去除率为
的去除率为___________ (忽略调 前后溶液的体积变化);过滤除去
前后溶液的体积变化);过滤除去 ,再向滤液中加入氨水调节
,再向滤液中加入氨水调节 ,此时滤液中
,此时滤液中 的浓度为
的浓度为___________  。(已知
。(已知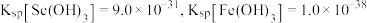 )
)
(5)“沉钪”时发生反应: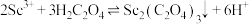 ,该反应的平衡常数
,该反应的平衡常数
___________ (用数字列式表示,不用计算结果)(已知草酸的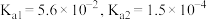 ;
;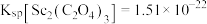 )。
)。
(6)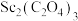 在空气中“焙烧”时生成
在空气中“焙烧”时生成 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
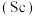 是一种功能强大的稀土金属,广泛用于航天、激光、导弹等尖端科学领域。
是一种功能强大的稀土金属,广泛用于航天、激光、导弹等尖端科学领域。钛铁矿主要成分为钛酸亚铁
 ,还含有少量
,还含有少量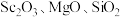 等杂质,从钛铁矿中提取
等杂质,从钛铁矿中提取 的流程如下图:
的流程如下图:
(1)“滤渣”的主要成分是
(2)“酸浸”后,钛主要以
 的形式存在于溶液中,
的形式存在于溶液中, 在一定条件下可完全水解生成
在一定条件下可完全水解生成 ,写出
,写出 水解的离子方程式:
水解的离子方程式:(3)“萃取”是用酸性磷酸酯萃取剂
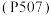 、苯乙酮、磺化煤油配成的混合液作萃取剂,
、苯乙酮、磺化煤油配成的混合液作萃取剂,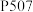 质量分数
质量分数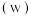 对萃取率的影响如表所示,料液温度对分离系数的影响如图所示,则萃取时
对萃取率的影响如表所示,料液温度对分离系数的影响如图所示,则萃取时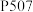 最佳质量分数及料液温度分别为
最佳质量分数及料液温度分别为 的分离系数
的分离系数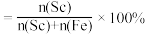 )
) /% /% | 分相情况 | 钪萃取率/% | 铁萃取率/% |
| 1 | 分相容易 | 90.74 | 14.89 |
| 2 | 分相容易 | 91.74 | 19.88 |
| 3 | 分相容易 | 92.14 | 13.30 |
| 5 | 有第三相 | 90.59 | 28.47 |
| 8 | 轻微乳化 | 90.59 | 34.85 |

 ”时,若调
”时,若调 前溶液中
前溶液中 浓度为
浓度为 ,先加氨水调节
,先加氨水调节 ,则
,则 的去除率为
的去除率为 前后溶液的体积变化);过滤除去
前后溶液的体积变化);过滤除去 ,再向滤液中加入氨水调节
,再向滤液中加入氨水调节 ,此时滤液中
,此时滤液中 的浓度为
的浓度为 。(已知
。(已知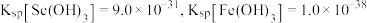 )
)(5)“沉钪”时发生反应:
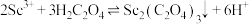 ,该反应的平衡常数
,该反应的平衡常数
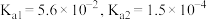 ;
;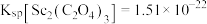 )。
)。(6)
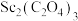 在空气中“焙烧”时生成
在空气中“焙烧”时生成 ,该反应的化学方程式为
,该反应的化学方程式为
您最近一年使用:0次
2024高三·全国·专题练习
名校
2 . 回答下列问题:
(1)随着钴酸锂电池的普及使用,从废旧的钴酸锂电池中提取锂、钴等金属材料意义重大。下图是废旧钴酸锂电池材料(主要成分为LiCoO2,含少量铁、铝、铜等元素的化合物)回收工艺流程:_______ 。
②滤液1中加入Na2SO3的主要目的是_______ ,加入NaClO3的主要目的是_______ 。
③“沉钴”过程中,(NH4)2C2O4的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示: )∶n(Co2+)为1.15的原因是
)∶n(Co2+)为1.15的原因是_______ ,温度高于50℃,钴的沉淀率降低的原因是_______ 。
(2)亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:_______ 。
②采取“减压蒸发”而不用“常压蒸发”,原因是_______ 。
③“反应2”中使用H2O2而不用其他物质的原因是_______ 。
(1)随着钴酸锂电池的普及使用,从废旧的钴酸锂电池中提取锂、钴等金属材料意义重大。下图是废旧钴酸锂电池材料(主要成分为LiCoO2,含少量铁、铝、铜等元素的化合物)回收工艺流程:

②滤液1中加入Na2SO3的主要目的是
③“沉钴”过程中,(NH4)2C2O4的加入量(图甲)、沉淀反应的温度(图乙)与钴的沉淀率关系如图所示:

 )∶n(Co2+)为1.15的原因是
)∶n(Co2+)为1.15的原因是(2)亚氯酸钠(NaClO2)具有强氧化性,受热易分解,可作漂白剂、食品消毒剂等。以氯酸钠等为原料制备亚氯酸钠的工艺流程如下:

②采取“减压蒸发”而不用“常压蒸发”,原因是
③“反应2”中使用H2O2而不用其他物质的原因是
您最近一年使用:0次
名校
解题方法
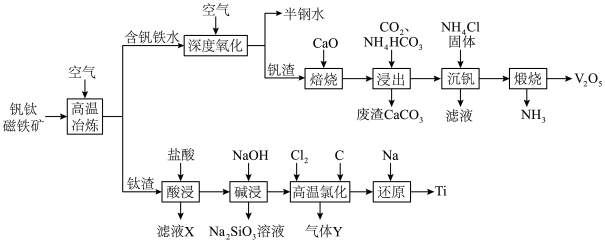
3 . 稀有金属钒和钛在钢铁、化工、航空航天等领域应用广泛。从钒钛磁铁矿中提取钒、钛的工艺流程图如下: 、
、 、
、 和
和 等。
等。
②“高温氯化”后的产物中含少量的 、
、 、
、 、
、 杂质,相关物质的沸点如下表:
杂质,相关物质的沸点如下表:
回答下列问题:
(1)钛在周期表中的位置为___________ ,上述获得钛单质的“还原”工序中需要通入氩气的目的是___________ 。
(2)滤液X中含有的主要金属离子有___________ 。
(3)“高温氯化”工序生成 和一种可燃性气体Y,该反应的化学方程式为
和一种可燃性气体Y,该反应的化学方程式为___________ ; 的粗产品可以通过分馏提纯,但收集的
的粗产品可以通过分馏提纯,但收集的 中总是混有
中总是混有 的原因是
的原因是___________ 。
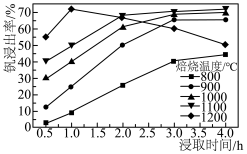
(4)钒的浸出率随焙烧温度和浸取时间的变化如图所示,则“焙烧”时最适合的反应条件为___________ 。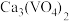 转化成
转化成 进入水相,以便后续沉钒,则“浸出”时反应的离子方程式为
进入水相,以便后续沉钒,则“浸出”时反应的离子方程式为___________ 。
(6)采用USTB工艺电解制备高纯钛,过程以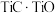 固体为阳极、碳棒为阴极,
固体为阳极、碳棒为阴极, 熔融盐为电解质。阳极产生
熔融盐为电解质。阳极产生 与
与 ,阴极只发生
,阴极只发生 的还原反应。请写出电池阳极反应的电极反应式:
的还原反应。请写出电池阳极反应的电极反应式:___________ 。
 、
、 、
、 和
和 等。
等。②“高温氯化”后的产物中含少量的
 、
、 、
、 、
、 杂质,相关物质的沸点如下表:
杂质,相关物质的沸点如下表:| 化合物 |  |  |  |  |  |
| 沸点/℃ | 136 | 310 | 56.5 | 180 | 127 |
(1)钛在周期表中的位置为
(2)滤液X中含有的主要金属离子有
(3)“高温氯化”工序生成
 和一种可燃性气体Y,该反应的化学方程式为
和一种可燃性气体Y,该反应的化学方程式为 的粗产品可以通过分馏提纯,但收集的
的粗产品可以通过分馏提纯,但收集的 中总是混有
中总是混有 的原因是
的原因是(4)钒的浸出率随焙烧温度和浸取时间的变化如图所示,则“焙烧”时最适合的反应条件为
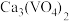 转化成
转化成 进入水相,以便后续沉钒,则“浸出”时反应的离子方程式为
进入水相,以便后续沉钒,则“浸出”时反应的离子方程式为(6)采用USTB工艺电解制备高纯钛,过程以
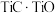 固体为阳极、碳棒为阴极,
固体为阳极、碳棒为阴极, 熔融盐为电解质。阳极产生
熔融盐为电解质。阳极产生 与
与 ,阴极只发生
,阴极只发生 的还原反应。请写出电池阳极反应的电极反应式:
的还原反应。请写出电池阳极反应的电极反应式:
您最近一年使用:0次
2024-04-22更新
|
470次组卷
|
4卷引用:2024届河北省邢台市部分高中高三下学期二模化学试题
名校
4 . 下列反应对应的离子方程式正确的是
A.乙酰胺与盐酸混合共热: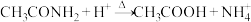 |
B.硫化钠溶液在空气中氧化变质: |
C.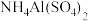 溶液与足量 溶液与足量 溶液反应: 溶液反应: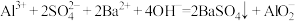 |
D.证明 、 、 、 、 三者的酸性强弱: 三者的酸性强弱: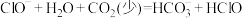 |
您最近一年使用:0次
2024-04-22更新
|
480次组卷
|
2卷引用:2024届河北省邢台市部分高中高三下学期二模化学试题
解题方法
5 . 某煤矸石经化学成分分析可知,其含有大量的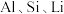 元素,还含有少量
元素,还含有少量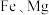 等杂质。下图为硝酸浸出铝、铁、锂等工业流程。按要求回答下列问题:
等杂质。下图为硝酸浸出铝、铁、锂等工业流程。按要求回答下列问题: 的操作是
的操作是______ 。
(2)富铁渣中的主要成分是______ (填化学式)。
(3)低温热解过程中有红棕色气体放出,则铝盐发生反应的化学方程式为______ (假设热解过程中只有一种含氮化合物生成);此时热解温度不宜过高的原因是______ 。
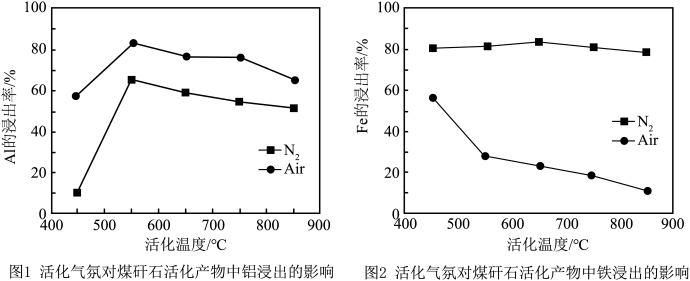
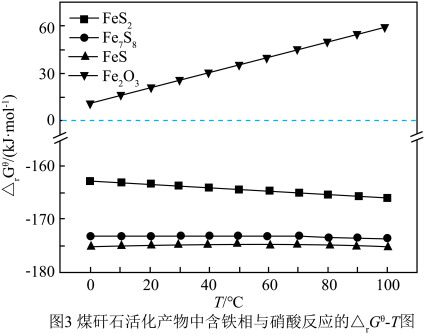
(4)热活化过程可在氮气或空气气氛中进行,其活化气氛在不同温度下对铝(图1)、铁(图2)浸出的影响,以及铁的活化产物与硝酸反应的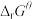 与温度的关系(图3)如下图所示。则热活化过程所选用的合适的条件是
与温度的关系(图3)如下图所示。则热活化过程所选用的合适的条件是______ (填标号)。
A. 气氛、
气氛、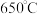 B.空气气氛、
B.空气气氛、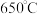 C.
C. 气氛、
气氛、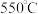 D.空气气氛、
D.空气气氛、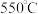
空气气氛中温度越高,铁的浸出率越小的原因可能是______ 。 )和碳酸酯类有机溶剂组成,充电过程中,石墨
)和碳酸酯类有机溶剂组成,充电过程中,石墨 电极发生阴离子插层反应得
电极发生阴离子插层反应得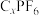 。则碳酸酯类为
。则碳酸酯类为______ (填“极性”或“非极性”)溶剂,放电时,正极发生的电极反应方程式为______ 。
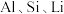 元素,还含有少量
元素,还含有少量 等杂质。下图为硝酸浸出铝、铁、锂等工业流程。按要求回答下列问题:
等杂质。下图为硝酸浸出铝、铁、锂等工业流程。按要求回答下列问题: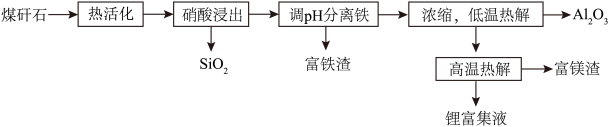
 的操作是
的操作是(2)富铁渣中的主要成分是
(3)低温热解过程中有红棕色气体放出,则铝盐发生反应的化学方程式为
(4)热活化过程可在氮气或空气气氛中进行,其活化气氛在不同温度下对铝(图1)、铁(图2)浸出的影响,以及铁的活化产物与硝酸反应的
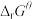 与温度的关系(图3)如下图所示。则热活化过程所选用的合适的条件是
与温度的关系(图3)如下图所示。则热活化过程所选用的合适的条件是A.
 气氛、
气氛、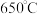 B.空气气氛、
B.空气气氛、 C.
C. 气氛、
气氛、 D.空气气氛、
D.空气气氛、
空气气氛中温度越高,铁的浸出率越小的原因可能是
 )和碳酸酯类有机溶剂组成,充电过程中,石墨
)和碳酸酯类有机溶剂组成,充电过程中,石墨 电极发生阴离子插层反应得
电极发生阴离子插层反应得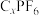 。则碳酸酯类为
。则碳酸酯类为
您最近一年使用:0次
6 . Ⅰ.高铁酸钾(K2FeO4) 是一种高效、无毒的强氧化剂,常温下为紫色固体,微溶于浓KOH溶液,能溶于水,且能与水反应放出氧气,并生成Fe(OH)3胶体。稳定性随pH的下降而减弱,酸性条件下易分解。
(1)下列有关铁及其化合物的性质与用途具有对应关系的是___________
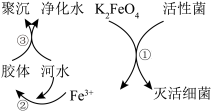
Ⅱ.K2FeO4的净水原理如图所示:
(2)下列说法错误的是___________
(3)写出K2FeO4与水反应的化学方程式___________ 。
Ⅲ.已知可用Cl2与Fe(NO3)3制备K2FeO4(含副产品KCl、KNO3),查阅资料得知高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:
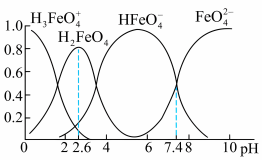
(4)①为获得尽可能纯净的高铁酸盐,pH应控制在___________ 。
②写出在此条件下,反应的离子方程式:___________ ;每生成39.6g K2FeO4,转移的电子数目为___________ ;
(5)已知溶液的酸碱性及离子浓度会对反应试剂的氧化性、还原性产生影响。
某实验小组研究不同反应试剂对K2FeO4产率的影响,对比实验如下:
注:上述实验中,溶液总体积、FeCl3和Fe(NO3)3的物质的量、Cl2的通入量均相同。
①由实验I、II的现象可知,Fe3+的还原性随溶液碱性的增强而___________ (填“增强”、“减弱”或“不变”);
②实验II中K2FeO4的产率比实验III低,试解释其可能的原因:___________ ;
③向实验II所得紫色溶液中继续通入Cl2,观察到溶液紫色变浅,试解释其可能的原因:___________ 。
(6)实验室测定含少量杂质的K2FeO4样品的纯度:称取0.1500g K2FeO4样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用0.1000 mol·L−1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液25.00 mL。滴定时,发生反应的离子方程式:FeO + 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O
+ 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O = S4O
= S4O + 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:
+ 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:___________ (写出计算过程)。
(1)下列有关铁及其化合物的性质与用途具有对应关系的是___________
| A.铁粉具有还原性,可防止食物氧化变质 | B.高铁酸钾能溶于水,可作氧化剂 |
| C.氢氧化铁胶体具有碱性,可用于净水 | D.纯铁无杂质,可用作建筑材料 |
Ⅱ.K2FeO4的净水原理如图所示:

(2)下列说法错误的是___________
| A.K2FeO4中铁元素显+6价 |
| B.过程①中K2FeO4被细菌还原 |
| C.过程②中的Fe(OH)3胶体粒子带正电荷 |
| D.过程③中聚沉是由于胶体发生了渗析 |
(3)写出K2FeO4与水反应的化学方程式
Ⅲ.已知可用Cl2与Fe(NO3)3制备K2FeO4(含副产品KCl、KNO3),查阅资料得知高铁酸盐在水溶液中有四种含铁形体。25℃时,它们的物质的量分数随pH的变化如图所示:

(4)①为获得尽可能纯净的高铁酸盐,pH应控制在
②写出在此条件下,反应的离子方程式:
(5)已知溶液的酸碱性及离子浓度会对反应试剂的氧化性、还原性产生影响。
某实验小组研究不同反应试剂对K2FeO4产率的影响,对比实验如下:
| 实验编号 | 反应试剂 | 实验现象 |
| Ⅰ | Cl2、FeCl3和少量KOH | 无明显现象 |
| Ⅱ | Cl2、FeCl3和过量KOH | 得到紫色溶液,无紫色固体 |
| Ⅲ | Cl2、Fe(NO3)3和过量KOH | 得到紫色溶液(颜色比Ⅱ深),有紫色固体 |
①由实验I、II的现象可知,Fe3+的还原性随溶液碱性的增强而
②实验II中K2FeO4的产率比实验III低,试解释其可能的原因:
③向实验II所得紫色溶液中继续通入Cl2,观察到溶液紫色变浅,试解释其可能的原因:
(6)实验室测定含少量杂质的K2FeO4样品的纯度:称取0.1500g K2FeO4样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用0.1000 mol·L−1的Na2S2O3标准溶液进行滴定,消耗Na2S2O3标准溶液25.00 mL。滴定时,发生反应的离子方程式:FeO
 + 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O
+ 4I−+ 8H+= Fe2+ + 2I2+ 4H2O;I2 + 2S2O = S4O
= S4O + 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:
+ 2I−。已知:M(K2FeO4) =198g·mol−1,试计算K2FeO4样品的纯度:
您最近一年使用:0次
7 . 从废旧磷酸铁锂电极材料(LiFePO4、导电石墨、铝箔)中回收锂的工艺流程如图,下列说法错误的是
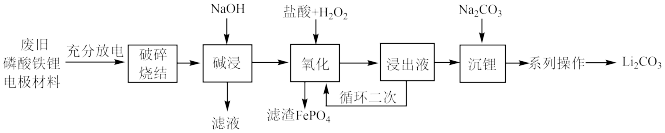
| A.旧电池拆解前进行充分放电是因为放电可使Li+在负极富集 |
| B.“氧化”时,H2O2可用KClO3代替 |
| C.“氧化”时发生的化学反应方程式为:2LiFePO4+H2O2+2HCl=2LiCl+2FePO4+2H2O |
| D.“系列操作”具体包括水浴加热、趁热过滤、洗涤、干燥 |
您最近一年使用:0次
2024-03-21更新
|
393次组卷
|
3卷引用:山东省济宁市2024届高三下学期一模考试化学试题
8 . 低碳经济已成为人们一种新的生活理念,二氧化碳的捕捉和利用是能源领域的一个重要研究方向。回答下列问题:
(1)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
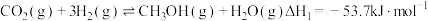
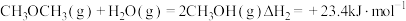
则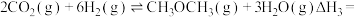
_______ kJ∙mol-1。
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: ,则
,则 的化学式为
的化学式为_______ ,“热分解系统”中每转移 电子,需消耗
电子,需消耗
_______  。
。
(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子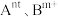 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示:_______ 。
ii.“高温相”具有良好的离子导电性,其主要原因是_______ 。
(4)铜基催化剂 (
( 为
为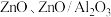 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 上发生反应的总化学方程式
上发生反应的总化学方程式_______ 。
(5)利用电解法在碱性或酸性条件下将 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: 和法拉第效率(
和法拉第效率(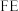 )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下:
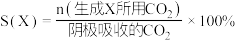

①实验测得,碱性条件生成 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是_______ 。
②实验测得,酸性条件生成 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是_______ 。
(1)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: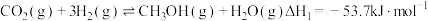
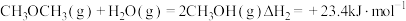
则
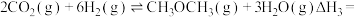
(2)二氧化碳的捕集、利用是我国能源领域的一个重要战略方向。科学家提出由
 制取
制取 的太阳能工艺如图:
的太阳能工艺如图: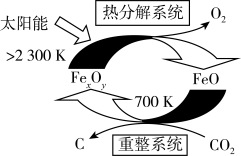
 ,则
,则 的化学式为
的化学式为 电子,需消耗
电子,需消耗
 。
。(3)催化时还可以使用一种无机固体电解质作催化剂,其由正离子
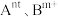 和负离子
和负离子 组成,该物质
组成,该物质 以上形成无序结构(高温相),
以上形成无序结构(高温相), 以下变为有序结构(低温相),二者晶体晶胞结构如图所示:
以下变为有序结构(低温相),二者晶体晶胞结构如图所示: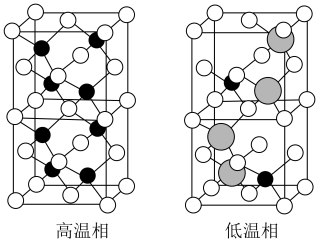
说明:图中,○球为负离子;高温相中的●深色球为正离子或空位;低温相中的 球为
球为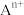 离子,●球为
离子,●球为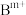 离子。
离子。
ii.“高温相”具有良好的离子导电性,其主要原因是
(4)铜基催化剂
 (
( 为
为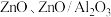 等)是
等)是 加氢制甲醇常用的催化剂,部分合成路线如图所示。
加氢制甲醇常用的催化剂,部分合成路线如图所示。 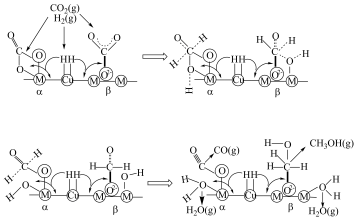
 上发生反应的总化学方程式
上发生反应的总化学方程式(5)利用电解法在碱性或酸性条件下将
 还原为
还原为 和
和 的原理如下图所示:
的原理如下图所示: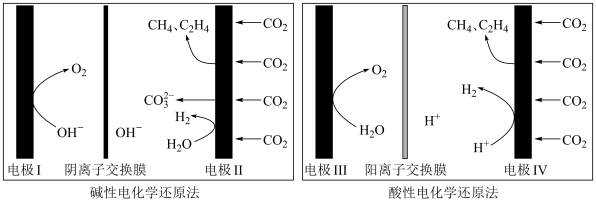
 和法拉第效率(
和法拉第效率(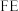 )的定义(X代表
)的定义(X代表 或
或 )如下:
)如下: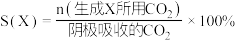

①实验测得,碱性条件生成
 总的选择性小于酸性条件,原因是
总的选择性小于酸性条件,原因是②实验测得,酸性条件生成
 总的法拉第效率小于碱性条件,原因是
总的法拉第效率小于碱性条件,原因是
您最近一年使用:0次
2024-03-11更新
|
427次组卷
|
4卷引用:江苏省常州市第一中学2023-2024学年高三下学期期初检测化学试卷
江苏省常州市第一中学2023-2024学年高三下学期期初检测化学试卷(已下线)大题预测卷(江西专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)江苏省扬州中学2024届高三下学期考前模拟化学试题江苏省常州市第一中2023-2024学年高二下学期5月月考化学试题
23-24高一上·全国·期末
名校
9 . 氯气和漂白粉是现代工业和生活中常用的杀菌消毒剂,以下为制备两种消毒剂的方法,请回答下列问题:
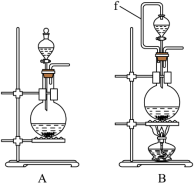
(1)实验室沿用舍勒的方法制取 时选用图中装置
时选用图中装置_______ (填“A”或“B”),反应的离子方程式为_______ ,装置B中管f的作用是_______ 。
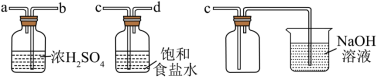
(2)实验室制取干燥、纯净的 ,所需图装置的接口连接顺序为:发生装置→
,所需图装置的接口连接顺序为:发生装置→_______ (填字母)。
(3)反应停止后,实验小组检验烧瓶中还有 和盐酸。小组同学探究不继续产生
和盐酸。小组同学探究不继续产生 的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
【提出猜想】
猜想1: 降低,氧化剂
降低,氧化剂_______ (填化学式)氧化性减弱。
猜想2:_______ 减弱。
猜想3: 增大,氧化剂氧化性减弱。
增大,氧化剂氧化性减弱。
【实验过程】向反应后剩余物质中加入以下物质,请补充表格:
【实验拓展】经过探究,小组同学认为硫酸、 固体和
固体和 混合加热也可制取
混合加热也可制取 。请配平该反应的方程式:
。请配平该反应的方程式:_______ 。
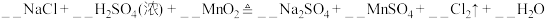
(1)实验室沿用舍勒的方法制取
 时选用图中装置
时选用图中装置
(2)实验室制取干燥、纯净的
 ,所需图装置的接口连接顺序为:发生装置→
,所需图装置的接口连接顺序为:发生装置→
(3)反应停止后,实验小组检验烧瓶中还有
 和盐酸。小组同学探究不继续产生
和盐酸。小组同学探究不继续产生 的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。
的原因。查阅资料表明,反应物或生成物浓度会影响氧化剂、还原剂的氧化性、还原性强弱。【提出猜想】
猜想1:
 降低,氧化剂
降低,氧化剂猜想2:
猜想3:
 增大,氧化剂氧化性减弱。
增大,氧化剂氧化性减弱。【实验过程】向反应后剩余物质中加入以下物质,请补充表格:
| 序号 | 实验操作 | 有、无氯气 | 结论 |
| 1 | 加入浓硫酸,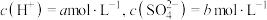 | 有氯气 | 猜想1正确 |
| 2 | 加入氯化钠固体,使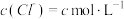 | 有氯气 | 猜想2正确 |
| 3 | 加入浓硫酸和 固体,使 固体,使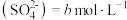 | 猜想3正确 |
 固体和
固体和 混合加热也可制取
混合加热也可制取 。请配平该反应的方程式:
。请配平该反应的方程式: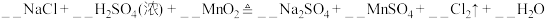
您最近一年使用:0次
2024-01-07更新
|
667次组卷
|
4卷引用:江西省上饶市清源学校2023-2024学年高三上学期12月考试化学试题
江西省上饶市清源学校2023-2024学年高三上学期12月考试化学试题(已下线)期末测试卷01-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册) 2023-2024学年高一上学期化学人教版(2019)必修第一册 期末综合测试题(一)河南省新乡市原阳县第一高级中学2023-2024学年高一上学期1月月考化学试题
名校
解题方法
10 . 镍、钴是重要的战略物资,但资源匮乏。一种利用酸浸出法从冶金厂废炉渣中提取镍和钴的工艺流程如下:
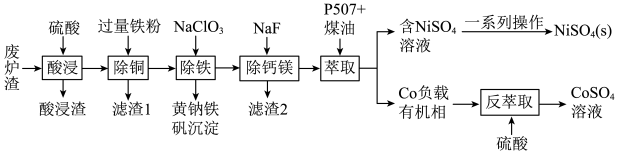
已知:i.酸浸液中的金属阳离子有Ni2+、Co2+、Cu2+、Mg2+、Ca2+等
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)“滤渣1”的主要成分是___________ 。(写化学式)
(2)黄钠铁矾的化学式为Na2Fe6(SO4)4(OH)12,“除铁”的离子方程式为___________ 。
(3)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是___________ (结合平衡理论解释)。Ca2+和Mg2+沉淀完全时,溶液中F-的浓度c(F-)最小为___________ mol·L-1。[已知离子浓度≤10-5mol/L时,认为该离子沉淀完全,Ksp(CaF2)=1.0×10-10(mol/L)3,Ksp(MgF2)=7.5×10-11(mol/L)3]
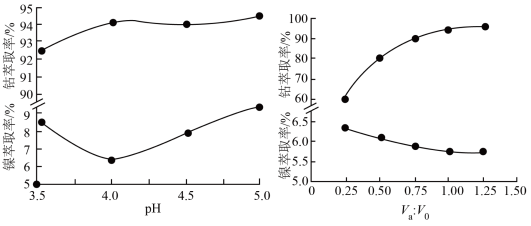
(4)镍、钴萃取率与料液pH、萃取剂体积与料液体积比Va:V0的关系曲线如下图所示,则“萃取”时应选择的pH和Va:V0分别为___________ 、___________ 。
(5)获得NiSO4(s)的“一系列操作”是___________ 。
(6)该工艺流程中,可循环利用的物质是___________ 。

已知:i.酸浸液中的金属阳离子有Ni2+、Co2+、Cu2+、Mg2+、Ca2+等
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)“滤渣1”的主要成分是
(2)黄钠铁矾的化学式为Na2Fe6(SO4)4(OH)12,“除铁”的离子方程式为
(3)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是
(4)镍、钴萃取率与料液pH、萃取剂体积与料液体积比Va:V0的关系曲线如下图所示,则“萃取”时应选择的pH和Va:V0分别为

(5)获得NiSO4(s)的“一系列操作”是
(6)该工艺流程中,可循环利用的物质是
您最近一年使用:0次
2023-12-27更新
|
605次组卷
|
4卷引用:山东省实验中学2023-2024学年高三上学期11月二诊化学试题
山东省实验中学2023-2024学年高三上学期11月二诊化学试题山东省淄博市部分学校2023-2024学年高三上学期联考化学试卷(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)广东省深圳市实验学校高中部2023-2024学年高二上学期第三阶段考试化学试题



