名校
1 . 菱锌矿(主要成分是 ,还含有MnO、FeO、
,还含有MnO、FeO、 、
、 等杂质)是制取锌单质的重要原料。回答下列问题:
等杂质)是制取锌单质的重要原料。回答下列问题:
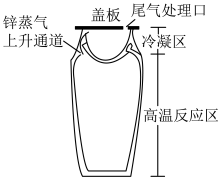
(1)古代以菱锌矿和煤炭饼为原料利用热还原法在如图所示的坩埚中制备Zn。
①该方法中,将菱锌矿敲碎与煤饼混合,此操作的主要目的是_______ 。
②图中盖板除了防止锌蒸气外逸外,另一主要作用是_______ ,尾气中含有CO,处理尾气的方法是_______ 。
(2)现代以菱锌矿为原料利用湿法冶炼锌主要分为如下五个步骤。
步骤1:用稀硫酸充分浸取菱锌矿:
步骤2:在步骤1的滤液中加入适量 除去其中的
除去其中的 ;
;
步骤3:在步骤2的滤液中加入试剂R调节溶液pH除去 ;
;
步骤4:经操作X从步骤3的滤液中获得 晶体:
晶体:
步骤5:将 溶于水配成饱和溶液,电解该饱和溶液得到Zn。
溶于水配成饱和溶液,电解该饱和溶液得到Zn。
①步骤1中用稀硫酸浸取后,所得滤渣的主要成分是_______ (填化学式)。
②步骤2中 与
与 反应生成
反应生成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:_______ 。
③为获得更多产品,步骤3中使用的试剂R应选择_______ (填字母)。
A. B.澄清石灰水 C.ZnO D.
B.澄清石灰水 C.ZnO D.
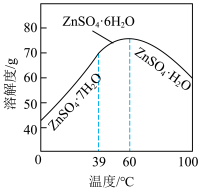
④温度与析出 的关系如图所示,则步骤4中操作X的具体操作是
的关系如图所示,则步骤4中操作X的具体操作是_______ 、冰水洗涤、干燥。
 ,还含有MnO、FeO、
,还含有MnO、FeO、 、
、 等杂质)是制取锌单质的重要原料。回答下列问题:
等杂质)是制取锌单质的重要原料。回答下列问题:
(1)古代以菱锌矿和煤炭饼为原料利用热还原法在如图所示的坩埚中制备Zn。
①该方法中,将菱锌矿敲碎与煤饼混合,此操作的主要目的是
②图中盖板除了防止锌蒸气外逸外,另一主要作用是
(2)现代以菱锌矿为原料利用湿法冶炼锌主要分为如下五个步骤。
步骤1:用稀硫酸充分浸取菱锌矿:
步骤2:在步骤1的滤液中加入适量
 除去其中的
除去其中的 ;
;步骤3:在步骤2的滤液中加入试剂R调节溶液pH除去
 ;
;步骤4:经操作X从步骤3的滤液中获得
 晶体:
晶体:步骤5:将
 溶于水配成饱和溶液,电解该饱和溶液得到Zn。
溶于水配成饱和溶液,电解该饱和溶液得到Zn。①步骤1中用稀硫酸浸取后,所得滤渣的主要成分是
②步骤2中
 与
与 反应生成
反应生成 ,写出该反应的离子方程式:
,写出该反应的离子方程式:③为获得更多产品,步骤3中使用的试剂R应选择
A.
 B.澄清石灰水 C.ZnO D.
B.澄清石灰水 C.ZnO D.
④温度与析出
 的关系如图所示,则步骤4中操作X的具体操作是
的关系如图所示,则步骤4中操作X的具体操作是
您最近一年使用:0次
2023-10-20更新
|
89次组卷
|
4卷引用:甘肃省武威市多校联考2024届高三上学期9月质量检测化学试题
名校
2 . 下列离子方程式书写正确的是
A. 溶于足量稀 溶于足量稀 中: 中: |
B. 溶于中加入 溶于中加入 溶液: 溶液: |
C. 溶液中通入少量 溶液中通入少量 : :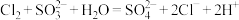 |
D.向 溶液中通入足量 溶液中通入足量 : :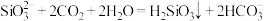 |
您最近一年使用:0次
2023-10-19更新
|
245次组卷
|
4卷引用:甘肃省武威市凉州区2024届高三第三次诊断考试化学试题
名校
解题方法
3 . 回答下列问题:
I.KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(1)请用“双线桥”表示上述反应电子转移的方向和数目_______ 。
(2)请将上述反应改写成离子方程式________ 。
(3)浓盐酸在反应中体现出来的性质有______ (填序号)。
①还原性 ②酸性 ③氧化性 ④碱性
(4)若反应生成21.3g氯气,则消耗还原剂的质量为______ g。
II.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是______ 。(填化学式)
(6)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:________ 。
②每生成1个FeO 转移
转移______ 个电子。
I.KClO3和浓盐酸在一定温度下反应会生成黄绿色的有毒气体氯气。其变化可表示为:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
(1)请用“双线桥”表示上述反应电子转移的方向和数目
(2)请将上述反应改写成离子方程式
(3)浓盐酸在反应中体现出来的性质有
①还原性 ②酸性 ③氧化性 ④碱性
(4)若反应生成21.3g氯气,则消耗还原剂的质量为
II.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(5)干法制备高铁酸钠的主要反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中还原剂是
(6)湿法制备高铁酸钾(K2FeO4)是在碱性环境中进行,反应体系中有六种反应微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①请依据上述信息,写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成1个FeO
 转移
转移
您最近一年使用:0次
名校
解题方法
4 . 亚硝酸钠( )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性。由于
,其水溶液呈碱性。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: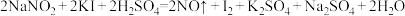
(1)在下面方框中写出氧化剂和还原剂的化学式及其系数,并用单线桥法标出电子转移的方向和数目:______

(2)从物质分类角度来看, 是
是___________ (填字母代号)。
a.酸 b.盐 c.碱 d.非电解质 e.电解质
(3)用上述反应来处理 并不是最佳方法,其原因是
并不是最佳方法,其原因是___________ 。从环保角度来讲,要将 转化为氮气,所用物质的
转化为氮气,所用物质的___________ (填“氧化性”或“还原性”)应该比KI更___________ (填“强”或“弱”)。
(4)下列方法不能用来区分固体 和NaCl的是
和NaCl的是___________ (填序号)。
A.分别溶于水,并滴加几滴酚酞溶液
B.分别加强热并收集气体检验
C.用筷子分别蘸取固体品尝味道
(5)误食 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列___________(填序号)反应中
表现出的性质与下列___________(填序号)反应中 表现出的性质相同。
表现出的性质相同。
(6)已知亚硝酸钠可以与氯化铵反应生成氮气和氯化钠,写出该反应的化学反应方程式:___________ ,产生氮气分子和转移电子数目比为:___________ 。
 )是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生
)是一种用途广泛的工业盐,因其外观和食盐相似容易误食中毒。亚硝酸钠加热到320℃以上会分解产生 、
、 和
和 ,其水溶液呈碱性。由于
,其水溶液呈碱性。由于 有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下:
有毒性,将含该物质的废水直接排放会引起水体严重污染,所以这种废水必须处理后才能排放。处理方法之一如下: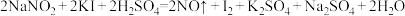
(1)在下面方框中写出氧化剂和还原剂的化学式及其系数,并用单线桥法标出电子转移的方向和数目:

(2)从物质分类角度来看,
 是
是a.酸 b.盐 c.碱 d.非电解质 e.电解质
(3)用上述反应来处理
 并不是最佳方法,其原因是
并不是最佳方法,其原因是 转化为氮气,所用物质的
转化为氮气,所用物质的(4)下列方法不能用来区分固体
 和NaCl的是
和NaCl的是A.分别溶于水,并滴加几滴酚酞溶液
B.分别加强热并收集气体检验
C.用筷子分别蘸取固体品尝味道
(5)误食
 会导致人体血红蛋白中的
会导致人体血红蛋白中的 转化为
转化为 而中毒,该过程中
而中毒,该过程中 表现出的性质与下列___________(填序号)反应中
表现出的性质与下列___________(填序号)反应中 表现出的性质相同。
表现出的性质相同。A. |
B. |
C. |
D.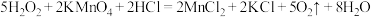 |
您最近一年使用:0次
名校
5 . 几种中学化学常见的单质及其化合物相互转化的关系如图:
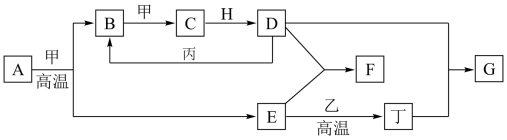
已知:
①甲、乙、丙、丁为单质,乙中元素在地壳中的含量占第三位,丙为红色固体,其余为化合物。
②A由X和Y两种元素组成,其原子个数比为1∶2,元素质量之比为7∶8。
③H常温下为无色、无味的液体,E常用作油漆、涂料的红色颜料。
回答下列问题:
(1)高温下,A和甲反应生成B和E的化学方程式为___________ ,每生成1 mol B,转移___________ mol电子。
(2)F的水溶液与丁单质反应也可以生成G,反应的离子方程式为___________ 。
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①②③。
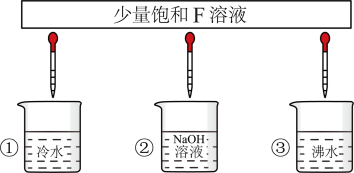
分散系②是___________ (填“胶体”“悬浊液”“乳浊液”或“溶液”),能鉴别分散系①③的实验现象称为___________ 。
(4)一定条件下,丙和D反应生成B的化学方程式为___________ 。

已知:
①甲、乙、丙、丁为单质,乙中元素在地壳中的含量占第三位,丙为红色固体,其余为化合物。
②A由X和Y两种元素组成,其原子个数比为1∶2,元素质量之比为7∶8。
③H常温下为无色、无味的液体,E常用作油漆、涂料的红色颜料。
回答下列问题:
(1)高温下,A和甲反应生成B和E的化学方程式为
(2)F的水溶液与丁单质反应也可以生成G,反应的离子方程式为
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①②③。

分散系②是
(4)一定条件下,丙和D反应生成B的化学方程式为
您最近一年使用:0次
名校
解题方法
6 . 工业综合处理含NH 废水和含N2、CO2、SO2、NO、CO的废气,得到无毒气体b,流程如下:
废水和含N2、CO2、SO2、NO、CO的废气,得到无毒气体b,流程如下:
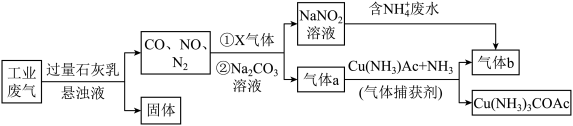
下列说法正确的是
 废水和含N2、CO2、SO2、NO、CO的废气,得到无毒气体b,流程如下:
废水和含N2、CO2、SO2、NO、CO的废气,得到无毒气体b,流程如下:
下列说法正确的是
| A.“固体”中含有CaSO4、CaSO3和CaCO3 |
B.X气体、NO与Na2CO3溶液的离子反应:4NO+O2+CO = 4NO = 4NO +CO2 +CO2 |
C.处理含NH 的废水时,离子方程式为NH 的废水时,离子方程式为NH +NO +NO = N2↑+2H2O = N2↑+2H2O |
| D.捕获剂捕获气体a中发生络合反应Cu(NH3)Ac+CO+NH3=Cu(NH3)3COAc |
您最近一年使用:0次
名校
7 . 根据所学知识,回答下列问题:
(1)现有下列物质:①熔融的 ②液态
②液态 ③蔗糖 ④银 ⑤
③蔗糖 ④银 ⑤ 溶液 ⑥稀硫酸 ⑦
溶液 ⑥稀硫酸 ⑦ ⑧
⑧ 晶体
晶体
其中属于电解质的是___________ ;属于非电解质的是___________ ;能导电的有___________ ;
(2)按要求填空。
① 溶液(写出电离方程式)
溶液(写出电离方程式)___________ 。
②纯碱和澄清石灰水反应(写出离子方程式)___________ 。
(3)配平下列氧化还原方程式:
①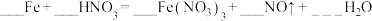
________ ;
②
________ 。
(1)现有下列物质:①熔融的
 ②液态
②液态 ③蔗糖 ④银 ⑤
③蔗糖 ④银 ⑤ 溶液 ⑥稀硫酸 ⑦
溶液 ⑥稀硫酸 ⑦ ⑧
⑧ 晶体
晶体其中属于电解质的是
(2)按要求填空。
①
 溶液(写出电离方程式)
溶液(写出电离方程式)②纯碱和澄清石灰水反应(写出离子方程式)
(3)配平下列氧化还原方程式:
①
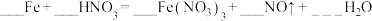
②

您最近一年使用:0次
8 . NaHSO3是常见的亚硫酸盐,在潮湿的空气中易被氧化,在工业生产和实验室都有着广泛的应用。为探究NaHSO3溶液的性质,甲同学配制了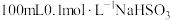 溶液。做了如下实验:
溶液。做了如下实验:
(1)配制溶液需用到的玻璃仪器有玻璃棒、量筒、烧杯、_____ 、_____ 。
(2)常温下,用pH计测量新配制的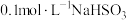 溶液的pH,测得pH约为4.1。
溶液的pH,测得pH约为4.1。
①若在实验室用pH试纸测量溶液的pH,其简单操作为_____ 。
②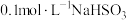 溶液呈酸性,说明H2SO3的第二步电离常数Ka2
溶液呈酸性,说明H2SO3的第二步电离常数Ka2_____ (填“>”、“<”或“=”) 的第二步水解常数
的第二步水解常数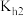 。
。
(3)将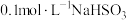 溶液与
溶液与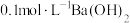 溶液等体积混合,产生白色沉淀,写出等物质的量的NaHSO3与Ba(OH)2在溶液中发生反应的离子方程式:
溶液等体积混合,产生白色沉淀,写出等物质的量的NaHSO3与Ba(OH)2在溶液中发生反应的离子方程式:_____ 。
探究白色沉淀的成分:
提出猜想:
a.只有BaSO3 b.只有BaSO4 c._____
验证猜想:
乙同学认为猜想b不正确,原因为_____
将白色沉淀加入足量盐酸中,若有气泡生成,且沉淀全部溶解,证明猜想a正确;若_____ ,证明猜想c正确。
(4)将 溶液和Na2S溶液混合,再滴入适量稀H2SO4,有淡黄色浑浊物出现。写出该反应的离子方程式:
溶液和Na2S溶液混合,再滴入适量稀H2SO4,有淡黄色浑浊物出现。写出该反应的离子方程式:_____ 。该现象说明NaHSO3溶液具有_____ (填“氧化性”、“还原性”或“氧化性和还原性”)。
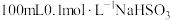 溶液。做了如下实验:
溶液。做了如下实验:(1)配制溶液需用到的玻璃仪器有玻璃棒、量筒、烧杯、
(2)常温下,用pH计测量新配制的
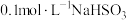 溶液的pH,测得pH约为4.1。
溶液的pH,测得pH约为4.1。①若在实验室用pH试纸测量溶液的pH,其简单操作为
②
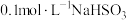 溶液呈酸性,说明H2SO3的第二步电离常数Ka2
溶液呈酸性,说明H2SO3的第二步电离常数Ka2 的第二步水解常数
的第二步水解常数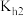 。
。(3)将
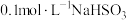 溶液与
溶液与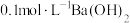 溶液等体积混合,产生白色沉淀,写出等物质的量的NaHSO3与Ba(OH)2在溶液中发生反应的离子方程式:
溶液等体积混合,产生白色沉淀,写出等物质的量的NaHSO3与Ba(OH)2在溶液中发生反应的离子方程式:探究白色沉淀的成分:
提出猜想:
a.只有BaSO3 b.只有BaSO4 c.
验证猜想:
乙同学认为猜想b不正确,原因为
将白色沉淀加入足量盐酸中,若有气泡生成,且沉淀全部溶解,证明猜想a正确;若
(4)将
 溶液和Na2S溶液混合,再滴入适量稀H2SO4,有淡黄色浑浊物出现。写出该反应的离子方程式:
溶液和Na2S溶液混合,再滴入适量稀H2SO4,有淡黄色浑浊物出现。写出该反应的离子方程式:
您最近一年使用:0次
2023-10-02更新
|
96次组卷
|
2卷引用:广东省东莞市部分名校高三上(9月联考)-化学试题
名校
解题方法
9 . 以黄铜矿( )为主要原料的炼铜方法之一是生物浸出法:在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
)为主要原料的炼铜方法之一是生物浸出法:在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
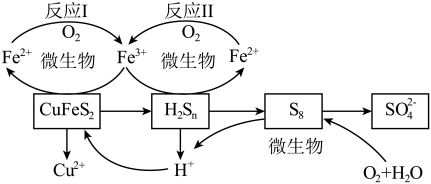
下列说法不正确的是
 )为主要原料的炼铜方法之一是生物浸出法:在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
)为主要原料的炼铜方法之一是生物浸出法:在反应釜中加入黄铜矿、硫酸铁、硫酸和微生物,并鼓入空气,黄铜矿逐渐溶解,反应釜中各物质的转化关系如图所示。
下列说法不正确的是
A.反应Ⅰ、Ⅱ中的离子方程式均为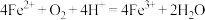 |
| B.此浸出过程,温度越高,浸出率越高 |
C.在微生物的作用下,可以循环使用的物质有 和 和 |
D.假如黄铜矿中的铁元素最终全部转化为 ,当有 ,当有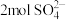 生成时,理论上消耗 生成时,理论上消耗 的物质的量为 的物质的量为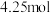 |
您最近一年使用:0次
2023-09-24更新
|
144次组卷
|
3卷引用:甘肃省张掖市高台县第一中学2023-2024学年高三上学期9月月考化学试题
名校
解题方法
10 . 硫酸铝在造纸、水净化、土壤改良中有着广泛应用。某化工厂利用含铅废料(成分为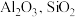 及少量
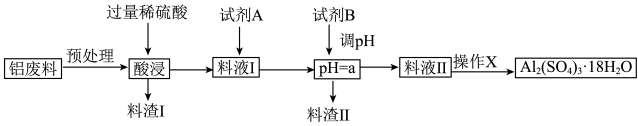
及少量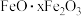 )制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
)制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
已知生成氢氧化物沉淀的 如下表:
如下表:
(1)“预处理”时需要将铝废料粉碎,目的是_______ 。
(2)料渣Ⅰ的成分是_______ ,酸浸时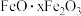 发生反应的离子方程式为
发生反应的离子方程式为_______ 。
(3)试剂 是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式
是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式_______ 。
(4) 的范围是
的范围是_______ ,试剂B最好是_______ ,目的是_______ 。(用离子方程式和必要的文字描述)
(5)操作 的内容是
的内容是_______ 、过滤、洗涤、干燥等。
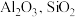 及少量
及少量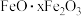 )制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
)制备硫酸铝晶体的工艺流程如下图所示,回答相关问题。
已知生成氢氧化物沉淀的
 如下表:
如下表: |  |  | |
开始沉淀时 | 3.6 | 6.3 | 2.3 |
完全沉淀时 | 4.9 | 8.3 | 3.2 |
(2)料渣Ⅰ的成分是
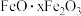 发生反应的离子方程式为
发生反应的离子方程式为(3)试剂
 是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式
是一种液态绿色氧化剂,料液Ⅰ中反应的离子方程式(4)
 的范围是
的范围是(5)操作
 的内容是
的内容是
您最近一年使用:0次



