名校
解题方法
1 . 从干海带中提取碘的实验流程如下:
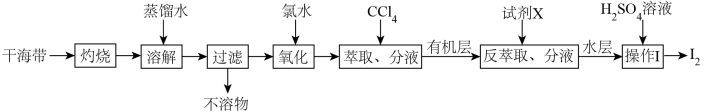
| A.氧化步骤中氯水可用过氧化氢代替 |
B.试剂X可以为 ,反萃取的离子方程式为: ,反萃取的离子方程式为: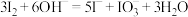 |
C. 可循环利用以有效提高干海带提碘的产率 可循环利用以有效提高干海带提碘的产率 |
| D.操作Ⅰ要用到普通漏斗、烧杯和玻璃棒 |
您最近一年使用:0次
2024-01-28更新
|
573次组卷
|
6卷引用:湖南省岳阳市 岳阳县第一中学2023-2024学年高一下学期开学化学试题
名校
解题方法
2 . 国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)发电玻璃被誉为“挂在墙上的油田”。一种以镉废渣(含 及少量
及少量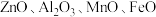 杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
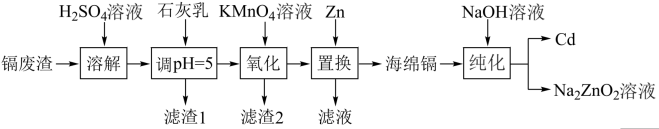
已知:部分金属阳离子以氢氧化物形式沉淀时溶液的 如下表所示:
如下表所示:
 及少量
及少量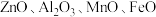 杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
杂质)为原料制备镉的工艺流程如图所示,下列说法错误的是
已知:部分金属阳离子以氢氧化物形式沉淀时溶液的
 如下表所示:
如下表所示:| 金属阳离子 |  |  |  |
开始沉淀时的 | 2.7 | 6.3 | 3.4 |
完全沉淀时的 | 3.2 | 8.3 | 5.0 |
A.滤渣1的主要成分是 |
B. 置换之后的滤液主要成分是 置换之后的滤液主要成分是 和 和 |
C.“纯化”过程中发生的反应为 |
| D.该工艺用到的主要分离操作是过滤 |
您最近一年使用:0次
2023-11-23更新
|
573次组卷
|
4卷引用:湖南省长沙市周南教育集团2023-2024学年高二下学期入学考试化学试题
3 . 四氧化三钴主要用作催化剂、氧化剂,也可用于制造钴盐、搪瓷颜料。某钴矿中含CoS、CuS、FeS,以该钴矿为原料制备四氧化三钴的工艺流程如图所示:

已知:①P5O7萃取剂的结构简式:
②Co2+沉淀的pH范围为6.7~8.7。
③pH=4~6时,Fe3+水解生成复杂的胶粒:Fe(OH)3·2nFe3+·3(n-x)
回答下列问题:
(1)Co在元素周期表中的位置为___________ ,其基态原子的价层电子轨道表示式为___________ 。
(2)可以电解含[Cu(NH3)4]2+的溶液制备金属铜,阴极的电极反应式为___________ 。
(3)写出“除硫”操作中FeS参加反应的化学方程式:___________ 。
(4)“除铁”时加入NaClO3的作用是___________ ;该操作中,pH影响到除铁率和Co的回收率,二者与溶液pH的关系如图所示,则pH>4时,随pH增大,Co的回收率快速下降的原因是_______ 。

(5)下列有关P507萃取剂的结构和性质的说法错误的是___________(填序号)。
(6)相比含Co2+溶液的pH,“萃取”后“水层1”的pH___________ (填“不变”“减小”或“增大”)。

已知:①P5O7萃取剂的结构简式:

②Co2+沉淀的pH范围为6.7~8.7。
③pH=4~6时,Fe3+水解生成复杂的胶粒:Fe(OH)3·2nFe3+·3(n-x)

回答下列问题:
(1)Co在元素周期表中的位置为
(2)可以电解含[Cu(NH3)4]2+的溶液制备金属铜,阴极的电极反应式为
(3)写出“除硫”操作中FeS参加反应的化学方程式:
(4)“除铁”时加入NaClO3的作用是

(5)下列有关P507萃取剂的结构和性质的说法错误的是___________(填序号)。
| A.难溶于水,能溶于有机溶剂 | B.1molP507含2mol手性碳原子 |
| C.常温常压下是无色气体 | D.碳原子均为sp3杂化 |
您最近一年使用:0次
名校
4 . 由软锰矿(主要成分 MnO2,及少量 CaO、MgO)制备 MnO2的工艺流程如下:

已知:“沉锰”所得 MnCO3在空气中“焙烧”时转化为 MnO2、Mn2O3、MnO 的混合物。下列说法正确的是

已知:“沉锰”所得 MnCO3在空气中“焙烧”时转化为 MnO2、Mn2O3、MnO 的混合物。下列说法正确的是
A.“浸取”时发生的主要反应离子方程式  |
B.“除杂”后的溶液中主要存在的阳离子有  |
C.“沉锰”时反应的离子方程式为  |
| D.“酸浸”时,每反应 2mol Mn2O3转移电子的物质的量为 6 mol |
您最近一年使用:0次
名校
5 . B、Al、Ga位于元素周期表中ⅢA族。 为无色气体,主要用作有机合成中的催化剂,极易水解生成
为无色气体,主要用作有机合成中的催化剂,极易水解生成 (
( 在水中完全电离为
在水中完全电离为 和
和 )和硼酸(
)和硼酸( )。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯
)。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯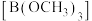 ,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下
,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下 和焦炭在氯气的氛围中获得
和焦炭在氯气的氛围中获得 。GaN的结构与晶体硅类似,是第三代半导体研究的热点。下列化学反应表示
。GaN的结构与晶体硅类似,是第三代半导体研究的热点。下列化学反应表示不正确 的是
 为无色气体,主要用作有机合成中的催化剂,极易水解生成
为无色气体,主要用作有机合成中的催化剂,极易水解生成 (
( 在水中完全电离为
在水中完全电离为 和
和 )和硼酸(
)和硼酸( )。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯
)。硼酸是一元弱酸,能溶于水,硼酸和甲醇在浓硫酸存在下生成挥发性的硼酸甲酯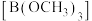 ,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下
,硼酸甲酯主要用作热稳定剂、木材防腐剂等。高温下 和焦炭在氯气的氛围中获得
和焦炭在氯气的氛围中获得 。GaN的结构与晶体硅类似,是第三代半导体研究的热点。下列化学反应表示
。GaN的结构与晶体硅类似,是第三代半导体研究的热点。下列化学反应表示A.制备 : : |
B. 和NaOH溶液反应: 和NaOH溶液反应: |
C.高温下 、焦炭在氯气中反应: 、焦炭在氯气中反应: |
D.电解 (熔融)制备Al的阳极反应: (熔融)制备Al的阳极反应: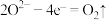 |
您最近一年使用:0次
2023-09-07更新
|
127次组卷
|
2卷引用:湖南省岳阳市第一中学2023-2024学年高三下学期开学化学试题
名校
解题方法
6 . 某实验小组利用如图装置模拟古法制硫酸并进行 SO2性质探究。
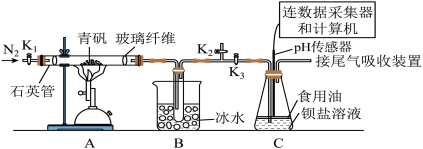
已知:①“青矾”是指FeSO4 7H2O ,高温受热可完全分解得红棕色固体和气体混合物;
②SO2熔点-75.5℃,沸点-10℃:SO3熔点 16.8℃,沸点 44.8℃。请回答下列问题:
I.制取硫酸,实验开始前打开活塞 K1、K2,关闭活塞 K3,通入一段时间 N2后,关闭活塞 K1、K2,打开活塞 K3,用酒精喷灯高温加热青矾。
(1)A 装置中发生反应的化学方程式为___________ 。
(2)B 装置的作用是___________ 和分离出___________ (填化学式)。
(3)实验结束后,打开活塞 K1,再通入一段时间 N2,这样做的目的是___________ 。
Ⅱ.探究 SO2的性质
在装置 C 中先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入 SO2流速一致。四次实验分别得到如表 pH-t 图:
(4)C 装置中覆盖食用油的目的是___________ 。
(5)分析 pH-t 图,写出③中发生反应的离子方程式___________ , 上述四次实验中有白色沉淀生成的是___________ (填编号)。

已知:①“青矾”是指FeSO4 7H2O ,高温受热可完全分解得红棕色固体和气体混合物;
②SO2熔点-75.5℃,沸点-10℃:SO3熔点 16.8℃,沸点 44.8℃。请回答下列问题:
I.制取硫酸,实验开始前打开活塞 K1、K2,关闭活塞 K3,通入一段时间 N2后,关闭活塞 K1、K2,打开活塞 K3,用酒精喷灯高温加热青矾。
(1)A 装置中发生反应的化学方程式为
(2)B 装置的作用是
(3)实验结束后,打开活塞 K1,再通入一段时间 N2,这样做的目的是
Ⅱ.探究 SO2的性质
在装置 C 中先后四次加入同浓度同体积不同情况的钡盐溶液,控制食用油油层厚度一致、通入 SO2流速一致。四次实验分别得到如表 pH-t 图:
| ① | ② | ③ | ④ |
| 已煮沸的 BaCl2(aq) | 未煮沸的 BaCl2(aq) | 已煮沸的 Ba(NO3)2(aq) | 未煮沸的 Ba(NO3)2(aq) |
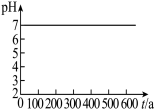 |  |  | 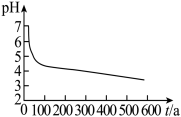 |
(4)C 装置中覆盖食用油的目的是
(5)分析 pH-t 图,写出③中发生反应的离子方程式
您最近一年使用:0次
2023-09-04更新
|
170次组卷
|
2卷引用:湖南省衡阳市第八中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
7 . 氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系:
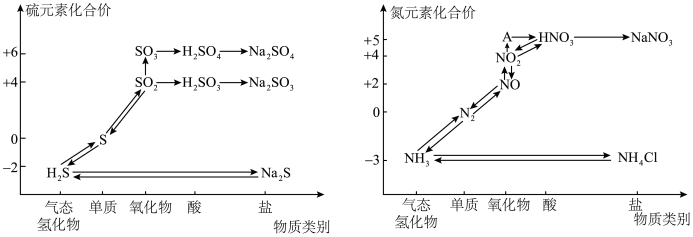
(1)根据 A 对应的化合价和物质类别,A 为___________ (写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的含氮化合物有___________ 。
(2)氮气的结构决定了氮气能够在空气中稳定存在,实验室可用加热 NaNO2与NH4Cl 的混合溶液制备N2,请写出反应的化学方程式___________ 。
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择___________ ,反应的离子方程式为___________ 。
(4)工业生产中利用氨水吸收SO2 和NO2 ,原理如图所示:
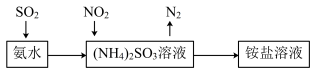
NO2 被吸收过程的离子方程式是___________ 。

(1)根据 A 对应的化合价和物质类别,A 为
(2)氮气的结构决定了氮气能够在空气中稳定存在,实验室可用加热 NaNO2与NH4Cl 的混合溶液制备N2,请写出反应的化学方程式
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层应选择
(4)工业生产中利用氨水吸收SO2 和NO2 ,原理如图所示:

NO2 被吸收过程的离子方程式是
您最近一年使用:0次
名校
解题方法
8 . 我国已成为氟最大产销国。由于其产品具有高附加值,其氟化工也被称之为“黄金产业”。
I.从氟硅酸(H2SiF6)制备氟化钙的流程如图:

(1)该工艺流程中可以循环使用的物质是_______ 。
(2)聚四氟乙烯反应釜中发生反应的化学方程式为_______ 。
II.氟化钙与浓硫酸反应可以制取HF,电子级HF是半导体材料的重要原材料。其中电子级HF的制取工艺流程如图:

(3)精制HF过程中,用高锰酸钾溶液(氧化剂)进行化学预处理,将AsF3氧化,氧化得到的物质AsF5与HF沸点相差较大,可以在后续精馏过程中除去。其化学处理的离子方程式为_______ 。
(4)氢氟酸是弱酸, ,Ka=6.3×10-3,当其浓度大于5.0mol/L时,溶液的酸性变强,试从结构的角度分析其可能的原因是
,Ka=6.3×10-3,当其浓度大于5.0mol/L时,溶液的酸性变强,试从结构的角度分析其可能的原因是_______ 。
(5)氟化钙的晶胞如图所示,则钙离子的配位数为_______ ,若晶胞参数为acm,则该晶体的密度为_______ g·cm-3(设CaF2的摩尔质量为Mg/mol)。
I.从氟硅酸(H2SiF6)制备氟化钙的流程如图:

(1)该工艺流程中可以循环使用的物质是
(2)聚四氟乙烯反应釜中发生反应的化学方程式为
II.氟化钙与浓硫酸反应可以制取HF,电子级HF是半导体材料的重要原材料。其中电子级HF的制取工艺流程如图:

(3)精制HF过程中,用高锰酸钾溶液(氧化剂)进行化学预处理,将AsF3氧化,氧化得到的物质AsF5与HF沸点相差较大,可以在后续精馏过程中除去。其化学处理的离子方程式为
(4)氢氟酸是弱酸,
 ,Ka=6.3×10-3,当其浓度大于5.0mol/L时,溶液的酸性变强,试从结构的角度分析其可能的原因是
,Ka=6.3×10-3,当其浓度大于5.0mol/L时,溶液的酸性变强,试从结构的角度分析其可能的原因是(5)氟化钙的晶胞如图所示,则钙离子的配位数为

您最近一年使用:0次
名校
解题方法
9 . PH3常作为一种熏蒸剂,在贮粮中用于防治害虫,一种制备PH3的流程如图所示:
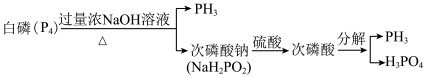
下列说法正确的是

下列说法正确的是
| A.流程中,每一步均属于氧化还原反应 |
| B.次磷酸的分子式为H3PO2,属于三元酸 |
C.白磷与浓NaOH溶液反应的化学方程式为:P4+3NaOH(浓)+3H2O PH3↑+3NaH2PO2 PH3↑+3NaH2PO2 |
| D.理论上,1 mol白磷可生产2.0 mol PH3 |
您最近一年使用:0次
2023-07-21更新
|
1036次组卷
|
9卷引用:湖南省长沙市雅礼中学2023-2024学年高二上学期入学考试化学试题
湖南省长沙市雅礼中学2023-2024学年高二上学期入学考试化学试题山东省德州市第一中学2023-2024学年高三上学期开学考试化学试题重庆育才中学2022届高考适应性考试二化学试题甘肃省天水市一中2021-2022学年高三上学期第二次阶段考试化学试题(已下线)考点01 物质的分类和转化-备战2023年高考化学一轮复习考点帮(全国通用)重庆市石柱中学校2021-2022学年高三上学期第四次月考化学试题(已下线)考点01 物质的分类和转化(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)湖北省黄石市第二中学2023-2024学年高二上学期9月月考化学试题安徽省淮北市树人高级中学2023-2024学年高一上学期11月考试化学试题
名校
解题方法
10 . 下列反应的离子方程式正确的是
A.用 溶液吸收 溶液吸收 制石膏乳: 制石膏乳: |
B.向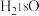 中投入 中投入 固体: 固体: |
C.向 溶液通入 溶液通入 : :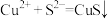 |
D.利用 和浓盐酸反应制备 和浓盐酸反应制备 : :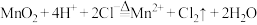 |
您最近一年使用:0次
2023-07-11更新
|
863次组卷
|
2卷引用:湖南省长沙麓山国际实验学校2023-2024学年高二上学期入学考试化学试题



